The overview of the most important vitreomacular diseases – diagnostic and therapeutic innovations
doi: 10.55342/szemhungarica.2026.163.1.2
Original scientific paper
Summary
The development of multimodal imaging and the evolution of vitrectomy devices and instruments have revolutionized macular surgery and induced changes affecting our present issues. The use of more detailed, pathomechanism revealing diagnostic tools has refined the planning of surgical approach, improving the prognosis of diseases. The aim of this article is to present the diagnostic steps and current classification of the most important vitreomacular pathologies: epiretinal membranes, partial-thickness and full-thickness macular holes, and to describe the latest surgical techniques associated with them.
Összefoglaló
A multimodális képalkotás megjelenése és a vitrectomiás eszközök, műszerek fejlődése forradalmasította a makulasebészetet, valamint napjainkban is ható változásokat indukál. A részletgazdagabb, a patomechanizmust is feltáró diagnosztikus eszközök használatával finomodott a sebészi megközelítés tervezése, folyamatosan javítva ezzel a betegségek prognózisát. Jelen cikk célja a legfontosabb vitreomakuláris kórképek: az epiretinális membránok, a részleges és a teljes vastagságú makulalyukak diagnosztikus lépéseinek, aktuális klasszifikációjának bemutatása, és a hozzájuk kapcsolódó legújabb sebészi technikák ismertetése.Keywords
vitreomacular traction, lamellar macular hole, epiretinal proliferation, macular pseudohole, epiretinal membrane, full-thickness macular hole
Kulcsszavak
vitreomakuláris trakció, lamelláris makulalyuk, epiretinális proliferáció, makuláris pszeudoforámen, epiretinális membrán, teljes vastagságú makulalyuk
Bevezetés
Makulasebészet alatt a központi retina, a hátsó pólus közvetlen, invazív sebészi manipulációját értjük. Robert Machemer zseniális újítása a pars plana vitrectomia (PPV) megjelenése után néhány évvel már fellelhető a makulasebészet irodalmi említése is (33), elsősorban proliferatív diabéteszes retinopátia és proliferatív vitreoretinopátia sebészi kezelésének részeként. Ekkor vált ismertté, hogy a foveát érintő trakció megszüntetése strukturális eredmények mellett látásjavulást is eredményezhet. Az 1980-as évek végén fontos mérföldkő volt a hátsó üvegtesti határhártya leválasztása (Han és mtsai), a vitreomakuláris trakció önálló kórképként való felismerése (Smiddy) és a makuláris neovaszkuláris membránok, vérzések sebészi eltávolítása is (de Juan és Machemer). Utóbbi valószínűleg a vitreoretinális génsebészet alapjait teremtette meg. Szintén áttörést jelentett 1991-ben egy addig gyógyíthatatlannak vélt vitreomakuláris kórkép, a makulalyuk első sikeres műtéti megoldása (28). Ezt követően a belső határhártya (ILM) eltávolításának bevezetése (1997, Eckardt) javította, és módosításaival a mai napig javítja a makuláris sebészi kórképek kezelésének sikerét. A műtéttechnikai újítások végtelen sora mellett meg kell említenünk az optikai koherencia tomográfia (OCT) megjelenését és térhódítását a makula sebészetében is. Alapjaiban alakította az idetartozó kórképek megértését, eleinte patomechanizmus szerinti majd mindinkább funkcionális szemléletű osztályozását és az erre épülő terápiás algoritmusok fejlődését. Vitathatatlan, hogy a makulasebészet közel 50 év alatt végbement fejlődése rendkívüli, ugyanakkor szinte valamennyi, egyre eredményesebben kezelt területe tartogat tisztázandó kérdéseket, és további finomításokra szorul. Ráadásul léteznek olyan, ebben a közleményben nem érintett, forradalmi technikák (pl. génterápia, retinaprotézisek), amelyek nemcsak a szerzett makulabetegségek, hanem az öröklődő makuladisztrófiák kezelésében is új korszakot nyitottak, de széles körű elterjedésük még várat magára (12).
Jelen közlemény célja a meglévő ismeretek összefoglalása a mindennapokban leggyakrabban előforduló, sebészi megoldást igénylő vitreomakuláris határfelszíni betegségek: az epiretinális membránok, a részleges és a teljes vastagságú makulalyukak tekintetében.
Vitreomakuláris trakció
A vitreomakuláris határfelszín kórképeinek etiopatogenetikai hátterét a hátsó üvegtesti határhártya-leválás (PVD) különböző patológiás mintázatai adják. Az üvegtest involúciós változásainak fiziológiás részeként az PVD kezdeti stádiumában az üvegtest perifoveálisan válik le, a makula területén az adhézió perzisztál a retina morfológiai eltérése nélkül (1. ábra).
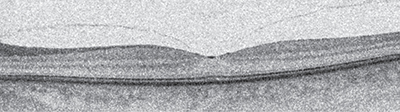
A vitreomakuláris adhézió (VMA) tehát az üvegtest életkorral összefüggő, fiziológiás leválási folyamatának részeként értelmezhető, és a PVD komplettálódásával megszűnhet, azonban kórosan fokozott adhézió esetén az üvegtest antero-poszterior húzóerőt fejt ki a makulára, és a VMA vitreomakuláris trakcióba (VMT) progrediálhat. Ennek megfelelően a VMT a folyamat patológiás kimenetelét képviseli. További progressziója a foveális depresszió (FD) fokozott torzulásához és különböző mértékben intraretinális vagy szubretinális folyadék megjelenéséhez vezethet. Az esetek egy részében spontán oldódás még ilyenkor is létrejöhet, azonban minél előrehaladottabb a folyamat, annál nagyobb esély van részleges vagy teljes vastagságú makulalyuk kialakulására. A VMT és a makula különböző, részleges és teljes vastagságú defektusainak összefüggésbe helyezését, rendszerbe foglalását az International Vitreomacular Traction Study jelentősen elősegítette. A klasszifikációban meghatározó szerep jut az üvegtesti határhártya és a retina belső felszíne közti érintkezési felület kiterjedésének: amennyiben ez 1500 μm-nél kisebb fokális VMT-ként értékelhető, míg az ennél szélesebb, már nagy kiterjedésű VMT-nek felel meg. Fokális VMT esetén erőteljesebb lehet az üvegtest húzó hatása, az intraretinális cisztoid-űrök (pszeudociszták) fala könnyebben megszakadhat, esetlegesen makulalyukat eredményezve, ugyanakkor a spontán oldódás esélyesebb. Ezzel szemben a szélesebb tapadási zóna mellett az oldódás kevésbé valószínű, így gyakrabban jelentkeznek krónikus folyamatok, pl. foveoszkízis (9).
A természetes lefolyás vizsgálatát célzó klinikai megfigyelések egy háromlépcsős stádiumrendszer bevezetéséhez vezettek (9, 25):
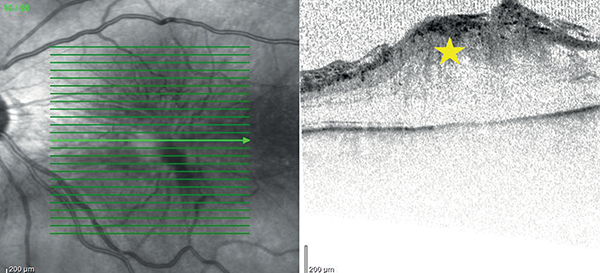
I. stádium: inkomplett PVD tapadással a foveában, amely a fovea kisebb fokú strukturális deformitását idézi elő (2. ábra). Az esetek mintegy harmadában spontán oldódhat.

II. stádium: intraretinális ciszták (IRC) megjelenése (3. ábra). Még itt is meglepően magas a spontán rendeződés esélye.
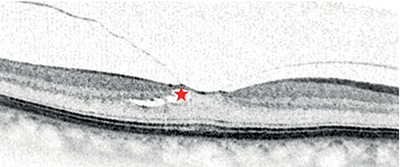
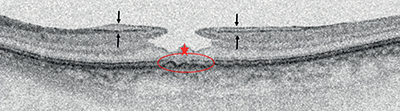
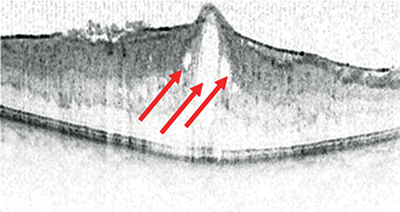
III. stádium: IRC-k mellett szubretinális folyadék (SRF) is megjelenik (4. ábra).

csillag) is megjelenik
Összességében a VMT, főleg kezdeti stádiumban, gyakran beavatkozás nélkül oldódik, a progresszió pedig általában lassú (25). Ezért az obszerváció sokszor biztonságos és megengedett, amit a legújabb európai ajánlások is megerősítenek: stabil vagy enyhe panaszok esetén, akár egyéves követés is megfelelő választás lehet (9, 11).
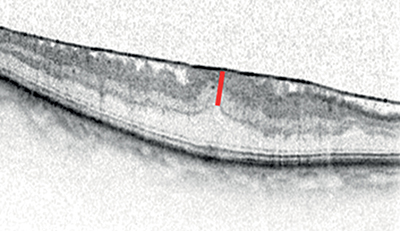
Jellemzően súlyosabb, II. vagy III. stádiumban kerül sor műtétre, elsősorban a beteget zavaró szubjektív panaszok (pl. torzlátás) miatt. A műtét legfontosabb célja a további funkcionális és anatómiai károsodás megakadályozása. Utóbbi alatt a részleges vagy teljes vastagságú makulalyukba történő progressziót értjük, ami ugyan a műtét során iatrogén módon is kialakulhat, de tapasztalt operatőr esetén ennek esélye minimalizálható, megfelelő műtéti technikával nagy arányban érhető el mind funkcionális, mind strukturális javulás (5. ábra).
Műtéttechnikai szempontból az üvegtesti határhártya megfestése triamcinolon segítségével, majd óvatos, centripetális irányú leválasztása, így végül a vitreofoveális trakció megszüntetése kiemelt jelentőségű. Habár a műtét közben esetlegesen kialakuló iatrogén makulalyuk jó eséllyel felismerhető, mégis előfordulhat, hogy rejtve marad, ezért gáz vagy legalább levegő endotamponád használata a legtöbb esetben ajánlott. További lehetséges komplikáció lehet, hogy az üvegtesti határhártya leválasztása a perifériás retinán szakadásokat okoz, ezért ennek ellenőrzése a folyadék-levegő csere előtt 360 fokos bedomborítással kiemelt jelentőségű (11, 25).
Az aranystandard PPV mellett egyéb kezelési lehetőségek is szóba jöhetnek. Az intravitreális ocriplazmin, és a pneumatikus vitreolízis (PV) elsősorban azon betegeknél lehet megfelelő választás, akiknél a műtét előrehaladott életkoruk, illetve számos komorbiditásuk miatt nem, vagy csak fokozott kockázattal végezhető el. Egyes szerzők szerint szintén kedvezőbb lehet, azoknál a betegeknél, akiknél az üvegtest megtartása előnyt jelenthet a további intravitreális gyógyszeres kezelés szempontjából (pl. diabéteszes makulaödéma), azonban ismerünk már olyan vizsgálatokat, ahol meggyőző eredmények születtek arra vonatkozóan, hogy az intravitreális injekciók hatékonysága független az üvegtesti státusztól (42, 68).
Az ocriplazmin intravitreális injekció formájában alkalmazott rekombináns proteáz, amely a vitreoretinális határfelületen a laminin és a fibronektin bontásán keresztül fejti ki hatását. Klinikai vizsgálatokban a VMT oldása az esetek mintegy 26,5%-ában sikeres volt (11). A gyakorlatban történő alkalmazása alapvetően enyhébb, korai stádiumú esetekben merülhet fel a folyamat progressziójának megelőzése céljából, másrészt előrehaladott állapotokban, ahol a PPV fokozott kockázatot jelenthet makulalyuk kialakulása szempontjából (73). Ezekben az esetekben az ocriplazmin alkalmazása lehetőséget adhatna egy kevésbé invazív megoldásra, használatát azonban jelentősen korlátozza a készítmény magas költsége, valamint viszonylag gyakori és potenciálisan súlyos mellékhatásai (pl. retinaszakadás vagy -leválás, makulaödéma kialakulása). Utóbbiak miatt 2023. augusztus 30-a óta az Európai Gyógyszerügynökség az Európai Unión belül kivonta a kereskedelmi forgalomból, ugyanakkor az USA-ban továbbra is használatos (29).
A PV alkalmazása szintén intravitreális injekció formájában történik, de nem enzimatikus, hanem mechanikai úton segíti elő a VMT oldódását. Az üvegtestbe juttatott gáz típusa hatékonyság szempontjából nem bír érdemi jelentőséggel. A PV hátránya, hogy szoros posztoperatív kontrollt és megfelelő kooperációt igényel a beteg részéről, beleértve az intravitreális gáz beadását követően rendszeresen végzett, ismételt fejmozgásokat („drinking bird” manőver). Lehetséges szövődményei között szintén fontos megemlíteni a retinaszakadást és -leválást, amely az üvegtesti határhártya szorosabb tapadási pontjain bekövetkező mechanikai erőhatások következményeként alakulhat ki (42, 49).
A makula részleges vastagságú defektusai
Lamelláris makulalyuk
A lamelláris makulalyuk (LMH) hosszú ideig rendkívül heterogén, folyamatosan újra definiált entitásnak számított, amibe a VMT-ben előforduló pszeudociszták „okozta” külső és belső réteglyukak, és a különböző megjelenésű foveoszkízis formák is beletartoztak. A modern, nagyfelbontású OCT-képek megjelenése lehetővé tette az LMH morfológiai leírásának finomítását, ami 2020-ban Hubschmann és munkatársai munkája nyomán konszenzusdefinícióhoz vezetett (22).
Az LMH diagnosztikus kritériumait az alábbi pontok szerint határozták meg (6. ábra) (22):
1. szabálytalan/irreguláris foveális kontúr, nyilvánvaló anyaghiánnyal a fovea területében,
2. foveális üregképződés a rétegek között, amely az üvegtesti térrel folytonosságot mutat, és aláásott szélekkel határolt,
3. és legalább 1 párhuzamosan fennálló jelenség, az alábbi három közül:
a: epiretinális proliferáció (EP), korábbi nevén lamelláris makulalyukhoz asszociált epiretinális proliferáció (LHEP), az OCT-felvételeken többnyire egy vastag, homogén, közepes reflektívitású nem kontraktilis rétegként jelenik meg a retina vagy az esetlegesen előforduló ERM felszínén. A korábban használt LHEP elnevezés arra utal, hogy megjelenése erősen kötődik az LMH-hoz, az esetek akár 80%-ában kimutatható. Az új nevezéktanra (EP), azért volt szükség, mert más entitásokhoz (pl. teljes vastagságú makulalyuk) is társulhat. Szövettani vizsgálatok alapján elsősorban Müller-sejt eredetű gliális proliferáció alkotja, amely a retina saját regenerációs és kompenzációs mechanizmusainak eredménye. Nem tartalmaz kontraktilis komponenseket, így nem zsugorodik, nem okoz trakciót, viszont jelenléte degeneratív, gyakran a retina külső rétegeinek károsodásával járó folyamatok markere, és rosszabb vizuális prognózissal párosul (45, 59);
b: foveális dudor (foveal bump) képződése. Lényegében egy retinális szövetsziget, amely nem, vagy csak részben érintett az alapfolyamat okozta szövetveszteségben;
c: az ellipszoid zóna (EZ) szabálytalansága, feltöredezettsége.
Korábbi terminológia, de még napjainkban is használatos az LMH trakciós és degeneratív formájának megkülönböztetése. Az utóbbi lényegében a Hubschmann szerinti, fentebb ismertetett LMH-val megegyezik cilinderre („tophat”) emlékeztető anyaghiányával (7. ábra).

A trakciós LMH olyan esetekre utal, amikor az eltérés ugyan lamelláris jellegű, de a rétegek egymástól való eltávolodása a makulára ható mechanikus erők, leggyakrabban epiretinális membrán (ERM) vagy VMT következménye. Ezekben az esetekben valódi szövetveszteség nincs, OCT-képe bajuszra emlékeztető konfigurációt mutat (8. ábra). Ezek alapján a trakciós LMH megnevezés félrevezető lehet, az ERM-fejezetben, mint ERM-foveoszkízis tovább részletezzük. Mindemellett a két altípus közötti átmenet – jellemző módon a trakciós forma degeneratív irányba való átalakulása – lehetséges. Prognózisukat tekintve a trakciós forma műtéti kimenetele kedvezőbb, a trakció megszüntetését követően a szerkezeti eltérések sokszor visszarendeződnek. Ezzel szemben a degeneratív altípus prognózisa általában rosszabb, a műtéti beavatkozás indikációja és technikája körültekintő mérlegelést igényel (14, 32).

Irodalmi áttekintés alapján elsősorban az EP jelenléte, műtét alatti menedzselése játszik kulcsfontosságú szerepet az operáció eredményességének alakulásában. Habár a betegség évekig stagnálhat, progresszív szövetvesztés, nemritkán teljes vastagságú makulalyuk (FTMH) kialakulása is előfordulhat. Utóbbi gyakorisága megközelítheti a 10%-ot, aminek magyarázatául szolgálhat, hogy az LMH előrehaladott eseteiben a centrális 200 mikronos területet kitöltő speciális gliatömörülés, az ún. Müller-sejt kúp (Müller cell cone) – aminek a fovea architektúra megtartásában döntő szerepe van – degeneratív módon károsodik. Ez egyrészt hozzájárul a fovea falába terjedő szövetveszteség kialakulásához és súlyosbodásához, másrészt sérülékenyebbé teszi a fovea alapzatát, különösen az ERM-ILM peeling során jelentkező mechanikus erőkkel szemben. Így a hagyományos, ERM-ILM peeling technikával a műtéti eredmények elmaradtak a trakciós formákéitól, és az iatrogén FTMH rizikója is magas, 9-30% közötti. Ezek eredőjeként a sebészek még a közelmúltban is elsősorban az obszervációt választották. Ezt a hozzáállást változtathatják meg az újabban megjelenő ígéretes technikák, mint az ILM és EP perifoveális megőrzése (sparing) vagy az EP makulalyukba történő beágyazása (embedding). Ezen módszerekkel a műtét funkcionális és strukturális eredményessége növelhető, az FTMH kialakulásának esélye csökkenthető. A jobb eredmények hátterében állhat, hogy a kavitációt kitöltő gliális szövet strukturális támaszt ad, és regenerációs potenciáljával segíti a funkcionális javulást is. Az EP pontos szövettani felépítése még nem teljesen tisztázott, de egyre több bizonyíték utal arra, hogy a benne található sárgás pigmentek a makula Müller-sejt eredetű xantofil pigmentjeiből származnak, amelyek antioxidáns tulajdonságaik révén neuroprotektív szerepet is betölthetnek (5, 31, 61).
AZ EP-vel szövődött LMH-műtét része az ILM eltávolítása, azonban azzal a módosítással, hogy a fovea körüli vékony sávot megkíméljük (perifoveal ILM sparing). Ugyancsak ajánlott a perifoveálisan lévő EP megőrzése, vagy csak lyuk szélén hagyva (perifoveal EP sparing), vagy finoman, a lyukba ágyazva (EP embedding), aminek a helyben maradását még egy visszahajtott ILM, ERM-ILM lebennyel felülről is biztosíthatunk (35, 59, 61). Fenti megoldásoknál a peelinget több helyről indítva, centripetális irányban végezzük, majd fokozatosan, lehetőleg atraumatikusan, a közvetlen perifoveális terület vongálása nélkül távolítjuk el a membránokat (20). Az LMH modern sebészetében meghonosodott különböző perifoveális szövetmegtartó technikák segítségével lehetségesnek látszik, hogy javítsuk a betegség prognózisát, valamint elkerüljük, illetve csökkentsük a fent részletezett műtéti rizikókat (9. ábra).
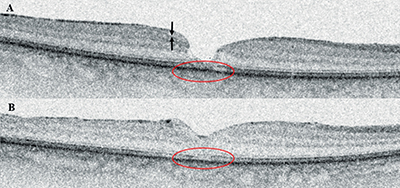
Ennek a minimálisan invazív, biológiai regenerációt aktiváló eljárásokat alkalmazó trendnek következő állomását jelenthetik az ún. „no-retina-touch” technikák, mint például az autológ trombocytakoncentrátum (platelet rich plasma) alkalmazása, de ezek egyelőre még kevésbé terjedtek el a mindennapi gyakorlatban (54).
A műtéttechnikai fejlesztéseken túl bizonyosan finomítani és szélesíteni kell az OCT-alapú diagnosztikus és prediktív biomarkerek használatát, mert jelen ismereteink mellett nem minden esetben tudunk pontosan prognosztizálni, vagyis teljességgel megalapozott döntést hozni (10. ábra).
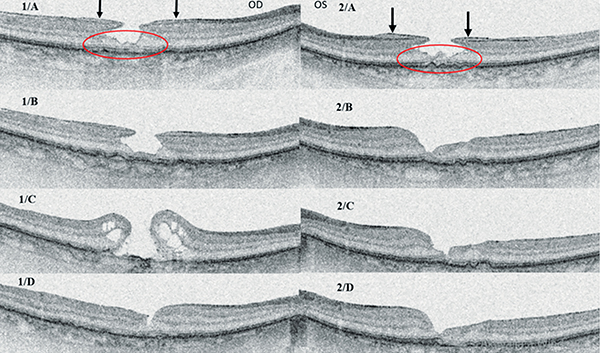
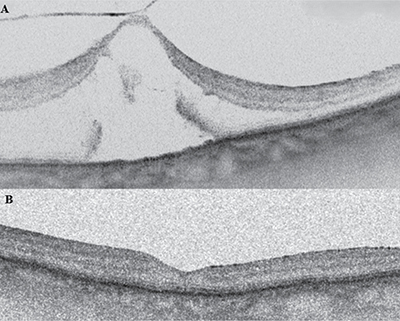
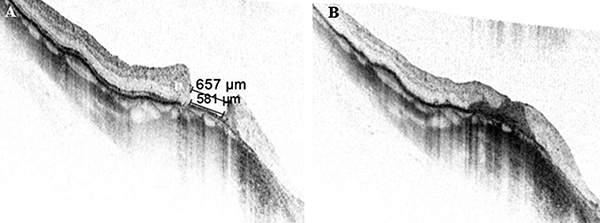
Bal szem esetében kezdetben obszerváció mellett döntöttünk, majd 3 hónapos követési idő alatt bekövetkező látóélesség-romlás (BCVA 20/25-ről 20/40-re csökkent) miatt műtétre került sor. Standard technikával (ERM-ILM peeling) végeztük a műtétet, amelyet kielégítő funkcionális és anatómiai javulás követett (2/B). A jobb szem obszervációja alatt is romlott a vízus (BCVA 20/25-ről 20/40-re csökkent), a kavitáció fokozódott, így standard technikával (ERM-ILM peeling) megtörtént a jobb szem operációja is. Azonban a bal szemen látott eredményesség elmaradt, a folyamat FTMH-ba progrediált (1/C). Reoperációra került sor az ILM peeling kiterjesztésével és gáztamponád alkalmazásával. A FTMH bezárult (1/D), azonban jobb szem látóélessége fél évvel később sem érte el a preoperatív vízust (posztoperatív BCVA 20/100). Mindeközben a bal szem strukturálisan stabilitást mutatott csaknem teljes vízussal (2/C-D)
Makuláris pszeudoforámen
Differenciáldiagnosztikai szempontból az LMH-t a makuláris pszeudoforámentől (MPH) nehéz elkülöníteni. A pszeudoforámen elnevezés magyarázata, hogy klinikailag, elsősorban biomikroszkópos képe, ahol jól körülhatárolt, vöröses, kerek vagy ovális elváltozásként jelenik meg a makulában, a megtévesztésig utánozza a FTMH-t. Ugyanakkor Allen–Watzke-tünetre negatív. Lényegében az ERM speciális megjelenési formája, ahol a membrán respektálja a fovea centrumát, azonban centripetális húzóhatást fejt ki a perifoveális retinára, és ennek következtében a fovea szélei invaginált, meredek, vertikalizált profilt vesznek fel. Az OCT-felvételen úgy tűnik, mintha egy „szűk, mély” foveális üreg lenne, azonban tényleges szövethiány nincs, és a retina központi részének struktúrája megtartott, vagy csak minimálisan tér el a normálistól (11. ábra).
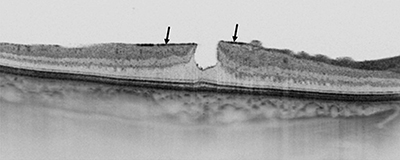
A centrális retinavastagság (CRT) sok esetben közel normális tartományban marad. En face OCT-n az ERM által létrehozott radiális mintázat és a fovea enyhe besüppedése figyelhető meg. Az MPH lassan progrediáló, néha VMT-vel szövődő, jó műtéti prognózissal rendelkező vitreomakuláris kórkép. A műtéti indikáció sokkal inkább a beteg panaszain és a funkció károsodásán alapul, mint az OCT-képen (22, 35).
Az MPH diagnózisához kötelező major kritériumok (22, 35):
- Foveát respektáló ERM.
- Megvastagodott perifoveális retina.
- Vertikális, meredek foveális profil (>90°).
Minor kritériumok (22):
- Mikrocisztoid terek a belső magvas rétegben (INL).
- Közel normális CRT.
Ezen betegségek (LMH, MPH, ERM- foveoszkízis) pontos diagnosztizálását megnehezíti, hogy patofiziológiájuk gyakran átfedésben van. OCT-felvételek részletes elemzésén alapuló vizsgálatok kimutatták, hogy az esetek kb. harmada „vegyes típus”, vagyis több entitás diagnosztikai kritériumai egyszerre teljesültek. Ráadásul a kórképek egymásba történő átmenete, átalakulása is lehetséges (35).
Epiretinális membrán
Az epiretinális membrán (ERM) egy fibrocelluláris proliferáció a vitreoretinális felszínen, az ILM felett. Elsőként Iwanoff írta le 1865-ben, azóta az ERM-mel kapcsolatos ismereteink folyamatosan fejlődnek (12).
Epidemiológia
Előfordulási gyakorisága elsősorban az életkortól függ, a prevalencia csúcsát a 7. évtizedre teszik. A legtöbb tanulmány szerint kevésbé fontos, illetve megkérdőjelezhető a nem, valamint az etnikai hovatartozás epidemiológiai szerepe. Az ERM felismeréséhez használt diagnosztikus módszer érzékenysége viszont jelentősen befolyásolhatja az előfordulási gyakoriság megítélését. A Beaver Dam Eye Study a 60 évesnél idősebb populációban 11,8%-os prevalenciát jelentett az idiopátiás ERM esetében színes fundusfotók használata alapján, viszont jóval magasabb, 34%-os előfordulási arányról számolt be, amikor a spectral domain OCT-t (SD-OCT) bevonták a diagnosztikába (16, 35).
Etiopatogenezis, patofiziológia
Nem teljesen tisztázott: több elmélet is létezik, de egyik sem ad teljeskörű magyarázatot. A felépítésében szerepet játszó preretinális myofibroblasztok feltehetően különböző sejtekből (pl. gliasejtekből, retinális pigmentepithel sejtekből, hyalocytákból) differenciálódnak, amelyek származhatnak a retinából, átjutva az ILM PVD során kialakuló mikrodefektusain keresztül, vagy az üvegtestből, inkomplett PVD következtében. Ezek a myofibroblasztok extracelluláris mátrix komponenseket és kontraktilis fehérjéket termelnek, amelyek az ERM zsugorodásáért és retinára kifejtett vongáló hatásáért felelnek (16, 35, 41).
Kórlefolyását tekintve az ERM lassan progrediáló betegség. Az ezredforduló környékén a Blue Mountains Eye Study arról számolt be, hogy 5 éves követési időszak alatt a legtöbb ERM súlyossága nem fokozódott: kb. 39% stabil maradt, 26% regrediált, és csak 29% mutatott progressziót színes fundusfotók elemzése alapján. OCT-t használva a progresszió megítéléséhez ezek a százalékok eltérőek lehetnek, de összességében elmondható, hogy az ERM-mel diagnosztizált betegeknek csak kis százaléka kerül műtétre a kezdeti észleléshez képest 5 éven belül és rövid távon a beavatkozás késleltetése nem jár jelentős hátránnyal (16).
Felosztás, nevezéktan
Egyes szerzők a premakuláris membrán elnevezést preferálják az epiretinálissal szemben, arra hivatkozva, hogy ez a terminológia specifikusabb, a membrán lokalizációját egyértelműbben meghatározza. Jelen közleményben az epiretinális membrán megnevezést használjuk, előzetesen utalva arra, hogy a vitreomakuláris határfelszínt érintő kórképekkel foglalkozunk (12).
Etiológia alapján 2 nagy típusát különbözetjük meg: az idiopátiás (iERM) és szekunder ERM-et. Az iERM jellemzője, hogy nincs társuló szemészeti rendellenesség. A fellelhető irodalom elsősorban ezzel foglalkozik. A PVD az esetek >90%-ában jelen van, ami arra utal, hogy fontos szerepet játszik a kialakulásában. A PVD nélküli esetek etiopatogenezise még nyitott kérdés. Szekunder ERM esetén egyéb szemészeti betegség (pl. vaszkuláris retinabetegség, uveitis, trauma, retinaszakadás/-leválás vagy intraokuláris műtét utáni állapot) is fennáll. Ilyenkor a sebészi megoldás maga nem különbözik, de a terápiás stratégia annyiban más, hogy előbb a társuló patológiát érdemes kezelni. Ha a beteg panaszai nem javulnak a farmakoterápia (pl. intravitreális anti-VEGF) alkalmazása mellett, akkor az a trakciós komponens kóroki szerepét valószínűsíti és műtéti indikációt jelent (16, 35, 40, 41).
Vizsgálómódszerek
Az ERM diagnózisának felállítása nem nehéz, zömében egyszerű réslámpás vizsgálattal elvégezhető. A multimodális vizsgálómódszerek inkább az ERM súlyosságának, progressziójának, végső soron a műtét indikációjának, valamint a műtét eredményességének megállapítását segítik.
Biomikroszkópos vizsgálat során a retina felszínén kezdetben celofánszerű csillogás (celofán makulopátia), majd az egyre vastagabbá váló membrán összehúzódásából eredő ráncosodás, redőképződés figyelhető meg (macular pucker). A környező erek lefutása is torzulhat. A redők lefutása gyakran mutat radier mintázatot egy vagy több kontrakciós gócpontból kiindulva. A Gass-féle klasszifikáció még erre a réslámpás képre támaszkodott. Később számos OCT-alapú osztályozási rendszer jelent meg, egyre inkább azzal a céllal, hogy segítse a műtéti indikáció felállítását ennek a lassan progrediáló kórképnek az esetén. Govetto és munkatársai 2017-ben 4 stádiumból álló, SD-OCT-alapú iERM-osztályozási rendszert dolgoztak ki, a magasabb stádium jól korrelál a súlyosabb kezdeti tünetekkel és a rosszabb prognózissal is (12. A–D ábra). A leggyakrabban használt B-scan képek mellett egyéb OCT-technikák is, mint például az en face és 3D OCT-felvételek (13. A–B ábra) segíthetik a pontosabb diagnózis és a műtéti indikáció felállítását (16, 41).
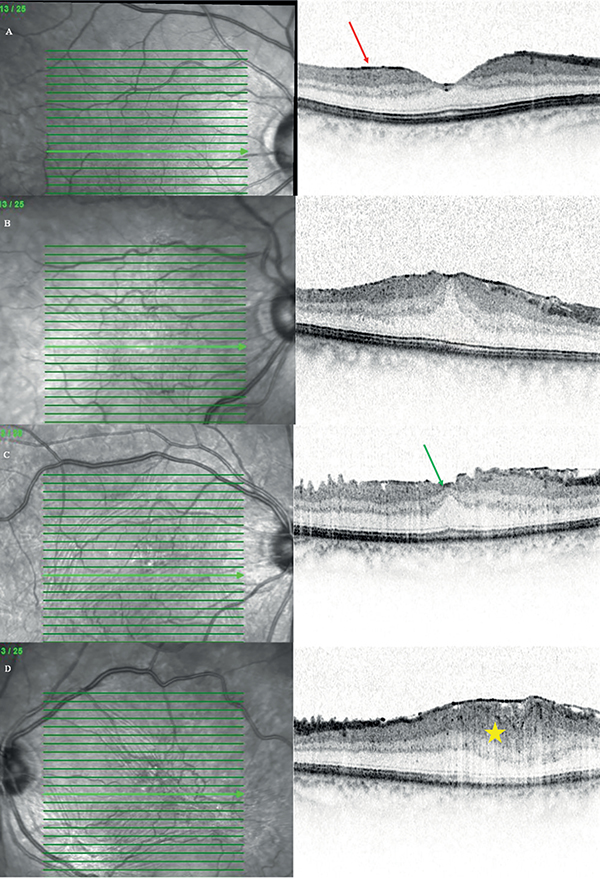
1. stádium (A): ERM megjelenése hiperreflektív sávként (piros nyíl) a vitreoretinális felszínen, de az FD még jelen van, a retina szerkezete megtartott; 2. stádium (B): FD eltűnése; 3. stádium (C): ektopikus belső foveális rétegek (EIFL) megjelenése (zöld nyíl); 4. stádium (D): retinarétegek dezorganizációjának megjelenése (sárga csillag). Az infravörös képen jól látható a retina felszínének fokozódó ráncosodása, redőképződése a magasabb stádiumok felé haladva
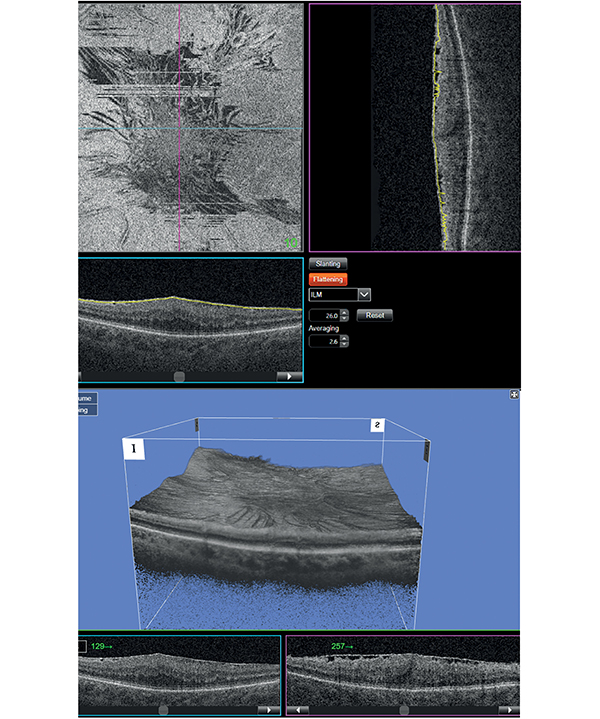
OCT biomarkerek
Számos OCT biomarker létezik, amelyek jól használhatók az iERM-esetek értékelése során. Újabban egyre nagyobb hangsúly helyeződik az ERM által okozott mechanikai stressznek közvetlenül kitett belső retinarétegekre, azon belül is azok dezintegrációjára (DRIL) (14. ábra), vastagságára vagy éppen az intraretinális ciszták (IRC) (15. ábra) jelenlétére, mint negatív prognosztikai faktorokra. A DRIL szerepe már régóta ismert a diabéteszes makulaödémával kapcsolatban, de a DREAM-study-ban leírták, hogy iERM esetén is független, negatív biomarkerként szolgálhat. Szignifikáns kapcsolatot találtak a DRIL súlyossága és a pre-, valamint posztoperatív legjobb korrigált látóélesség (BCVA) között. A belső magvas rétegben (INL) lévő ciszták a Müller-sejtek mechanikai erők okozta pusztulásával létrejövő hiporeflektív lakunák, amelyek az esetek jelentős részében a műtét után is megmaradnak, negatívan befolyásolva ezzel a vizuális prognózist. Ezeket a trakciós eredetű cisztoid űröket mikrocisztás makulaödéma (MMO) néven különbözteti meg az irodalom az exszudatív eredetű cisztoid makulaödémától (CMO), amely elsősorban iszkémia vagy gyulladás okozta vaszkuláris permeabilitás fokozódás következtében alakul ki, a retina belső és külső rétegeiben egyaránt (12, 43, 47, 60, 75).
A Govetto-féle 3. stádiumban megjelenő ektopikus belső foveális rétegek (EIFL) szintén egy klinikailag jól használható OCT biomarker (16. ábra). Egy folyamatos, FD helyét kitöltő, belső retinarétegekből álló hiper- és hiporeflektív sáv jelenléteként definiálható, amely az OCT-felvételen kaliper segítségével μm-ben pontosan meghatározható. Kialakulásáért elsősorban a centripetális irányú trakciós erőket teszik felelőssé. Bár vastagsága jelentősen csökkenhet a műtét után, az esetek 90%-ában nem tűnik el teljesen. Jelenléte és vastagsága függetlenül más OCT-eltérésektől negatívan befolyásolja a pre- és posztoperatív BCVA-t és torzlátást is. Így a műtét optimális időpontja még az EIFL kialakulása előtt, azaz a Govetto-féle 2. stádiumban lehet (7, 12, 16, 34, 35, 43, 47, 72).
Kanzaki és munkatársai en face OCT segítségével az ún. maximális retinaredő mélységet (MDRF) vizsgálták, amely objektív és kvantitatív biomarkere lehet a pre- és posztoperatív metamorfopsziának (MM). Eredményeik azt mutatják, hogy az iERM-műtét időzítése akkor megfelelő, amikor a preoperatív MDRF parafoveálisan 69 és 118 μm közötti értéket vesz fel. Ezekben az esetekben az MM életminőséget nem rontó szintig csökkent. A jelzett intervallum alatti MDRF esetén nem érdemes operálni, mert a torzlátás még nem rontja az életminőséget, míg ha felette van, akkor a posztoperatív MM jelentős, életminőséget rontó marad (7, 27).
A szubfoveálisan elhelyezkedő fotoreceptorok különösen kitettek az ERM okozta trakciós erőknek, szemben a parafoveális régióval, ahol a Henle-rostok protektív szerepe még érvényesül. Ezt a 100 μm átmérőjű szubfoveális területet „central bouquet” névvel illeti az irodalom. Itt axiális trakciós erők hatására különböző külső elemeket érintő abnormalitások alakulhatnak ki, amelyek egy klinikai spektrumot képeznek. Ezek az ERM progresszióját jelző külső retinális biomarkerek (17. A–C ábra). A „cotton ball sign” egy kerek, diffúz, hiperreflektív terület megjelenése az interdigitációs zóna (IZ) és az ellipszoid zóna (EZ) között (17. A ábra). Ez a fotoreceptorok trakció okozta vertikális elmozdulásából adódik. Ennek progressziója a foveola leválásához vezet az alatta lévő retinális pigmentepithelről (RPE), ami centrális SRF felhalmozódását eredményezi (17. B ábra). Ezek műtét után, a trakciós erők oldásával általában megszűnnek. Azonban krónikus trakció esetén az SRF tartós fennállása megzavarja az RPE-fotoreceptor komplex működését, ami metabolikus törmelék progresszív felhalmozódását eredményezheti a szubretinális térben, ezzel ún. szerzett vitelliform megjelenést okozva (17. C ábra). Ez utóbbi a fotoreceptorok irreverzibilis károsodását jelzi, műtét után gyakran atrófia alakul ki (12, 16, 52).
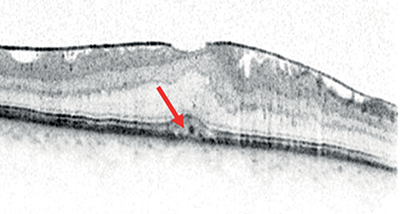

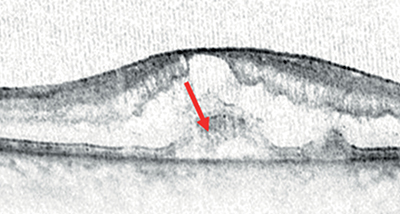
Újabban az ERM-spektrum témakörében tárgyalják az ERM-foveoszkízist, amely az ERM által kifejtett centrifugális trakciós erők következményének tartható. Általában stabil, ritkán progrediál teljes vastagságú makulalyukba és a szignifikáns strukturális eltérések ellenére a funkciókárosodás ritka. A diagnózis felállításához két major kritériumnak kell teljesülnie, azaz szükséges az ERM jelenléte és a foveoszkízisnek a Henle-rostok rétegét kell érintenie (18. ábra).

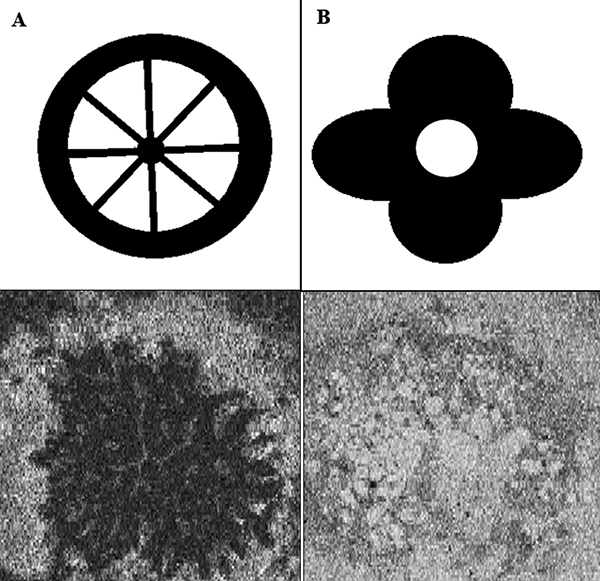
Minor kritérium az INL-ben jelen lévő IRC-k, a retina megvastagodása és ráncolódása. Az ERM-foveoszkízishez kapcsolódó trakciós eredetű intraretinális cisztoid űröket az exszudatív mechanizmusúaktól kell megkülönböztetnünk. Előbbiek kerékküllő, utóbbiak szirom alakú mintázatot mutatnak en face OCT-felvételeken (12) (19. ábra).
Klinikai tünetek
Az előbb említett OCT biomarkerek jól korrelálnak az ERM okozta panaszokkal, de mégsem hagyhatjuk figyelmen kívül a páciens gondos kikérdezését. Akár maszkolva is lehetnek, ha nem a domináns szem érintett, ezért irányított módon mindig rá kell kérdezni a látásromlás mellett a torzlátásra és a mikropsziára, makropsziára (aniseikonia) is. Ráadásul, ha a betegnek panaszai vannak, akkor sem mindig egyértelmű, hogy indokolt-e az operáció, megfelelő eszközökkel objektivizálni kell őket és figyelembe kell venni az életminőséget befolyásoló hatásukat is (7, 16, 35, 40, 41).
Habár az iERM negatívan befolyásolja a BCVA-t, a műtéti indikáció meghatározásakor nem célszerű kizárólag erre hagyatkozni, mivel korai szakaszban gyakran nem romlik, inkább más, pl. szürkehályog, állhat mögötte, valamint az egyéb szubjektív tünetek sokkal negatívabban tudják befolyásolni az életminőséget (39, 44).
Specifikusabb és hamarabb jelentkező szubjektív tünet az MM, ami gyakran sajnos a műtét után sem szűnik meg teljesen, csak mérséklődik. A beteg a függőleges vagy vízszintes (néha mindkettő) egyenesekben megjelenő hullámosodást, olvasásnál a sorok hullámzását panaszolja. Kialakulását egyre inkább a belső retinarétegek rendezetlenségével, a Müller-sejtek torzulásával hozzák összefüggésbe. Az ERM eltávolításával ezt a strukturális elváltozást a műtét csak részben tudja megoldani. Az MM értékelésére jelenleg az Amsler-rács és az M-CHARTS használatos. Az előbbi hasznos az MM jelenlétének vagy hiányának szűrésére, de nem képes kvantitatív értékelésre. Erre az M-CHARTS használható, amivel a horizontális és vertikális MM is számszerűleg megadható. A horizontális metamorfopsziát (MH) általában a betegek jobban megélik. Kanzaki és munkatársai megállapították, hogy ha az MH ≥0,5°, az a mindennapi életet már negatívan befolyásolja. Így a műtét célja, hogy a posztoperatív MH <0,5° legyen, ami akkor teljesülhet, ha a preoperatív MH ≤0,9°. A műtét optimális időzítése az MM fokát figyelembe véve tehát így határozható meg: 0,5° ≤ MH ≤ 0,9° (7, 27, 39, 65).
Szintén jellemző tünet, az aniseikonia, azon belül is főleg a makropszia, amelyet a csapoknak a membrán centripetális húzásának következtében kialakuló összetorlódása eredményez. Ehhez kapcsolódik az ERM egyik talán kevésbé ismert tünete az ún. binokuláris interferencia, amely akkor jelentkezik, amikor a betegnek be kell csuknia az egyik szemét, hogy javítsa látását. Ez lehet az érintett és nem érintett szem is. A megnövekedett INL-vastagság mind a pre- mind a posztoperatív aniseikoniának mérhető OCT biomarkere lehet. Az MM-mel szemben az aniseikonia gyakran nem javul, sőt a sikeres műtét ellenére is előrehaladhat. Érdemes tudni, hogy kvantitatív értékelésére az ún. New Aniseikonia Test használható, de ez a mindennapi klinikumban még kevésbé ismert, mint az M-CHARTS (7, 23, 39).
A műtét időzítése
A műtéti technika minimál invazív irányú fejlődésével és a műtéti idő rövidülésével megfigyelhető a tendencia, hogy a sebészek könnyebben döntenek az obszerváció vs. műtét dilemma során az operáció mellett. Ebben szerepet játszik az a tudásunk is, hogy korai műtéttel megelőzhetünk olyan potenciálisan irreverzibilis elváltozásokat, mint például a súlyos MM, amely viszonylag jó vízus mellett is kialakulhat.
A korábban használt műtéti indikációs faktorok, mint bizonyos vízushatárok (gyakran 20/32), CRT-növekedés, retina külső szegmens érintettség helyett egyre inkább a funkcionális stádiumbeosztást (lásd Govetto), és az MM megjelenését tartjuk meghatározónak, mindamellett, hogy továbbra sincs Cochrane study szintű evidencia a műtét pontos időzítésével kapcsolatban. Ha kedvezőtlen prognosztikai faktorokat detektálunk (1. táblázat), bölcsebb a betegnek „csupán” a további rosszabbodás megállítását „ígérni” a látásjavulással szemben. Ez különösen igaz, ha a műtét nem szürkehályog-eltávolítással kombináltan történik, ami a beteg elégedettséget kedvezőtlen ERM-prognózis mellett is fokozhatja. Továbbá a mérlegelés során a páciens igényeit, életminőségét befolyásoló tényezőket is figyelembe kell venni (12).

Műtét
Habár van többé-kevésbé kialakult, standard műtéti megoldás, ami, lehetőleg kisebb kaliberű (25, 27-gauge) „core” PPV-t, vitális festést és end-gripping üvegtesti csipesz használatát, a periféria ellenőrzését bedomborítással (!) foglalja magába, továbbra is vannak vitatott kérdések. Az egyik ilyen, hogy az ERM peelinggel egy időben kell-e ILM peelinget is végezni. Az ILM peeling valószínűleg összefüggésbe hozható bizonyos, posztoperatív strukturális eltérésekkel, mint például a foveától temporálisan eső neuroretina elvékonyodása (20. ábra), perzisztáló intraretinális ödéma (21. ábra), az RNFL átmeneti ödémája vagy disszociációja (DONFL), azonban ezeknek klinikailag szignifikáns funkcionális következményét eddig nem tudták igazolni. Ugyanakkor az ILM peeling mellett szól, hogy általa biztosabbra vehető az ERM komplett eltávolítása, és habár az iERM esetekben a kiújulási arány alacsony, az ILM peeling ezt is tovább csökkenti, tekintettel arra, hogy az ILM gyaníthatóan egyfajta alapként szolgálhat az ERM-képző sejtek proliferációjának. A legtöbb esetben az ILM-et az ERM peelinggel egyidejűleg (en-bloc) eltávolítjuk, részben akaratlanul a kettő közötti szoros tapadás miatt, részben szándékosan, mert az ERM szélének megragadása és izolált eltávolítása műtéttechnikailag sokkal nehezebb, mint a membránon túlnyúló ILM megkezdése, és innen indítva, a „szőnyeggel a piszkot” módszerrel az ERM komplett eltávolítása. Azokban a ritka esetekben, amikor az ERM izoláltan levonható tényleg felmerülhet ennek kérdése, ilyenkor ajánlott lehet ismételt festés után az ILM peelinget csak azon a területen elvégezni, ahol az feltétlen szükséges. Ez a parafoveális terület, azaz a fovea középpontjától mért 3 mm átmérőjű kör területe, ezen kívül a reziduális vagy recidiváló ERM valószínűleg nem befolyásolja a posztoperatív funkcionális eredményeket. Ugyanakkor egyes szerzők nem ajánlják az ILM peelinget preoperatív MMO esetében, mert annak perzisztálását vagy progresszióját idézheti elő. A műtét még precízebb kivitelezését nagyban segítheti majd az intaroperatív OCT széles körű elterjedése (7, 12, 13, 16, 35–37, 57, 58).
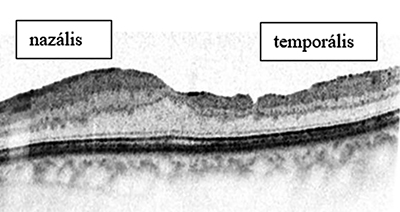
nazális része pedig megvastagszik

A kromovitrectomia olyan vitális festékanyagok használatát jelenti, amelyek megkönnyítik a transzparens, szemitranszparens membránok vizualizációját és eltávolítását a műtét során. Az indocianin-zöld volt az első, klasszikus festék a makulasebészetben. Habár kiválóan alkalmas az ILM szelektív megfestésére, potenciális retinatoxikus hatása miatt Európában visszaszorult az alkalmazása. Hazánkban elsősorban kombinált, Trypan Blue és Brilliant Blue G festéket is tartalmazó formulák terjedtek el az ERM és ILM egyidejű megfestéséhez. Magasabb fajsúlyú formulák kifejlesztése polietilén-glikol hozzáadásával tovább mérsékelte a toxicitást, mert azáltal, hogy folyadék alatt beadhatók (wet technique), koncentrációjuk is csökken. Ráadásul gyorsabban süllyednek le a vitreoretinális felszínre, így az expozíciós idő is csökken. A kombinált formulák tehát mind hatékonysági, mind biztonsági profiljukat tekintve előnyösebbek. Újabban a luteintartalmú készítmények is egyre nagyobb teret hódítanak kedvező tulajdonságaik miatt (pl. neuroprotektív, antioxidáns hatás) (3, 12, 16, 35. 50).
Adjuváns szteroidkezelés, azaz a műtét végén adott intravitreális trimacinolon vagy dexamethasone előnyeivel kapcsolatban sincs egységes álláspont. Változó strukturális és funkcionális eredményekkel találkozhatunk az irodalmat olvasva. Egy 2022-ben közölt metaanalízis szerint az intravitreális kortikoszteroid injekcióval kombinált vitrectomia, különösen a lassú felszabadulású dexamethasone implantátum, előnyös lehet a CRT-csökkenés tekintetében az ERM-műtét után 3 hónappal. Azonban a BCVA javulása és hosszabb, 6 hónapos követés után a CRT változása sem volt szignifikáns a kontrollcsoporthoz képest. Mindemellett az intravitreális szteroid megemelheti a szemnyomást mind a korai mind a késői posztoperatív időszakban, illetve saját lencsés betegeknél fokozhatja a szürkehályog progresszióját (6, 46, 71).
Teljes vastagságú makulalyuk
A teljes vastagságú makulalyuk (FTMH) a makula középső részén a neuroszenzoros retinán található teljes vastagságú defektus, amely a centrális látás elvesztését, illetve torzlátást okoz (2).
Epidemiológia
A makulalyukak mechanizmust tekintve kialakulhatnak idiopátiásan (24, 26), és szekunder módon: trauma következtében, myopia talaján, intravitreális anti-VEGF injekcióval kezelt nedves típusú időskori makuladegenerációban, 2-es típusú makuláris teleangiectasiában stb. Az idiopátiás makulalyuk prevalenciája 3:1000, gyakoribb nőknél, és általában 55 éves kor után fordul elő, ellentétben a traumás makulalyukkal, amely gyakrabban fordul elő fiatal férfiaknál (20-as és 30-as évek). Megemlítendő, hogy a trauma következtében kialakult makulalyukak általában nagyobbak (2).
Prognózis
A záródás tekintetében a prognózist alapvetően három tényező befolyásolja: a makulalyuk mérete, konfigurációja és a fennállási ideje. A látásjavulás legerősebb prognosztikai faktora a preoperatív vízus, ami általában lineáris összefüggésben van a forámen átmérőjével. A Gass szerinti 2., 3. és 4. stádiumú makulalyukakkal rendelkező betegek többségénél kezelés nélkül várható a centrális látás progresszív elvesztése. Ötéves követés alatt a páciensek 60%-a 2 vagy több sort veszít (Snellen-tábla), 3-5 éves követés után a szemek 70-80%-ának 20/200 vagy annál rosszabb lesz a látóélessége, a fennmaradó 20-30% látóélessége pedig általában 20/70 és 20/100 között lesz. A Gass 2. stádiumú FTMH-ak körülbelül 75%-a progrediál 3. vagy 4. stádiumba. A kezelés késleltetése csökkentheti a záródási arányt és a várható posztoperatív vízust. Habár a makulalyuk sikeres záródását követően a vízusbeli prognózis jó, a látóélesség általában nem tér vissza az eredeti állapotba, valamint az MM és a mikropszia/makropszia is sokáig, akár véglegesen fennmaradhat. A másik, nem érintett szem vizsgálata is fontos. PVD nélküli esetekben 10-15% esély van arra, hogy az ellenoldali szemben is makulalyuk alakul ki 5 éven belül. Amennyiben a PVD már jelen van, ez az arány kisebb (2).
Traumás makulalyukak esetén a spontán záródás lehetősége jól ismert, de Garg és munkatársai 2022-ben publikált szakirodalmi áttekintő tanulmánya alapján idiopátiás FTMH esetén is megfigyelhető. A ≤250 µm-es minimum lineáris átmérőjű (MLD) makulalyukak spontán záródási aránya 22,2%, a >250–400 µm-es intervallumban 13,3% és ha MLD ≥400 µm akkor 0% (17). Ugyanakkor fontos hangsúlyozni, hogy idiopátiás FTMH esetén a korai vitrectomia minden esetben magasabb záródási arányt, jobb posztoperatív látóélességet eredményez, így a jelenlegi ajánlások mielőbbi műtétet javasolnak (2). A 400 µm-nél kisebb átmérőjű, kevesebb, mint 6 hónapja fennálló FTMH műtéttel közel 100%-ban zárható. A látásjavulás esélye azonban a felére csökken azoknál, akiknél a lyuk fennállási időtartama meghaladja a 4 hónapot (10).
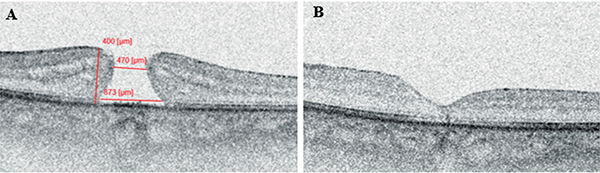
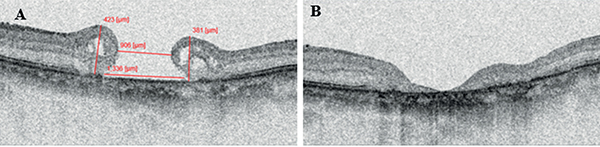
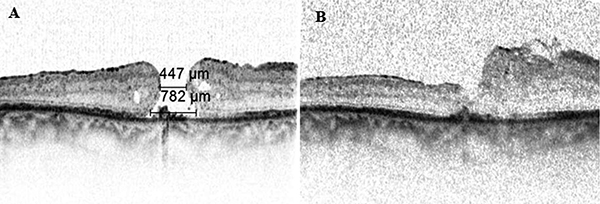
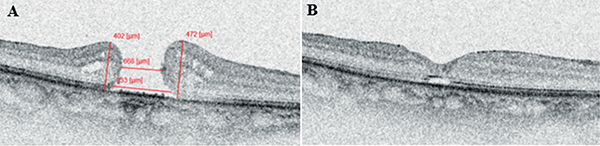
A Szegedi Tudományegyetem (SZTE) Szemészeti Klinikáján makulalyuk miatt operált betegek körében végzett felmérésünk szerint az MLD az esetek 60%-ában nagyobb volt, mint 400 µm (22. ábra). Míg vitrectomiával a kisméretű forámenek közel 100%-a záródott, az átmérő növekedésével párhuzamosan a záródási arány csökkent (23. ábra). Fenti adatok alapján kiemelten fontos a betegség korai felismerése és kezelése (21, 22).
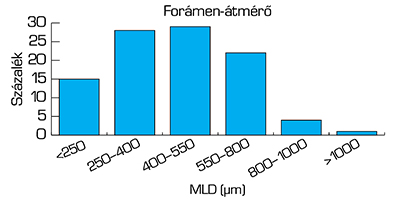
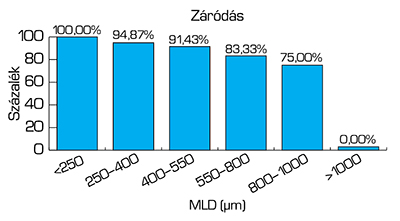
Preoperatív OCT-felvételek segítségével az MLD mellett több, a betegség súlyosságát jelző, prognózist meghatározó biomarker meghatározható, például az alap lineáris átmérő (BLD) és a makulalyuk magassága (H) (24. ábra). Leírható a lyuk széleinek alakja (pl. felemelkedő, letapadó, cisztoid), valamint az esetlegesen társuló patológia (pl. ERM, EP, VMT) (25. ábra) jelenléte is (1).
A fovea átlagos vastagsága a centrális 1 mm átmérőjű területen (CSFT) szintén hasznos prognosztikai faktor. A 300 μm-nél kisebb preoperatív CSFT az anatómia siker szempontjából kedvezőtlen jellemzőnek tartható (63).

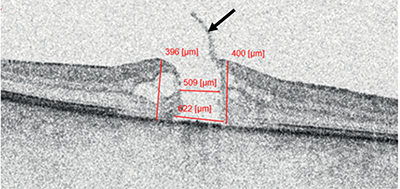
Az alapadatokból a következő értékek számolhatók:
- A makulalyuk-index (MHI) a makulalyuk magasság és a BLD hányadosaként definiálható. Az MHI >0,5 értékhez jobb posztoperatív anatómiai és funkcionális eredmények társulnak, míg alacsonyabb érték esetén a záródás esélye és a várható látásjavulás mértéke csökken (53).
- A tractional hole index (THI) a makulalyuk magasságának és az MLD-nek a hányadosaként számítható. Az 1,4-nél nagyobb érték jobb posztoperatív vízust valószínűsít (56).
- A hole form factor (HFF) kiszámítható, ha az FTMH két szélén az alaptól az isthmusig mért távolság összegét elosztjuk a BLD-vel. Ullrich és munkatársai 2002-ben publikált tanulmánya szerint 0,9-nél nagyobb értékek esetén a forámenek 100%-a záródik, viszont 0,5-nél kisebb értéknél a záródási arány 67%-ra csökken (70).
- A diameter hole index (DHI) az MLD és a BLD hányadosa. Amennyiben DHI <0,5, az jó prognózist jelent (66).
Osztályozás
Széles körben ismert az FTMH Gass által 1988-ban közzé tett stádiumbeosztása. Gass zsenialitása – többek között – abban rejlett, hogy biomikroszkópos képük alapján osztályozta a forámeneket, és következtetett a szövettani struktúrára, valamint a kialakulás mechanizmusára (2). Az első OCT-alapú osztályozást, a patomechanizmusban leggyakrabban szerepet játszó VMT mértékét, valamint az MLD-t figyelembe véve az International Vitreomacular Traction Study Group javasolta 2013-ban (2, 9).
Az a tény, hogy a 400 μm-nél nagyobb makulalyukak műtéti sikeraránya jóval alacsonyabb a kisebb forámenekhez képest, életre hívott egy újabb, ezek eredményesebb műtéti kezelését is előmozdító osztályozást. A CLOSE Study Group (Classification for Large Macular Hole Studies) néhány évvel ezelőtt kidolgozott egy új OCT-alapú, kifejezetten a nagyméretű (MLD >400 μm) FTMH-ak értékelésére alkalmas klasszifikációs rendszert. MLD szerint a 26. ábrán látható kategóriák különíthetők el.
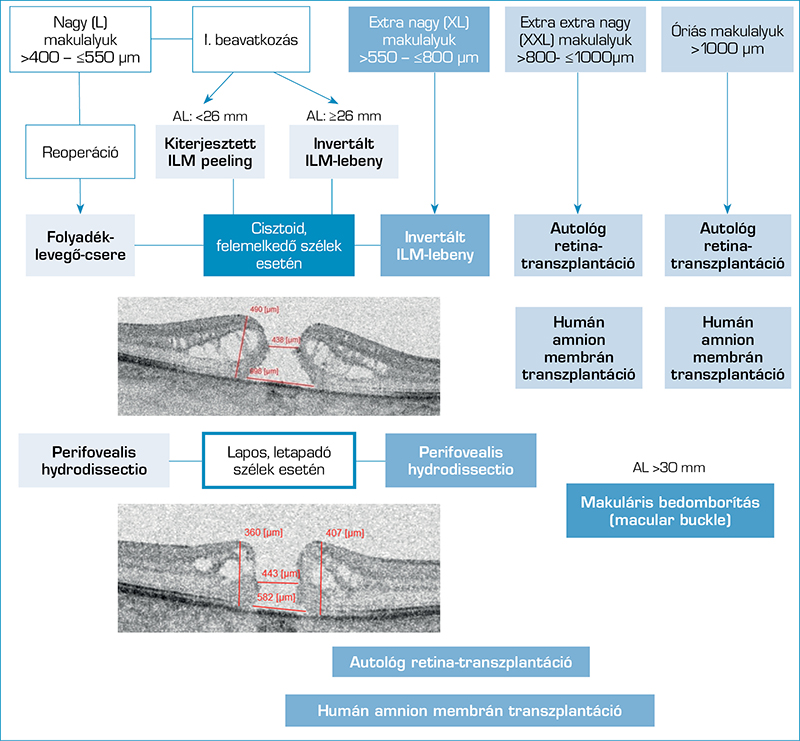
A felosztás klinikailag releváns, mivel a záródási arány és a funkcionális kimenetel szoros összefüggést mutat a preoperatív MLD-vel. Ez az osztályozás kezelési algoritmust nyújtva a műtéti stratégia megválasztását is segíti. A 400 µm feletti makulalyukaknál a standard technika (PPV ILM peelinggel és gáztamponáddal) eredményessége elmarad a kisebb makulalyukaknál tapasztaltakhoz képest, ezért ezekben az esetekben már a primer műtétnél javasolt az augmentált sebészi technikák, mint például a kiterjesztett vagy invertált ILM-flap, alkalmazása. Lapos, letapadó szélek esetén perifoveális hydrodissectio preferálandó. Refrakter, illetve nagyon nagy átmérőjű makulalyuk esetén további alternatív technikák jöhetnek szóba. Ide tartozik többek között az autológ szövetek felhasználása (pl. autológ retinagraft), valamint biológiai segédanyagok alkalmazása (pl. a humán amnionmembrán-transzplantáció). Ezen eljárások célja nem csupán a mechanikus defektus fedése, hanem a gliasejtes proliferáció és a retina regenerációs folyamatait támogató mikrokörnyezet kialakítása is (53).
Az augmengtációs technikák megjelenése új szempontokat hozott a műtét anatómiai sikerességének megítélésében. Az OCT-felvételeken a retina rétegeinek pontos megjelenítése és elkülönítése révén lehetőség nyílt arra is, hogy elkülönítsünk bizonyos záródási mintázatokat, amelyek összefüggésben állnak a posztoperatív funkcionális eredményekkel.
Imai és munkatársai három FTMH záródási mintázatot írt le: U-típusú (normális foveális kontúr) (27. ábra), V-típusú (meredek foveális kontúr) (28. ábra) és W-típusú (a neuroszenzoros retina foveális defektusa) (29. ábra). A posztoperatív látóélesség az U-típusnál volt a legjobb, ezt követte a V-típus, míg a legrosszabb eredmény a W-típusú csoportban volt megfigyelhető (24).
Rossi és munkatársai 2020-ban publikált egy részletes, SD-OCT-alapú osztályozást a makulalyukak műtét utáni anatómiai záródási mintázatainak leírására, amely túlmutat a korábbi, egyszerű „nyitott” vagy „zárt” megközelítésen. Az új rendszer a retina rétegeinek posztoperatív helyreállását veszi alapul, és három fő záródási típust különít el. A 0-s típus esetén a lyuk nem záródik, és a retina folytonossága nem áll helyre; ezen belül a szélek lehetnek laposak, megemelkedettek vagy ödémásak. Ezek az esetek anatómiai sikertelenséget jelentenek, következményes rossz funkcionális kimenetellel. Az 1-es típus valódi anatómiai záródást tükröz. Az 1A altípusban mind a belső, mind a külső retinarétegek helyreállnak (27. ábra), ami a legkedvezőbb látóélesség-javulással társul. Az 1B altípusra a belső rétegek záródása mellett a külső retinarétegek hiányos regenerációja jellemző (30. ábra), míg az 1C altípusban a külső retinarétegek folytonossága figyelhető meg, a belső rétegek részleges defektusával. A 2-es típusú záródás olyan helyzeteket ír le, amikor az FTMH anatómiailag záródik, de nem a retina rétegeinek helyreállásával, hanem idegen (pl. amnionmembrán) vagy autológ szövet (pl. ILM-lebeny, autológ retinaszövet) közbeiktatásával (31. ábra). Ilyenkor a retina fotoreceptor-rétegének folytonossága megszakad, a lyuk fedetté válik, de a normális rétegszerkezet nem áll helyre teljes mértékben. Funkcionális javulás ezekben az esetekben is detektálható (pl. csökken a centrumban látott fekete folt mérete) (55).
Kezelés
Alapvetően az idiopátiás makulalyuk kezelése elsősorban műtéti.
Az imminens makulalyuk, ahol tulajdonképpen nincs teljes vastagságú defektus, csak VMT intraretinális pszeudocisztákkal (Gass 1A, 1B stádium) obszerválható, mert az állapot gyakran stabil marad vagy spontán javulhat, és nincs evidencia arra, hogy a műtét javítaná a prognózist (2).
A traumás makulalyukak (TMH) több mint 80%-a spontán záródhat a traumát követő fél éven belül, amit az magyarázhat, hogy a TMH zömében a fiatalabb korosztályban fordul elő, ahol az üvegtest még egészséges, elasztikusabb, így a vitreofoveális kontaktus fiziológiás. Ugyanakkor, Qi Zhou és munkatársai által 2021-ben publikált 36 tanulmányt és 1009 szemet magába foglaló metaanalízise azt a következtetést közölte, hogy a vitrectomia hatékonyabb módszer a TMH kezelésére, mint az obszerváció. A vitrectomizált csoportban a TMH záródásának és a páciensek látóélesség javulásának aránya szignifikánsan magasabb volt, mint abban a csoportban, amelyik esetén a spontán záródást várva obszerváció mellett döntöttek (74).
A Kelly és Wendel által 1991-ben publikált, áttörést jelentő technika, amelyben gáztamponád alkalmazásával végzett PPV-t javasoltak posztoperatív pozicionálással, 58%-os záródási arányt eredményezett. Ez kiváló kimenetelt jelentett egy addig gyógyíthatatlannak tartott kórkép kezelésében (28).
A következő áttörést az ILM peeling bevezetése jelentette. Érdekes módon nem FTMH, hanem Terson-szindrómához társuló szub-ILM-vérzés megoldására írták le először 1990-ben (Morris és munkatársai). A makulalyuk sebészetében először Eckardt számolt be az ILM peeling alkalmazásáról 1997-ben. Újítása révén a műtétet követő záródási arány 90% fölé emelkedett. Napjainkban is az aranystandard-kezelés alatt az ILM peelinget és gáztamponádot alkalmazó PPV-t értjük (62).
Megemlítendő, hogy az FTMH miatt vitrectomián áteső betegeknél, tekintve az átlagos életkorukat, amikor már bizonyos fokú lencsehomály és a presbiopia jellemzően előfordul, gyakran szükséges és ajánlott egyidejű szürkehályog-ellenes műtét is. Kombinált műtétnél praktikusan a pars plana portok behelyezése után, a vitrectomia előtt végezzük. Jól készített, tisztán cornealis seb nem igényel varratot a műtét során. Tórikus műlencsék jó eredménnyel implantálhatók, multifokális műlencsék azonban nem javallottak. A kombinált műtét mellett szól az is, hogy a műtétet követő néhány éven belül a betegek több mint 80%-ában szürkehályog alakul ki, ráadásul a szürkehályog-ellenes műtét technikailag nehezebb vitrectomizált szemeken az írisz-lencse diafragma nagyfokú mobilitása miatt. Phacovitrectomia során hátsó capsulectomia is könnyű szerrel végezhető, megelőzve ezzel az egyébként gyakori utóhályog kialakulását, nem beszélve arról, hogy szükség esetén (pl. iatrogén retinaszakadás, -leválás) a periféria könnyebben megközelíthető, a komplikáció jobban kezelhető műlencse mellett. Ez fontos szempont lehet annak tükrében, hogy retinaszakadás az esetek 3-17%-ában, posztoperatív retinaleválás pedig 1-5%-ban fordulhat elő (2). Nem utolsó sorban a kombinált beavatkozás a beteg gyorsabb rehabilitációját eredményezi, és költséghatékonyabb (67).
A kombinált műtét ellen szól, hogy a korai posztoperatív szakban a műlencse elmozdulhat, írisz capture alakulhat ki, és gyakrabban jelenik meg CMO. Daud és munkatársai több mint 800 esetet involváló metaanalízise 12 hónapos követés során nem talált különbséget a kombinált és a szekvenciális műtéti csoport között sem a BCVA, sem a záródási ráta, sem pedig a szövődmények tekintetében (9). Egy 2024-ben publikált retrospektív összehasonlító tanulmányban viszont a hosszú távon mért látóélesség tekintetében a kombinált műtéti csoport alulteljesített a konszekutív műtétekkel szemben (48).
Nagyméretű (MLD >400 μm) FTMH-ak esetén a posztoperatív záródási arány, ezáltal a potenciális látásjavulás esélye rosszabb a kisebb makulalyukaknál tapasztaltakhoz képest. Napjaink makulasebészetében az egyik fő törekvés ezen makulalyukak műtéti eredményességének javítása. Ehhez alternatív műtéti technikákra van szükség. Frisina és munkatársai 2020-as, a refrakter FTMH-ak aktuális sebészi megoldásáról szóló áttekintő tanulmányában a következő műtéttechnikai alcsoportokat határozták meg: autológ vérlemezke-koncentrátum, lencse kapszula lebenyátültetés, autológ ILM-lebeny transzplantáció (szabad ILM-lebeny), ILM peeling kiterjesztése, perifoveális hydrodissectio, autológ retinagraft, szilikonolaj, humán amnionmembrán-transzplantáció, perifoveális relaxáló retinotomia, ívelt temporális retinotomia (15).
Az alábbiakban néhány, általunk is alkalmazott alternatív technika kerül rövid ismertetésre.
Az ILM-lebeny technika során az ILM-et nem teljes egészében távolítjuk el a makula környezetéből, hanem egy részét a makulalyuk széléhez rögzülve meghagyjuk, majd visszahajtva a lyuk fölé pozícionáljuk (inverted flap). A kívánt nagyságú lebeny kialakítása nem mindig könnyű, segíthet, ha először a peelingelni kívánt területnek a temporális szélén, a makulára érintőleges irányban távolítunk el egy vékony ILM-csíkot, amire merőleges irányban, a csík adta szélességben indítjuk meg a lebeny kialakítását. Szintén nehézséget jelenthet a lebeny kívánt helyen tartása a folyadék-levegő csere során. Gyakorlatunkban a lebeny stabilizálása perfluorokarbon folyadékkal (PFCL) meg tudja akadályozni a lebeny elmozdulását vagy akaratlan „beszippantását” a folyadékeltávolítás alkalmával. A technika célja, hogy az ILM biológiai vázként szolgáljon, elősegítve a Müller-sejtek proliferációját és a retina záródását. Ezt a műtéti technikát egyre gyakrabban alkalmazzuk primer műtétként is nagyobb, a biomarkerek alapján rossz záródási hajlamú lyukak kezelésénél. Ghoraba és munkatársai 2023-ban publikált Cochrane tanulmánya szerint a nagy makulalyukak kezelésében az ILM-lebeny technikával végzett PPV segítségével jobb eredmények érhetők el, mint az tradicionális ILM peelinggel végzett PPV során (18).
A humán amnionmembrán-technika során a kipreparált közel kerek amnionmembrán-graftot a szubretinális térbe, a makulalyuk széle alá helyezik, ahol érintkezve az RPE sejtekkel, az in vitro modellek alapján, stimulálni képes ezen sejtek szaporodását (4).
A perifoveális hydrodissectio lényege, hogy az FTMH körül folyadékot juttatunk a szubretinális térbe, ezáltal mobilizáláljuk a feszes retinát elősegítve a lyukszélek közeledését. Elsősorban letapadt, merev szélű, refrakter lyukak esetén alkalmazzuk, amikor a módszer célja a retina biomechanikai tulajdonságainak megváltoztatása és ezzel a fiziológiás záródási folyamat támogatása. A módszer alkalmazható önállóan vagy más eljárások kiegészítéseként. A műtét során szükség esetén megnagyobbítjuk az ILM peeling területét, majd kis PFCL-gömbbel „lezárjuk” a lyukat, és finom hegyű tű vagy soft-tip kanül (pl. 41 vagy 38 gauge) segítségével fiziológiás sóoldatot injektálunk a retina alá kontrollált, lokális retinaleválást hozva létre. Ezt követően folyadék-levegő csere, gáztamponád, majd posztoperatív pozicionálás történik (69).
Az autológ retinagraft-technika során a beteg saját perifériás retinájából származó szövetrészlet kerül átültetésre a makulalyuk területére. A módszer alapelve, hogy a graft mechanikus támaszt nyújt a defektus záródásához, valamint biológiai vázként szolgálhat a glia- és idegszöveti regeneráció számára. Elsősorban nagyon nagy, illetve többszörösen sikertelen műtéten átesett refrakter FTMH-ak esetén jön szóba, amikor más, kevésbé invazív technikák nem vezettek eredményre. A műtét fő lépései közé tartozik a PPV és az ILM eltávolítása után egy megfelelő méretű retinagraft kimetszése a perifériáról, majd annak atraumatikus áthelyezése és pozicionálása a makulalyukba. A beavatkozást rendszerint hosszabb hatású tamponád (hosszabb felszívódási idejű gáz vagy szilikonolaj) egészíti ki. A technika komplexitása és a perifériás retina károsításának kockázata miatt gondos indikációt, tapasztalt operatőrt igényel (38).
Valamennyi technika esetén alkalmazunk gáz endotamponádot, egyes esetekben szilikonolajat. A leggyakrabban alkalmazott intraokuláris gázok és izovolémiás koncentrációjuk: 20% kén-hexafluorid (SF6), 16% hexafluor-etán (C2F6) és 14% perfluor-propán (C3F8), amelyek eltérő expanziós és felszívódási tulajdonságokkal rendelkeznek. A rövidebb hatású gázok elsősorban kisebb makulalyukak esetén elegendők, míg nagyobb vagy refrakter lyukaknál hosszabb hatású tamponád alkalmazása válhat indokolttá. A gáztamponád elősegíti a lyukszélek appozícióját és stabil mechanikai környezetet biztosít a korai posztoperatív záródáshoz, azonban felmerül, hogy kisméretű makulalyukaknál nem is feltétlenül szükséges endotamponád. Ennek igazolására további vizsgálatok szükségesek (30).
Ne felejtsük el szóban és írásban (a zárójelentésben) is figyelmeztetni a beteget, hogy amíg a bulbusban gázbuborék van, nem ülhet repülőgépre és nem mehet magashegyi környezetbe, mert a magasabb tengerszint feletti magasságban a gáz parciális nyomása megnövekszik, ami veszélyes mértékben megemelheti a szemnyomást. Az intraokuláris gáz jelenlétében korlátozott az inhalatív érzéstelenítők, mint például a dinitrogén-oxid használata hasonló okok miatt.
Az endotamponád használatához kapcsolódóan a pozicionálás hagyományosan elengedhetetlen része a posztoperatív menedzsmentnek. Célja, hogy a gázbuborék hosszú távon, minél teljesebben fedje a makulalyuk területét, és nagy felületi feszültségével segítse vízmentesen tartani, ezáltal támogatva az anatómiai záródást. Újabban azonban swept source OCT (SS-OCT) alkalmazásával követhetővé vált a makula posztoperatív állapota, ugyanis a készülékben használt nagyobb, 1058 nanométeres hullámhossz áthalad a gázbuborékon is. Ilyen módszerrel Ahn és munkatársai, illetve Kikushima és munkatársai azt találták, hogy az FTMH-ak 90,5%-a már az első napon záródik, illetve, hogy a záródási idő a lyukmérettel arányosan nő, de a nagy átmérőjű lyukaknál sem tart 3 napnál tovább. A rendelkezésre álló evidenciák alapján a 400 µm alatti makulalyukak esetében az arccal lefelé történő pozicionálás szükségessége már nem egyértelmű, míg 400 µm feletti lyukaknál a pozicionálás szignifikánsan javíthatja a záródási arányt és a funkcionális kimenetelt. A korai posztoperatív SS-OCT-vizsgálat lehetőséget ad a záródás dinamikájának megítélésére és a feleslegesen hosszú pozicionálás elkerülésére. A jelenlegi ajánlások szerint a pozicionálás optimális időtartama általában nem haladja meg a 3 napot, mivel a makulalyukak döntő többsége a műtétet követő első 24–72 órában záródik. A 400 µm-nél nagyobb makulalyukakkal rendelkező betegek esetében 3 napos, arccal lefelé történő pozícionálást javasolt, viszont a pozicionálás előnyei 3 nap után elapadnak (1, 51).
Fenti megállapítások különösen fontosak annak fényében, hogy a hosszú ideig tartó pozicionálás a beteg számára jelentős terhelést jelenthet, és ritkán neurológiai vagy mozgásszervi szövődményekkel is társulhat. Ennek megfelelően a posztoperatív menedzsment individualizálása javasolt, amely figyelembe veszi a makulalyuk méretét, morfológiáját, az alkalmazott sebészi technikát, valamint ideális esetben korai posztoperatív SS-OCT-vizsgálatok eredményét (51).
Következtetések
Közleményünkben a leggyakoribb sebészi makula betegségekre vonatkozó ismereteket kíséreltük meg összefoglalni. Terjedelmi korlátok miatt nem tértünk ki az egyébként szintén jelentős miópiás trakciós makulopátia, a génterápia és a szubretinális implantátumok kérdéskörére.
A makulasebészet teljes vertikumában a diagnózistól a klasszifikáción és műtéti indikáción át a követésig alapvető jelentőséggel bír az OCT megjelenése és a képalkotás folyamatos fejlődése.
Alapvetően OCT segítségével született meg az LMH, a korábban sokféle lamelláris makulalézióval egybemosott elváltozás, konszenzus definíciója, valamint az EP leírása, és jelentőségének felismerése. Ennek eredményeként az LMH elsősorban obszerválandó entitásból egyre inkább operálható kategóriába sorolódik, az anatómiai és funkcionális javulás megalapozott esélyével.
Az ERM sebészete az utóbbi években az obszerváció-műtét skálán szintén az utóbbi felé mozdult, miközben a patofiziológiai alapú klasszifikációt egyre inkább a funkcionális szemléletű, OCT-alapú osztályozás váltja le (lásd Govetto), ami a műtéti indikáció és a prognózis felállításában hatékonyabb segítséget nyújt az operatőröknek.
A makulalyukak sebészetében a fókusz az eddig kisebb eredményességgel kezelt nagy, 400 micron feletti léziók területére helyeződött. A CLOSE-study új klasszifikációja a nagyméretű makulalyukak (MLD >400 μm) teljes spektrumára vonatkozó terápiás algoritmust kínál a tengelyhosszt és az FTMH morfológiáját is figyelembe véve, ami műtéti prognózis jelentős javulását eredményezte mind a primer, mind a reoperációk tekintetében. A már korábban is eredményesen kezelt kisebb FTMH-ak területén a minimál invazivitás szemlélete, a műtéttel járó megterhelés csökkentése ad új távlatokat, mint például a korai posztoperatív szakban SS-OCT-vel nyert ismereteink a beteget jelentősen terhelő pozicionálás elvetésének, illetve időtartama csökkentésének irányába mutatnak.
Nyilatkozat
A szerzők kijelentik, hogy a pontszerző, továbbképző tanulmány megírásával kapcsolatban nem áll fenn velük szemben pénzügyi vagy egyéb lényeges összeütközés, összeférhetetlenségi ok, amely befolyásolhatja a közleményben bemutatott eredményeket, az abból levont következtetéseket vagy azok értelmezését.
Rövidítések:
BCVA: legjobb korrigált látóélesség; BLD: alap lineáris átmérő; CMO: cisztoid makulaödéma; CRT: centrális retinavastagság; CSFT: a fovea átlagos vastagsága a centrális 1 mm átmérőjű területen; DRIL: belső retinarétegek dezintegrációja; EIFL: ektopikus belső foveális rétegek; EP: epiretinális proliferáció; ERM: epiretinális membrán; EZ: ellipszoid zóna; FD: foveális depresszió; FTMH: teljes vastagságú makulalyuk; H: makulalyuk magassága; ILM: belső határhártya; INL: belső magvas réteg; IRC: intraretinális ciszta; IZ: interdigitációs zóna; LHEP: lamelláris makulalyukhoz asszociált epiretinális proliferáció; LMH: lamelláris makulalyuk; MDRF: maximális retinaredő-mélység; MLD: minimum lineáris átmérő; MM: metamorfopszia; MMO: mikrocisztás makulaödéma; MPH: makuláris pszeudoforámen; OCT: optikai koherencia tomográfia; PFCL: perfluorokarbon folyadék; PPV: pars plana vitrectomia; PV: pneumatikus vitreolízis; PVD: hátsó üvegtesti határhártya-leválás; RNFL: retinális idegrostréteg; RPE: retinális pigmentepithel; SD-OCT: spectral domain-OCT; SRF: szubretinális folyadék; SS-OCT: swept source-OCT; TMH: traumás makulalyuk; VMA: vitreomakuláris adhézió; VMT: vitreomakuláris trakció
Irodalom
1. Ahn SJ, Park SH, Lee BR. VISUALIZATION OF THE MACULA IN GAS-FILLED EYES: Spectral Domain Optical Coherence Tomography Versus Swept-Source Optical Coherence Tomography. Retina 2018; 38(3): 480–489.
https://doi.org/10.1097/IAE.0000000000001560
2. American Academy of Ophthalmology. Idiopathic Macular Hole Preferred Practice Pattern. Edited by Susan Garratt. American Academy of Ophthalmology 2024. Available at: www.aao.org/ppp
3. Bergamo VC, Caiado RR, Maia A, et al. Role of Vital Dyes in Chromovitrectomy. Asia Pac J Ophthalmol (Phila) 2020; 10(1): 26–38. Published 2020 Nov 24. https://doi.org/10.1097/APO.0000000000000344
4. Capeáns C, Piñeiro A, Pardo M, et al. Amniotic membrane as support for human retinal pigment epithelium (RPE) cell growth. Acta Ophthalmol Scand 2003; 81(3): 271–277.
https://doi.org/10.1034/j.1600-0420.2003.00076.x
5. Chehaibou I, Tadayoni R, Hubschman JP, et al. Natural History and Surgical Outcomes of Lamellar Macular Holes. Ophthalmol Retina 2024; 8(3): 210–222.
https://doi.org/10.1016/j.oret.2023.09.016
6. Chen HJ, Hsiao CH, Chang CJ. Efficacy of Combined Vitrectomy with Intravitreal Corticosteroid Injection for Idiopathic Epiretinal Membrane Removal on Anatomical and Functional Outcomes: A Meta-Analysis. Ophthalmologica 2022; 245(3): 218–229.
https://doi.org/10.1159/000522263
7. Chua PY, Sandinha MT, Steel DH. Idiopathic epiretinal membrane: progression and timing of surgery. Eye (Lond) 2022; 36(3): 495–503.
https://doi.org/10.1038/s41433-021-01681-0
8. Daud F, Daud K, Popovic MM, et al. Combined versus Sequential Pars Plana Vitrectomy and Phacoemulsification for Macular Hole and Epiretinal Membrane: A Systematic Review and Meta-Analysis. Ophthalmol Retina 2023; 7(8): 721–731.
https://doi.org/10.1016/j.oret.2023.03.017
9. Duker JS, Kaiser PK, Binder S, et al. The International Vitreomacular Traction Study Group classification of vitreomacular adhesion, traction, and macular hole. Ophthalmology 2013; 120(12): 2611–2619.
https://doi.org/10.1016/j.ophtha.2013.07.042
10. Essex RW, Hunyor AP, Moreno-Betancur M, et al. The Visual Outcomes of Macular Hole Surgery: A Registry-Based Study by the Australian and New Zealand Society of Retinal Specialists. Ophthalmol Retina 2018; 2(11): 1143–1151.
https://doi.org/10.1016/j.oret.2018.04.022
11. Faatz H, Hattenbach LO, Krohne TU, et al. Vitreomakuläre Traktion: Diagnostik, natürlicher Verlauf, Therapieentscheidung und Leitlinienempfehlungen [Vitreomacular traction: diagnostics, natural course, treatment decision and guideline recommendations]. Ophthalmologie 2024; 121(6): 470–475.
https://doi.org/10.1007/s00347-024-02042-4
12. Fabio Patelli, Stanislao Rizzo, Carl Awh (ed.): Macular Surgery. Springer Nature Schwitzerland; 2024.
13. Far PM, Yeung SC, Ma PE, et al. Effects of Internal Limiting Membrane Peel for Idiopathic Epiretinal Membrane Surgery: A Systematic Review of Randomized Controlled Trials. Am J Ophthalmol 2021; 231: 79–87.
https://doi.org/10.1016/j.ajo.2021.04.028
14. Figueroa MS, Govetto A, Steel DH, et al. Pars plana vitrectomy for the treatment of tractional and degenerative lamellar macular holes: Functional and Anatomical Results. Retina 2019; 39(11): 2090–2098.
https://doi.org/10.1097/IAE.0000000000002326
15. Frisina R, Gius I, Tozzi L, Midena E. Refractory full thickness macular hole: current surgical management. Eye (Lond) 2022; 36(7): 1344–1354.
https://doi.org/10.1038/s41433-020-01330-y
16. Fung AT, Galvin J, Tran T. Epiretinal membrane: A review. Clin Exp Ophthalmol 2021; 49(3): 289–308.
https://doi.org/10.1111/ceo.13914
17. Garg A, Ballios BG, Yan P. Spontaneous Closure of an Idiopathic Full-Thickness Macular Hole: A Literature Review. J Vitreoretin Dis 2021; 6(5): 381–390. Published 2021 Oct 24.
https://doi.org/10.1177/24741264211049873
18. Ghoraba H, Rittiphairoj T, Akhavanrezayat A, et al. Pars plana vitrectomy with internal limiting membrane flap versus pars plana vitrectomy with conventional internal limiting membrane peeling for large macular hole. Cochrane Database Syst Rev 2023; 8(8): CD015031. Published 2023 Aug 7.
https://doi.org/10.1002/14651858.CD015031.pub2
19. Govetto A, Lalane RA 3rd, Sarraf D, et al. Insights Into Epiretinal Membranes: Presence of Ectopic Inner Foveal Layers and a New Optical Coherence Tomography Staging Scheme. Am J Ophthalmol 2017; 175: 99–113.
https://doi.org/10.1016/j.ajo.2016.12.006
20. Hagenau F, Osterode EV, Klaas JE, et al. Long-Term Results of Adjunct Autologous Platelet-Rich Plasma in Lamellar Macular Hole Surgery Showing Lasting Restoration of Foveal Anatomy. Int J Mol Sci 2023; 24(5): 4589. Published 2023 Feb 27.
https://doi.org/10.3390/ijms24054589
21. Hári KA, Thury G, Héjja R, et al. Kurzus – Evidenciák és újdonságok a macula sebészetében. A Magyar Szemorvostársaság 2025. Kongresszusa, Siófok, 2025. 06. 19–21.
22. Hubschman JP, Govetto A, Spaide RF, et al. Optical coherence tomography-based consensus definition for lamellar macular hole. Br J Ophthalmol 2020; 104(12): 1741–1747.
https://doi.org/10.1136/bjophthalmol-2019-315432
23. Ichikawa Y, Imamura Y, Ishida M. Associations of aniseikonia with metamorphopsia and retinal displacements after epiretinal membrane surgery. Eye (Lond) 2018; 32(2): 400–405.
https://doi.org/10.1038/eye.2017.201
24. Imai M, Iijima H, Gotoh T, Tsukahara S. Optical coherence tomography of successfully repaired idiopathic macular holes. Am J Ophthalmol 1999; 128(5): 621–627.
https://doi.org/10.1016/s0002-9394(99)00200-7
25. John VJ, Flynn HW Jr, Smiddy WE, et al. Clinical course of vitreomacular adhesion managed by initial observation. Retina. 2014; 34(3): 442–446.
https://doi.org/10.1097/IAE.0b013e3182a15f8b
26. Johnson RN, Gass JD. Idiopathic macular holes. Observations, stages of formation, and implications for surgical intervention. Ophthalmology 1988; 95(7): 917–924.
https://doi.org/10.1016/s0161-6420(88)33075-7
27. Kanzaki Y, Shinichiro D, Matoba R, et al. Objective and quantitative estimation of the optimal timing for epiretinal membrane surgery on the basis of metamorphopsia. Retina April 2022; 42(4): 704–711.
https://doi.org/10.1097/IAE.0000000000003401
28. Kelly NE, Wendel RT. Vitreous surgery for idiopathic macular holes. Results of a pilot study. Arch Ophthalmol 1991; 109(5): 654–659.
https://doi.org/10.1001/archopht.1991.01080050068031
29. Khan MA, Haller JA. Ocriplasmin for Treatment of Vitreomacular Traction: An Update. Ophthalmol Ther 2016; 5(2): 147–159.
https://doi.org/10.1007/s40123-016-0062-6
30. Kikushima W, Imai A, Toriyama Y, Hirano T, Murata T, Ishibashi T. Dynamics of macular hole closure in gas-filled eyes within 24 h of surgery observed with swept source optical coherence tomography. Ophthalmic Res 2015; 53(1): 48–54.
https://doi.org/ 10.1159/000368437
31. Lai TT, Hsieh YT, Lee Y, Yang CM. Embedding and sparing of lamellar hole-associated epiretinal proliferation in the treatment of lamellar macular holes. Eye (Lond) 2022; 36(6): 1308–1313.
https://doi.org/10.1038/s41433-021-01631-w
32. Lee CY, Hsia Y, Yang CM. Formation and evolution of idiopathic lamellar macular hole-a pilot study. BMC Ophthalmol 2022; 22(1): 432. Published 2022 Nov 14.
https://doi.org/10.1186/s12886-022-02669-4
33. Machemer R. A new concept for vitreous surgery. 7. Two instrument techniques in pars plana vitrectomy. ArchOphthalmol 1974; 92(5): 407–412.
https://doi.org/10.1001/archopht.1974.01010010419009
34. Mafi M, Govetto A, Mahmoudinezhad G, et al. Pathogenesis of ectopic inner foveal layers and its impact on visual recovery after epiretinal membrane peeling. Retina 2025; 45(6): 1108–1116.
https://doi.org/10.1097/IAE.0000000000004418
35. Matoba R, Morizane Y. Epiretinal membrane: an overview and update. Jpn J Ophthalmol 2024; 68(6): 603–613.
https://doi.org/10.1007/s10384-024-01127-6
36. Matoba R, Morizane Y. Surgical Treatment of Epiretinal Membrane. Acta Med Okayama 2021; 75(4): 403–413.
https://doi.org/10.18926/AMO/62378
37. Mihalache A, Huang RS, Ahmed H, et al. Pars Plana Vitrectomy with or without Internal Limiting Membrane Peel for Epiretinal Membrane: A Systematic Review and Meta-Analysis. Ophthalmologica 2024; 247(1): 30–43.
https://doi.org/10.1159/000534851
38. Moysidis SN, Koulisis N, Adrean SD, et al. Autologous Retinal Transplantation for Primary and Refractory Macular Holes and Macular Hole Retinal Detachments: The Global Consortium. Ophthalmology 2021; 128(5): 672–685.
https://doi.org/10.1016/j.ophtha.2020.10.007
39. Nakashizuka H, Kitagawa Y, Wakatsuki Y, et al. Prospective study of vitrectomy for epiretinal membranes in patients with good best-corrected visual acuity. BMC Ophthalmol 2019; 19(1): 183. Published 2019 Aug 14.
https://doi.org/10.1186/s12886-019-1185-z
40. Okada M, Chiu D, Yeoh J. Vitreomacular disorders: a review of the classification, pathogenesis and treatment paradigms including new surgical techniques. Clin Exp Optom 2021; 104(6): 672–683.
https://doi.org/10.1080/08164622.2021.1896946
41. Ozóg MK, Nowak-Was M, Rokicki W. Pathophysiology and clinical aspects of epiretinal membrane – review. Front Med (Lausanne) 2023; 10: 1121270. Published 2023 Aug 10.
https://doi.org/10.3389/fmed.2023.1121270
42. Özdemir HB, Özdek Ş, Hasanreisoğlu M. Pneumatic Vitreolysis for the Treatment of Vitreomacular Traction Syndrome. Turk J Ophthalmol 2019; 49(4): 201-208.
https://doi.org/10.4274/tjo.galenos.2019.00400
43. Pandya BU, Grinton M, Mandelcorn ED, Felfeli T. Retinal optical coherence tomography imaging biomarkers: A Review of the Literature. Retina 2024; 44(3): 369–380.
https://doi.org/10.1097/IAE.0000000000003974
44. Pandya BU, Popovic MM, Patil NS, Al-Rubaie S, Kertes PJ, Muni RH. Preoperative Visual Acuity Thresholds in Pars Plana Vitrectomy for Epiretinal Membrane: A Systematic Review. Ophthalmic Surg Lasers Imaging Retina 2024; 55(7): 400–407.
https://doi.org/10.3928/23258160-20240223-01
45. Pang CE, Maberley DA, Freund KB, et al. Lamellar hole-associated epiretinal proliferation: A Clinicopathologic Correlation. Retina 2016; 36(7): 1408–1412.
https://doi.org/10.1097/IAE.0000000000001069
46. Paspulati A, Punjabi OS, Theodoropoulou S, Singh RP. Triamcinolone acetonide as an adjuvant to membrane peeling surgery: a pilot study. Ophthalmic Surg Lasers Imaging Retina 2013; 44(1): 41–45.
https://doi.org/10.3928/23258160-20121221-11
47. Patheja RS. Preoperative ocular coherence tomographic prognosticators of visual acuity after idiopathic epiretinal membrane surgery. Int Ophthalmol 2022; 42(10): 3243–3252.
https://doi.org/10.1007/s10792-022-02317-2
48. Prabhu V, Gandhi P, Kathare R, et al. Phacovitrectomy vs. consecutive vitrectomy for idiopathic macular holes: short and long-term outcomes and OCT image quality assessment. Int J Retina Vitreous 2024; 10(1): 92. Published 2024 Dec 6.
https://doi.org/10.1186/s40942-024-00614-9
49. Quiroz-Reyes MA, Quiroz-Gonzalez EA, Quiroz-Gonzalez MA, et al. Pneumatic vitreolysis versus vitrectomy for the treatment of vitreomacular traction syndrome and macular holes: complication analysis and systematic review with meta-analysis of functional outcomes. Int J Retina Vitreous 2023; 9(1): 33. Published 2023 May 22.
https://doi.org/10.1186/s40942-023-00472-x
50. Quiroz-Reyes MA, Quiroz-Gonzalez EA, Quiroz-Gonzalez MA, et al. Surgical management, use and efficacy of adjuvant dyes in idiopathic epiretinal membranes: a systemic review with network meta-analysis. Int J Retina Vitreous 2023; 9(1): 77. Published 2023 Dec 6.
https://doi.org/10.1186/s40942-023-00515-3
51. Raimondi R, Tzoumas N, Toh S, et al. Facedown Positioning in Macular Hole Surgery: A Systematic Review and Individual Participant Data Meta-Analysis. Ophthalmology 2025; 132(2): 205.
https://doi.org/10.1016/j.ophtha.2024.08.012
52. https: //www.retina-specialist.com/article/top-10-oct-terms-for-vitreoretinal-surgery , hozzáférés dáruma: 2025. június
53. Rezende FA, Ferreira BG, Rampakakis E, et al. Surgical classification for large macular hole: based on different surgical techniques results: the CLOSE study group. Int J Retina Vitreous 2023; 9(1): 4. Published 2023 Jan 30.
https://doi.org/10.1186/s40942-022-00439-4
54. Ricardi F, Gelormini F, Parisi G, et al. The no-retina-touch technique: vitrectomy and platelet-rich plasma in the treatment of lamellar macular hole. New insights into pathogenesis. Eye (Lond). 2025; 39(2): 300–306.
https://doi.org/10.1038/s41433-024-03414-5
55. Rossi T, Bacherini D, Caporossi T, et al. Macular hole closure patterns: an updated classification. Graefes Arch Clin Exp Ophthalmol 2020; 258(12): 2629–2638.
https://doi.org/10.1007/s00417-020-04920-4
56. Ruiz-Moreno JM, Staicu C, Piñero DP, et al. Optical coherence tomography predictive factors for macular hole surgery outcome. Br J Ophthalmol 2008; 92(5): 640–644.
https://doi.org/10.1136/bjo.2007.136176
57. Sadeghi E, Colorado-Zavala MF, Almuhtaseb H, et al. Anatomical and functional changes after internal limiting membrane peeling. Surv Ophthalmol 2025; 70(3): 357–368.
https://doi.org/10.1016/j.survophthal.2025.01.008
58. Schechet SA, DeVience E, Thompson JT. The effect of internal limiting membrane peeling on idiopathic epiretinal membrane surgery, with a review of the literature. Retina 2017; 37(5): 873–880.
https://doi.org/10.1097/IAE.0000000000001263
59. Shiode Y, Morizane Y, Takahashi K, et al. Embedding of lamellar hole-associated epiretinal proliferation combined with internal limiting membrane inversion for the treatment of lamellar macular hole: a case report. BMC Ophthalmol 2018; 18(1): 257. Published 2018 Sep 24.
https://doi.org/10.1186/s12886-018-0926-8
60. Shiode Y, Morizane Y, Toshima S, et al. Surgical Outcome of Idiopathic Epiretinal Membranes with Intraretinal Cystic Spaces. PLoS One 2016; 11(12): e0168555. Published 2016 Dec 19.
https://doi.org/10.1371/journal.pone.0168555
61. Shiraga F, Takasu I, Fukuda K, et al. Modified vitreous surgery for symptomatic lamellar macular hole with epiretinal membrane containing macular pigment. Retina 2013; 33(6): 1263–1269.
https://doi.org/10.1097/IAE.0b013e31828bcb61
62. Steel DH, Donachie PHJ, Aylward GW, et al. Factors affecting anatomical and visual outcome after macular hole surgery: findings from a large prospective UK cohort. Eye (Lond) 2021; 35(1): 316–325.
https://doi.org/10.1038/s41433-020-0844-x
63. Shpak AA, Shkvorchenko DO, Sharafetdinov IKh, Yukhanova OA. Predicting anatomical results of surgical treatment of idiopathic macular hole. Int J Ophthalmol 2016; 9(2): 253–257. Published 2016 Feb 18.
https://doi.org/10.18240/ijo.2016.02.13
64. Tadayoni R, Gaudric A, Haouchine B, Massin P. Relationship between macular hole size and the potential benefit of internal limiting membrane peeling. Br J Ophthalmol 2006; 90(10): 1239–1241.
https://doi.org/10.1136/bjo.2006.091777
65. Takano SI, Ishida M, Ichikawa Y, et al. Optical coherence tomography-based epiretinal membrane stage correlates with tangential retinal displacement and metamorphopsia. Retina 2024; 44(12): 2140–2145.
https://doi.org/10.1097/IAE.0000000000004237
66. Tayyab H, Siddiqui R, Jahangir S, et al. Optical Coherence Tomography based indices in predicting functional outcome of macular hole surgery: A retrospective chart review. Pak J Med Sci 2021; 37(5): 1504–1508.
https://doi.org/10.12669/pjms.37.5.4126
67. Theocharis IP, Alexandridou A, Gili NJ, et al. Combined phacoemulsification and pars plana vitrectomy for macular hole treatment. Acta Ophthalmol Scand 2005; 83(2): 172–175.
https://doi.org/10.1111/j.1600-0420.2005.00417.x
68. Thury G, Baranyi N, Rárosi F, et al. Efficacy of aflibercept in vitrectomized vs. non-vitrectomized eyes with diabetic macular edema: a prospective study. Int J Retina Vitreous 2025; 12(1): 9. Published 2025 Dec 9.
https://doi.org/10.1186/s40942-025-00778-y
69. Tripepi D, Jalil A, Ally N, et al. The Role of Subretinal Injection in Ophthalmic Surgery: Therapeutic Agent Delivery and Other Indications. Int J Mol Sci 2023; 24(13): 10535. Published 2023 Jun 23.
https://doi.org/10.3390/ijms241310535
70. Ullrich S, Haritoglou C, Gass C, et al. Macular hole size as a prognostic factor in macular hole surgery. Br J Ophthalmol 2002; 86(4): 390–393.
https://doi.org/10.1136/bjo.86.4.390
71. Villegas VM, González MP, Berrocal AM, et al. Pharmacotherapy as an adjunct to vitrectomy. Ther Adv Ophthalmol 2021; 13: 25158414211016105. Published 2021 May 23.
https://doi.org/10.1177/25158414211016105
72. Yoon YH, Joe SG, Hwang JU, et al. Insights Into Epiretinal Membranes: Presence of Ectopic Inner Foveal Layers and a New Optical Coherence Tomography Staging Scheme. Am J Ophthalmol 2017; 177: 226–227.
https://doi.org/10.1016/j.ajo.2017.01.033
73. Zhang WF, Zhao XY, Meng LH, et al. The efficacy and safety of ocriplasmin for patients with vitreous macular traction. Acta Ophthalmol 2022; 100(1): e304–e313.
https://doi.org/10.1111/aos.14867
74. Zhou Q, Feng H, Lv H, et al. Vitrectomy vs. Spontaneous Closure for Traumatic Macular Hole: A Systematic Review and Meta-Analysis. Front Med (Lausanne) 2021; 8: 735968. Published 2021 Dec 23.
https://doi.org/10.3389/fmed.2021.735968
75. Zur D, Iglicki M, Feldinger L, et al. Disorganization of Retinal Inner Layers as a Biomarker for Idiopathic Epiretinal Membrane After Macular Surgery-The DREAM Study. Am J Ophthalmol 2018; 196: 129–135.
https://doi.org/10.1016/j.ajo.2018.08.037
