Is Central Retinal Thickness a Relevant Biomarker of Visual Acuity During Anti-Vascular Endothelial Growth Factor Therapy for Exudative Age-Related Macular Degeneration?
doi: https://doi.org/10.55342/szemhungarica.2025.162.1.20
Original scientific paper
Summary
Purpose: To investigate the relationship between best-corrected visual acuity (BCVA) and central retinal thickness (CRT) in eyes receiving anti-vascular endothelial growth factor (VEGF) for exudative age-related macular degeneration (AMD).
Methods: In our retrospective case series study, we compared the CRT values of the spectral-domain optical coherence tomography (SD-OCT) images of 37 eyes of 37 patients treated with exudative AMD with the BCVA values examined at the same time. We compared CRT and BCVA values measured before anti-VEGF (aflibercept) treatment and in the twelfth month of treatment. The relationship between the changes in the two parameters during the treatment was analysed using Pearson correlation.
Results: The average CRT decreased from 467.8 (±20.3) µm measured before the start of treatment to 321.4 (±11.3) µm by the 12th month. Compared to baseline, the mean value of BCVA increased from 56.8 (±1.7) to 63.8 (±2.2) letters at 12 months. At the beginning of the study, we measured a low correlation between BCVA and CRT values (r=–0.379). After 12 months of treatment, there was no detectable correlation between CRT and BCVA (r=–0.082), and in the 12th month no correlation was found between the changes of BCVA and CRT compared to the baseline value (r= 0.307).
Conclusion: The low correlation between CRT and BCVA measured at baseline was not detectable in the 12th month of treatment and the change between the two time points suggest that the progression of visual acuity is a combination of more complex processes. In line with clinical experience, visual function is not solely determined by changes in CRT.
Összefoglaló
Célkitűzés: A legjobb korrigált látóélesség (BCVA) és a centrális retinavastagsága (CRT) közötti összefüggés vizsgálata nedves típusú makuladegeneráció miatt antivaszkuláris endothelialis növekedési faktor (VEGF) terápiában részesülő szemekben.
Betegek és módszerek: Retrospektív, esetszéria tanulmányunkban 37 nedves típusú makuladegenerációval egyszemes kezelésben részesülő beteg 37 szeméről készült spectral-domain optikai koherencia tomográfia (SD-OCT) felvétel CRT értékeit hasonlítottuk össze az azonos időben vizsgált BCVA-értékekkel. Az összes BCVA-érték ugyanazon olvastató által került meghatározásra. Összehasonlítottuk az anti-VEGF- (aflibercept) kezelés előtti, a kezelés 12. hónapjában mért CRT- és BCVA-értékeket. A kezelés alatt a két paraméterben bekövetkező változás összefüggését Pearson-korrelációval elemeztük.
Eredmények: A kezelés megkezdése előtt mért 467,8 (±20,3) µm-ről a 12. hónapra 321,4 (±11,3) µm-re csökkent az átlag CRT. A kiinduláshoz képest a BCVA átlagos értéke 56,8 (±1,7) betűről 63,8 (±2,2) betűre emelkedett a 12. hónapra. A vizsgálat kezdetén alacsony korrelációt mértünk a BCVA- és a CRT-értékek között (r=–0,379). 12 hónapos kezelést követően nem volt kimutatható korreláció a CRT és a BCVA között (r=–0,082), illetve a 12. hónapban nem találtunk összefüggést a BCVA és a CRT kiindulási értékhez viszonyított változásai között (r=0,307).
Következtetések: A kiinduláskor mért alacsony korreláció a CRT és a BCVA között a kezelés 12. hónapjában és a két időpont közötti változásban nem volt kimutatható, amiből arra következtethetünk, hogy a látóélesség alakulása komplexebb folyamatok együttese. A klinikai tapasztalatokkal összhangban a látásfunkciót nem kizárólag a CRT változása határozza meg.
Keywords
macular degeneration, optical coherence tomography, biomarker, visual acuity, central retinal thickness
Kulcsszavak
makuladegeneráció, optikai koherencia tomográfia, biomarker, látóélesség, centrális retinavastagság
Bevezetés
A nedves típusú időskori makuladegeneráció (age-related macular degeneration, rövidítve: nAMD) hazánkban és világszerte is a vezető vaksági okok között szerepel. Az AMD az Egyesült Államokban a 65 év feletti populációban a vezető vaksági ok, és az előrehaladottabb állapotai, mint a nAMD, illetve a retinalis pigmentepithelium elvékonyodásával járó geografikus atrófia megközelíthetőleg 1,75 millió embert érint (1, 2). A különböző vaszkuláris növekedésifaktor-gátló (anti-VEGF) hatóanyagok és kezelési stratégiák alkalmazásával hatékonyan csökkenthető a hirtelen kialakuló látásromlás, és késleltethető a látóélesség károsodása (3, 4). A kezelések hatásfokának két fő indikátora a látóélesség (BCVA – Best corrected visual acuity, legjobb korrigált látóélesség) vizsgálat során az ETDRS (Early Treatment of Diabetic Retinopathy Study) betűk száma, és a centrális retinavastagság (CRT – central retinal thickness, centrális retinavastagság) csökkenése (5, 6). Utóbbit optikai koherencia tomográfia (OCT) készülék segítségével mérjük (7). A nemzetközi tanulmányokban, és a mindennapi tapasztalatok szerint is a funkcionális javulás összefügg az anatómiai helyzet javulásával, leegyszerűsítve a CRT csökkenésével. A VEGF-gátló kezelés mellett a nagyobb tanulmányok szerint (ANCHOR (8), MARINA (9), CATT (10), VIEW (11) az első néhány kezelés után 6-10 betű javulás érhető el, amely évekig fenntartható megfelelő követés mellett (12).
A retinalis folyadék jelenléte jó mutatója lehet a betegség aktivitásának, illetve jó előrejelzője a látóélesség javulásának, de az intra- vagy subretinalis folyadék csökkenésének következményeként változó mértékben számíthatunk a makula szerkezetének, és funkciójának javulására (4, 13, 14).
Ma a „biomarker” szó alatt olyan morfológiai és strukturális elváltozásokat értünk, amelyek fontos információt szolgáltathatnak a betegség stádiumáról. Az OCT lehetővé teszi a látóélességgel összefüggő specifikus retinalis biomarkerek azonosítását a kiindulási állapotban, és információt nyújt a beteg látásjavulásáról az anti-VEGF-kezelést követően, így hatékony és személyre szabott kezelést kínál a nAMD kezelésére (13, 15).
Az OCT biomarkerek az nAMD-ben két különböző kategóriába sorolhatók. Egyrészt a folyadékok retinalis eloszlásán alapuló biomarkerek, másrészt a retina rétegeiben, a chorioideában vagy a vitreomakuláris határfelületen megfigyelhető specifikus jellemzők jelenlétén, vagy hiányán alapuló strukturális biomarkerek. A retinalis folyadékok az exsudatív AMD-ben figyelhetők meg, és a CNV (Chorioideal Neovascularisation, chorioidealis érújdonképződés) – az utóbbi időben MNV (Macular Neovascularisation, makuláris érújdonképződés) jelenlétét támasztják alá, míg a strukturális biomarkerek mind az exsudatív, mind a száraz AMD-ben megfigyelhetők, és csupán a betegség progressziójának jelzői. Trinh legutóbbi összefoglaló közleményében már több mint száz OCT biomarkert említ AMD vonatkozásában (16).
Célkitűzés
A BCVA és a CRT közötti összefüggés vizsgálata nAMD miatt anti-VEGF-terápiában részesülő szemekben. A kérdés felvetését az a klinikai megfigyelés adta, hogy több esetben jelentős anatómiai javulás mellett sem jön létre látásjavulás, és fordítva is tapasztaljuk, azaz a retinalis folyadékok perzisztálása ellenére mégis javul a látóélesség. Az anti-VEGF-kezelés célja a kóros retinalis folyadékok megszűntetése, és ezzel párhuzamosan a látás megőrzése, illetve javítása. Ennek a folyamatnak a részletesebb megértését célozza tanulmányunk.
Betegek és módszerek
Betegek
A Semmelweis Egyetem Szemészeti Klinikáján végzett retrospektív esetszéria tanulmányunkba 37 beteget vontunk be (13 férfi, 24 nő, átlagéletkor a bevonáskor 75,0±6,9 év), akik egyszemes kezelésben részesültek. Minden beteg kezelt szemének adatait elemeztük. A kezelés időtartama 12 hónap volt.
Kezelés
A betegek „treat and extend” protokollnak megfelelően alkalmanként 0,05 ml (2 mg) aflibercept (Eylea, Bayer) intravitreális injekcióban részesültek. A kezelési séma megfelelt a gyógyszerleirat aktuális adagolási sémájának. A feltöltő szakaszban az első 3 kezelést havonta adtuk, majd áttértünk a kéthavi adagolásra, amelyet 2 hetes időintervallumokkal növeltük stabil retinaszerkezet és látóélesség esetén (17). Ezzel a kezelési sémával individuálisan megtervezhető az optimális funkcionális eredményhez szükséges terápia, minimalizálható a szükséges injekciók száma, ami vizsgálatunkban: 7,2±1,2 volt.
Vizsgálatok
A BCVA meghatározását ETDRS- táblán végeztük standardizált körülmények között. Spectralis (Heidelberg Engineering Inc, Heidelberg, Németország) típusú spectral-domain OCT (SD-OCT) készülékkel felvételeket készítettünk a makula területéről 20 fokos szögben. Minden felvétel 49 párhuzamos horizontális metszetből állt. Minden metszetet 16 kép átlagolásából kalkulált a számítógép, aktív szemkövető rendszer (eye tracker) alkalmazása mellett. Csak olyan betegeket vontunk be a vizsgálatba, akiknél megfelelő képminőség (az elérhető max. 30-ból min. 20-as volt a jelerősség minden szelvényben) volt biztosítható. Felvétel készült a kezelés előtt, és minden további viziten 12 hónapig follow-up funkcióval, amely biztosította, hogy a retina ugyanazon pontjain tudtuk végezni az ismételt méréseket.
Vizsgált adatok
A BCVA értékelését az ETDRS-betűk számának változásával írtuk le. A CRT értékét a foveára centrált 1 mm sugarú körben a műszer saját szoftverének segítségével mértük meg.
Statisztikai elemzés
A kiindulási állapothoz képest bekövetkező változást Wilcoxon-teszt segítségével (Statistica 13, Statsoft Inc, USA) értékeltük. A p<0,05 értéket fogadtuk el szignifikáns különbségnek. Összehasonlítottuk az anti-VEGF-kezelés (aflibercept) előtti és a kezelés 12. hónapjában mért CRT- és BCVA-értékeket. A kezelés alatt a két paraméterben bekövetkező változás összefüggését Pearson-korrelációval (GraphPad Prism 5; p <0,05, Dotmatics) elemeztük.
Eredmények
A makula szerkezetében az anti-VEGF-kezelés hatására az OCT- felvételeken minden esetben szignifikáns javulást figyeltünk meg a subretinalis és/vagy az intraretinalis folyadék csökkenése, megszűnése esetén, illetve bizonyos esetekben a pigmenthám-leválás mértéke is csökkent (1. ábra). Az 1. kezelést követően minden szem esetében csökkent a CRT, átlagosan 138,5 ± 100,8 µm (min. 23, max. 437 µm) csökkenést mértünk.
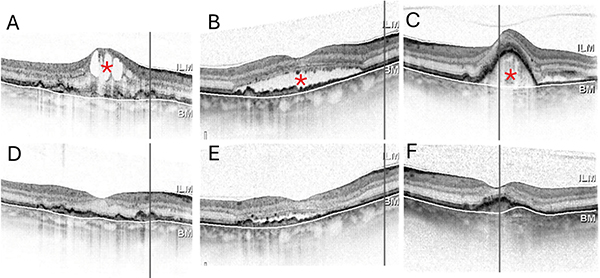
A BCVA átlagos értéke a kezelés végére mintegy 7 betűnyit javult, amely megfelel az irodalmi adatoknak. Egyidejűleg a CRT is szignifikáns csökkenést mutatott, közel 150 µm-t csökkent az átlagos centrális retinavastagság (1. táblázat).

A követési idő köztes időpontjaiban is feltüntettük a BCVA-értékeket. A látóélesség már az 1. hónapban javulást mutatott, amely fokozatosan tovább javult a 6. hónapig, majd stagnált (2. ábra).
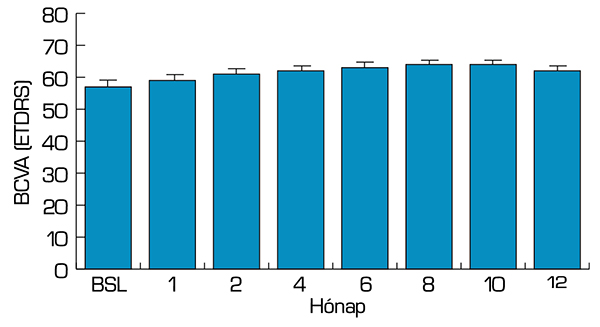
Ezzel párhuzamosan már az 1. hónapban jelentős csökkenés látszott a CRT-ben, amely fennmaradt a követési idő végéig (3. ábra).
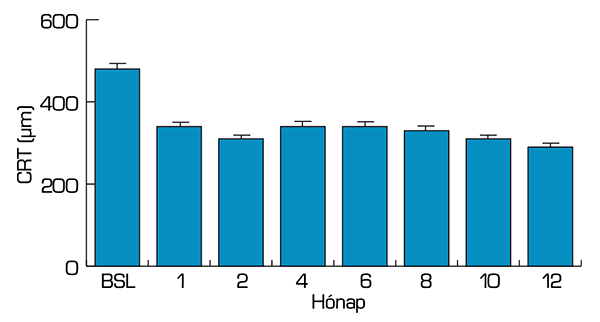
Statisztikai elemzésünk során a BCVA és a CRT között negatív korrelációt tudtunk kimutatni (p=0,0207, r= –0,3789) a kezelés megkezdése előtt (4. ábra).
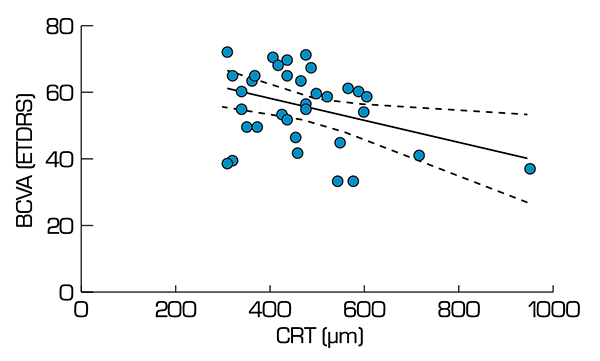
Az esetek jelentős részében a CRT 300 és 600 µm között változott. A követési idő végén a BCVA és a CRT közötti összefüggés nem volt szignifikáns, minimális negatív korrelációra utaló tendencia látszott (p=0,6134, r= –0,08236) (5. ábra).

Ezen az ábrán látható, hogy a CRT az esetek nagyobb részében 200-400 µm tartományba esett.
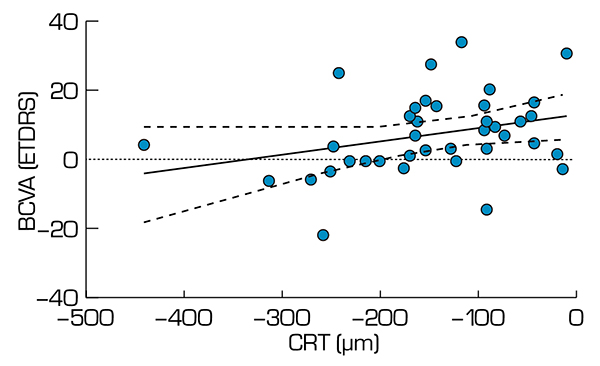
A klinikailag releváns kérdésre a változások közötti összefüggés vizsgálata mutatott rá. A változás értékeinek elemzésekor sem volt kimutatható szignifikáns korreláció a BCVA és a CRT között (p=0,0723, r=–0,3076) (6. ábra). A görbén látható, hogy az esetek többségében a BCVA-változás pozitív érték, tehát a látóélesség javult, viszont a CRT minden esetben negatív érték, tehát a kezelés hatására csökkent a makulaödéma mértéke. Voltak esetek, amikor a CRT jelentősen csökkent, de a látóélesség mégsem javult, és ellenkezőleg, nagyfokú látóélesség-javulást is észleltünk a CRT minimális csökkenése ellenére.
Megbeszélés
Vizsgálatunk megerősítette azt a klinikai tapasztalatot és vizsgálati eredményeket, miszerint az anti-VEGF-kezelés hatékonyan csökkenti a makula kóros folyadék gyülemét és stabilizálja, illetve javítja a látást. Több tanulmány is megállapította, hogy az nAMD változó aktivitásából eredő CRT-ingadozás negatív hatással van a végső látóélességre az anti-VEGF-terápiában részesülő betegeknél (18). Bár a retina bármelyik szöveti kompartmentjében bekövetkező fluktuáció negatív hatással van a látóélességre, az intraretinalis folyadéknak van a legrosszabb hatása a funkcióra. A vizsgálatok azonban eltérő eredményeket mutattak ki ezzel a korrelációval kapcsolatban, és úgy tűnik, hogy a CRT mégsem olyan pontos előrejelzője a látásfunkciónak (19). Valójában az egyéb paramétereket, például a folyadék elhelyezkedését, a fibrózist és az egyes retinarétegek integritását figyelembe vevő vizsgálatok pontosabbak lehetnek. A CRT önmagában azért nem jó biomarker, mert a különböző retinarétegeket egyben veszi figyelembe, amik önmagukban befolyásolhatják a funkcionális eredményeket. Különösen az intraretinalis cisztoid űrökről mutatták ki, hogy a többi folyadékjellemzőhöz képest a legnagyobb hatással van a CRT-re és a funkcióra (20). Az intraretinalis ciszták a kiinduláskor már meglévő retinakárosodást vagy az nAMD agresszívebb formáját jelezhetik, ami csökkenti a látóélesség helyreállításának lehetőségét. Ezen okok miatt fontos a retina rétegeiben lévő folyadékok eloszlásának elemzése nAMD-ben. Megkülönböztethetünk IRC-t (Intraretinal Cystoid Fluid, intraretinalis cisztoid folyadék), SRF-et (Subretinal Fluid, szubretinális folyadék), és PED-et (Pigment Epithelial Detachment, pigmenthám-leválás). Érdemes ezeket a folyadéktereket külön is részletesebben áttekinteni (21).
Intraretinalis cisztoid folyadék
Az IRC a retina belső rétegeiben felhalmozódó cisztoid folyadékként definiálható, amely jellemzően fokozott retinavastagsággal jár együtt vagy hiporeflektív cisztoid űrökként ábrázolódik. Az IRC általában a 2. és 3. típusú MNV-vel függ össze, de a betegség későbbi stádiumában az 1. típusú MNV-ben is előfordulhat. Számos átfogó irodalmi áttekintés az IRC-t a legfontosabb negatív prognosztikai biomarkernek minősíti nAMD-ben, amely a látásvesztés és a fibrózis vagy atrófia kialakulásának nagyobb kockázatával jár együtt (22). Az ezeken felül megjelenő cisztózus degeneráció már kezelést nem igényel, rossz funkcionális prognózist jelent. A külső retinalis tubuláció gyakran megfigyelhető, negatív prognosztikai jel, elsősorban a hosszú távú követések során (23). A kezelés kiindulásakor már meglévő/perzisztáló IRF negatív hatással van a kezelés elkezdése után várható BCVA-ra. Lokalizációt tekintve fontos, hogy a folyadék érinti-e a foveát, mivel a hiányzó, vagy csak extrafoveális elhelyezkedésű folyadék jobb prognózisú. A post hoc Harbor tanulmány szerint volumenfüggő az IRF hatása a visusra (20).
Subretinalis folyadék
Az SRF a fotoreceptorok külső határa és az RPE belső határa között megjelenő exsudáció. Az SRF a leggyakoribb folyadéklokalizáció az 1. típusú MNV-ben, és előfordulhat a 2. típusú MNV-vel összefüggésben is. A 3. típusú MNV-ben az SRF általában a PED fölötti IRC-vel együtt található. Az SRF jelenléte gyakran jobb látási eredményekkel és alacsonyabb atrófiaaránnyal jár, függetlenül az intravitreális kezelés gyakoriságától. Az ilyen szemek nagy része jól reagál treat and extend kezelési algoritmusra (24). Fontos megjegyezni, hogy az SRF-nek az IRF-hez képest kevésbé egyértelmű a megítélése. Nincs negatív korreláció a látóélességgel 1 év távlatában. A második évnél Jaffe szerint a látóélességre jó hatással van, az 5. évnél a fovea alatti SRF esetén jobb volt a látóélesség, mint nélküle (25–27). A 2. táblázatban foglaltuk össze az egyes folyadékterek látást befolyásoló jelentőségét.

Sub-RPE folyadék, PED
A PED-et az RPE és a Bruch-membrán belső kollagénrost rétege közötti elválása jellemzi. Az elválás által létrehozott helyet drusenoid anyag, savós exsudátum, vér, fibrovaszkuláris szövet vagy a fentiek kombinációja foglalja el. A drusenoid PED-ek leginkább a nem neovaszkuláris AMD-ben fordulnak elő. A szerózus PED-ek jellemzően az AMD neovaszkuláris formájához társulnak. Úgy tűnik, hogy kevésbé fontos a nAMD-ben szenvedő betegek látásprognózisa szempontjából, mint az IRC vagy az SRF jelenléte. A vaszkuláris PED-ek az 1. típusú (sub-RPE) neovaszkularizációval és nedves AMD-vel társulnak, és nagyobb látásvesztési kockázattal járnak. A fibrovaszkuláris PED az okkult MNV egy alcsoportja. AMD-s szemekben nem ritka, hogy többféle PED-típust látunk egyazon szemben.
Korábbi vizsgálatok eltérő korrelációt mutattak a CRT és a BCVA kapcsolatában
Eredményeink alapján önmagában a CRT nem megbízható prognosztikai faktora a várható funkciónak nAMD-ben. Habár a CRT a leggyakoribb és a legkönnyebben meghatározható OCT-paraméter, ma már más kvalitatív és kvantitatív biomarkerek pontosabb előrejelzői a betegség aktivitásának, kiváló prognosztikai értéket és útmutatást nyújtanak az individuális terápiás döntésekhez (28). A folyadékterek változásán túl a retina érszerkezeti változásai is részben magyarázatot szolgáltatnak az anatómiai és funkcionális eredmények eltéréseire (29–31)
Különösen érdekesek a retinalis folyadékterek korai változásai: Gigon és munkatársai 1 héttel és 1 hónappal az első injekciót követően elemezték a retina vastagságát, és azt tapasztalták, hogy az egy hónapnál már recidívát mutató esetekben is sokszor jó morfológia látszott 1 hétnél, ám egy hónapra már ismét jelentős folyadékmennyiség újult ki (32). Ma már elérhető az otthoni OCT-készülék is, amellyel a páciens akár naponta mérheti meg a saját retina vastagságát, így feltárhatók azok a változások, amely alapján az egyéni kezelési terv pontosítható (33).
A hosszú távú eredmények tekintetében egyértelművé válik, hogy az atrófia uralja a képet, így ebben a fázisban már a látóélességgel nincs korrelációban a CRT (26, 27). A sorvadás miatt kifejezetten elvékonyodik a makula a Seven-Up-tanulmány szerint is, amelyben azt találták, hogy a VEGF-gátlóval kezelt betegeknél a 2. év végére az esetek 95%-ában, és 7. év végére 100%-ban jelentős atrófia alakult ki (27). Ugyanezen tanulmány szerint 170 µm-re csökkent a neuroretina átlagos vastagsága a 7. év végére, amely jelentősen elmarad a normális állapottól.
Következtetések
Annak ellenére, hogy fejlett képalkotási technikák és kezelési lehetőségek állnak rendelkezésre, az nAMD még mindig a vezető vaksági okok közé tartozik Magyarországon is.
Saját kutatásunkban elemeztük a CRT és BCVA összefüggését anti-VEGF-kezelés vonatkozásában, kisebb, klinikai beteganyagon. Munkánkban a retinalis folyadék és látóélesség közötti változást vizsgáltuk. Saját eredményeink kapcsán anti-VEGF-kezelés megkezdése előtt alacsony korrelációt találtunk, míg a kezelés 12. hónapjában és a két időpont közötti változásban korreláció nem volt kimutatható a CRT és a BCVA között. A képalkotó technikák javulása mellett egyre több biomarker válik ismertté, amelyek komplex értékelése meghaladja a vizsgáló orvos lehetőségeit, ugyanakkor új utakat nyit meg a mesterséges intelligencia bevonása a képelemzésbe így előmozdítva a kezelési eredmények optimalizálását (34, 35).
Nyilatkozat
A szerzők kijelentik, hogy eredeti közleményük megírásával kapcsolatban nem áll fenn velük szemben pénzügyi vagy egyéb lényeges összeütközés, összeférhetetlenségi ok, amely befolyásolhatja a közleményben bemutatott eredményeket, az abból levont következtetéseket vagy azok értelmezését.
Irodalom
1. Kiss H, Németh J. A vakság okai Magyarországon. Szemészet 2013; 150: 103–110.
2. Bressler NM. Age-related macular degeneration is the leading cause of blindness. Jama 2004; 291: 1900–1.
https://doi.org/10.1001/jama.291.15.1900
3. Schmidt-Erfurth U, Chong V, Loewenstein A, Larsen M, Souied E, Schlingemann R, et al. Guidelines for the management of neovascular age-related macular degeneration by the European Society of Retina Specialists (EURETINA). Br J Ophthalmol 2014; 98: 1144–1167.
https://doi.org/10.1136/bjophthalmol-2014-305702
4. Papp A. Az időskori makuladegeneráció és modern kezelési lehetőségei. Magyar Orvos 2013; 21: 14–7.
5. Lukács R, Tóth-Kovács K, Pámer Zs. Anatómiai és funkcionális javulás korrelációja intravitrealis VEGF-gátló injekcióval kezelt időskori maculadegenerációban szenvedő betegeknél. Szemészet 2010; 147: 127–132.
6. Lukács R, Resch M, Papp A, Szabó A, Borbándy Á, Menkens H, Kiss H, Németh J. Hosszú távú intravitrealis ranibizumab kezelés exsudativ időskori maculadegenerációban. Orvosi Hetilap 2013; 154: 1790–1797.
7. Papp A. Az OCT szerepe az időskori macula degeneratio diagnosztikájában. In: Optikai koherencia tomográfia a szemészetben. Szerk. Nagy ZZ, Récsán Z. Budapest: Semmelweis Kiadó; 2008. p. 94–106.
8. Brown DM, Michels M, Kaiser PK, Heier JS, Sy JP, Ianchulev T. Ranibizumab versus verteporfin photodynamic therapy for neovascular age-related macular degeneration: Two-year results of the ANCHOR study. Ophthalmology 2009; 116: 57–65.
https://doi.org/10.1056/NEJMoa054481
9. Rosenfeld PJ, Brown DM, Heier JS, Boyer DS, Kaiser PK, Chung CY, et al. Ranibizumab for neovascular age-related macular degeneration. The New England journal of medicine 2006; 355: 1419–1431. 10.
https://doi.org/1056/NEJMoa054481
10. Martin DF, Maguire MG, Ying GS, Grunwald JE, Fine SL, Jaffe GJ. Ranibizumab and bevacizumab for neovascular age-related macular degeneration. The New England journal of medicine 2011; 364: 1897–1908. 10.
https://doi.org/1056/NEJMoa1102673
11. Mitchell P. VIEW Study Group. Intravitreal aflibercept versus ranibizumab for neovascular age-related macular degeneration: 52-week subgroup analyses from the combined VIEW studies. Clinical and Experimental Ophthalmology 2012; 40: 41–56.
12. Lotery A, Griner R, Ferreira A, Milnes F, Dugel P. Real-world visual acuity outcomes between ranibizumab and aflibercept in treatment of neovascular AMD in a large US data set. Eye (London, England) 2017; 31: 1697–706.
https://doi.org/10.1038/eye.2017.143
13. Kaiser PK, Wykoff CC, Singh RP, Khanani AM, Do DV, Patel H, Patel N. Retinal Fluid and Thickness as measures of Disease Activity in Neovascular Age-related Macular Degeneration. Retina 2021; 41: 1579–1586.
https://doi.org/10.1097/IAE.0000000000003194
14. Chaudhary V, Matonti F, Zarranz-Ventura J, Stewart MW. Impact of Fluid Compartments on Functional Outcomes for Patients with Neovascular Age-Related Macular Degeneration: A Systematic Literature Review. Retina 2022; 42: 589–606.
https://doi.org/10.1097/IAE.0000000000003283
15. Metrangolo C, Donati S, Mazzola M, Fontanel L, Messina W, D'alterio G, Rubino M, Radice P, Premi E, Azzolini C. OCT Biomarkers in Neovascular Age-Related Macular Degeneration: A Narrative Review. J Ophthalmol 2021; 2021: 9994098.
https://doi.org/10.1155/2021/9994098
16. Trinh M, Cheung R, Duong A, Nivison-Smith L, Ly A. OCT Prognostic Biomarkers for Progression to Late Age-related Macular Degeneration: A Systematic Review and Meta-analysis. Ophthalmol Retina 2024; 8: 553–565.
https://doi.org/10.1016/j.oret.2023.12.006
17. Patel PJ, Villavicencio P, Hanumunthadu D. Systematic Review of Neovascular Age-Related Macular Degeneration Disease Activity Criteria Use to Shorten, Maintain or Extend Treatment Intervals with Anti-VEGF in Clinical Trials: Implications for Clinical Practice. Ophthalmol Ther 2023; 12: 2323–2346.
https://doi.org/10.1007/s40123-023-00768-z
18. Bakri SJ, Thorne JE, Ho AC, Ehlers JP, Schoenberger SD, Yeh S, et al. Safety and Efficacy of Anti-Vascular Endothelial Growth Factor Therapies for Neovascular Age-Related Macular Degeneration: A Report by the American Academy of Ophthalmology. Ophthalmology 2019; 126(1): 55–63.
https://doi.org/10.1016/j.ophtha.2018.07.028
19. Holland R, Kaye R, Hagag AM, Leingang O, Taylor TRP, Bogunović H, Schmidt-Erfurth U, Scholl HPN, Rueckert D, Lotery AJ, Sivaprasad S, Menten MJ. Deep Learning-Based Clustering of OCT Images for Biomarker Discovery in Age-Related Macular Degeneration (PINNACLE Study Report 4). Ophthalmol Sci 2024 May 31; 4(6): 100543.
https://doi.org/10.1016/j.xops.2024.100543
20. Sadda SR, Tuomi LL, Ding B, Fung AE, Hopkins JJ. Macular Atrophy in the HARBOR Study for Neovascular Age-Related Macular Degeneration. Ophthalmology 2018; 125: 878–886.
https://doi.org/10.1016/j.ophtha.2017.12.026
21. Moraes G, Struyven R, Wagner SK, Liu T, Chong D, Abbas A, Chopra R, Patel PJ, Balaskas K, Keenan TDL, Keane PA. Quantifying Changes on OCT in Eyes Receiving Treatment for Neovascular Age-Related Macular Degeneration. Ophthalmol Sci 2024 Jun 28; 4(6): 100570.
https://doi.org/10.1016/j.xops.2024.100570
22. Ho AC, Saroj N, Baker K, Vitti R, Berliner AJ, Thompson D, Roth DB. Impact of Baseline Characteristics on Treatment Response to Intravitreal Aflibercept Injection for Wet Age-Related Macular Degeneration. Ophthalmol Retina 2018; 2: 676–683.
https://doi.org/10.1016/j.oret.2017.10.017
23. Kovacs A, Kiss T, Rarosi F, Somfai GM, Facsko A, Degi R. The effect of ranibizumab and aflibercept treatment on the prevalence of outer retinal tubulation and its influence on retreatment in neovascular age-related macular degeneration. BMC Ophthalmol 2018; 18: 298.
https://doi.org/10.1186/s12886-018-0960-6
24. Silva R, Berta A, Larsen M, Macfadden W, Feller C, Mones J. Treat-and-Extend versus Monthly Regimen in Neovascular Age-Related Macular Degeneration: Results with Ranibizumab from the TREND Study. Ophthalmology 2018; 125: 57–65.
https://doi.org/10.1016/j.ophtha.2017.07.014
25. Jaffe GJ, Ying GS, Toth CA, Daniel E, Grunwald JE, Martin DF, Maguire MG; Comparison of Age-related Macular Degeneration Treatments Trials Research Group. Macular Morphology and Visual Acuity in Year Five of the Comparison of Age-related Macular Degeneration Treatments Trials. Ophthalmology 2019; 126: 252–260.
https://doi.org/10.1016/j.ophtha.2018.08.035
26. Rofagha S, Bhisitkul RB, Boyer DS, Sadda SR, Zhang K. Seven-year outcomes in ranibizumab-treated patients in ANCHOR, MARINA, and HORIZON: a multicenter cohort study (SEVEN-UP). Ophthalmology 2013; 120(11): 2292–9.
https://doi.org/10.1016/j.ophtha.2013.03.046
27. Bhisitkul RB, Mendes TS, Rofagha S, Enanoria W, Boyer DS, Sadda SR, et al. Macular atrophy progression and 7-year vision outcomes in subjects from the ANCHOR, MARINA, and HORIZON studies: the SEVEN-UP study. American journal of ophthalmology 2015; 159(5): 915–24.
https://doi.org/10.1016/j.ajo.2015.01.032
28. Ohji M, Okada AA, Sasaki K, Moon SC, Machewitz T, Takahashi K; ALTAIR Investigators. Relationship between retinal fluid and visual acuity in patients with exudative age-related macular degeneration treated with intravitreal aflibercept using a treat-and-extend regimen: subgroup and post-hoc analyses from the ALTAIR study. Graefes Arch Clin Exp Ophthalmol 2021; 259: 3637–3647.
https://doi.org/10.1007/s00417-021-05293-y
29. Resch M, Németh C, Barcsay Gy, Ecsedy M, Borbándy Á, Géhl Z, Balogh A, Szabó A, Nagy ZZ, Papp A. Szemfenéki érfestés festék nélkül: Az optikai koherencia tomográfia alapú angiográfia exsudativ típusú időskori maculadegenerációban. Orvosi Hetilap 2016; 157: 1683–1690.
https://doi.org/10.1556/650.2016.30548
30. Resch MD, Balogh A, Deak GG, Nagy ZZ, Papp A. Vascular density in age-related macular degeneration after one year of antiVEGF treatment with treat-and-extend and fixed regimens. PloS one 2020; 15(2).
https://doi.org/10.1371/journal.pone.0229388
31. Resch MD, Balogh A, Kurth T, Nagy ZZ, DeBuc DC, Papp A. Atrophy of retinal vessels in neovascular age-related macular degeneration following long-term treatment with 20 intravitreal anti-VEGF injections. BMC Ophthalmol 2022; 22: 469. https://doi.org/10.1186/s12886-022-02700-8
32. Gigon A, Iskandar A, Kasser S, Naso S, Zola M, Mantel I. Short-term response to anti-VEGF as indicator of visual prognosis in refractory age-related macular degeneration. Eye (Lond) 2024; 38: 1342–1348.
https://doi.org/10.1038/s41433-023-02900-6
33. Liu Y, Holekamp NM, Heier JS. Prospective, Longitudinal Study: Daily Self-Imaging with Home OCT for Neovascular Age-Related Macular Degeneration. Ophthalmol Retina 2022; 6: 575–585.
https://doi.org/10.1016/j.oret.2022.02.011
34. Keenan TDL, Clemons TE, Domalpally A, Elman MJ, Havilio M, Agrón E, Benyamini G, Chew EY. Retinal Specialist versus Artificial Intelligence Detection of Retinal Fluid from OCT: Age-Related Eye Disease Study 2: 10-Year Follow-On Study. Ophthalmology 2021; 128: 100–109.
https://doi.org/10.1016/j.ophtha.2020.06.038
35. Valsecchi N, Shah S, Zarnegar A, Tang A, Yagobian S, Fontana L, Iannetta D, Chhablani J. Assessment of optical coherence tomography biomarkers in patients with non-neovascular age-related macular degeneration (AMD) converting to exudative AMD according to the status of the fellow eye. Eye (Lond) 2024 Sep 20. Epub ahead of print. PMID: 39304740.
https://doi.org/10.1038/s41433-024-03357-x
