Evaluation and management of Descemet’s membrane detachment related to cataract surgery
doi: 10.55342/szemhungarica.2025.162.2.77
Case report
Summary
Introduction:Descemet membrane detachment (DMD) mostly occurs as an intraoperative complication of intraocular interventions, especially cataract surgeries. There are many risk factors, and the frequency of DMD is surprisingly high, but it often remains hidden in the absence of clinical symptoms and signs. However, in cases of central involvement or large extent, choosing the optimal management can be challenging for the surgeon.
Materials and Methods:: Our case presentation aims to demonstrate the anterior segment optical coherence tomography (AS-OCT)-based evaluation and management of cataract surgery-related DMD with the help of AS-OCT images and literature data.
Case report: During the incision closure of a 64-year-old male patient’s routine cataract surgery, we experienced the separation of corneal layers. An AS-OCT examination was performed to determine the exact location and extent of the DMD. After the shortage of air injected into the anterior chamber and conservative therapy, we decided to apply 20% SF6 intracamerally. As a result of this therapy, the DMD resolved.
Discussion: Since clinically manifest cases may occur less frequently, DMD is thought to be an uncommon complication related to cataract surgery; however, according to literature data, it can be observed in nearly 43% of operations. It should be considered in cases of persistent postoperative corneal oedema. Among the various classifications, we highlight the HELP algorithm, which provides a therapeutic approach in the management of DMD using AS-OCT-based parameters (the DMD’s height, extension, length and position to the pupil).
Összefoglaló
Bevezetés: A Descemet-membrán-leválás (Descemet Membrane Detachment, DMD) leggyakrabban iatrogén eredettel, főként szürkehályogműtétek szövődményeként fordul elő. Számos kockázati tényezőt ismerünk és előfordulási gyakorisága meglepően magas, viszont sokszor rejtve marad a klinikai tünetek és jelek hiányában. Centrális érintettség vagy nagyfokú kiterjedés esetén azonban a megfelelő terápia megválasztása kihívást jelenthet az operatőr számára.
Célkitűzés és módszerek: Esetünk kapcsán bemutatjuk a szürkehályogműtét során bekövetkező DMD elülső szegment optikai koherencia tomográfia (AS-OCT) alapú értékelését és ellátását betegünk AS-OCT-felvételei és irodalmi adatok felhasználásával. Esetismertetés: Egy 64 éves férfi beteg rutin szürkehályogműtéte során a sebzáráskor a szaruhártya rétegeinek szétválását tapasztaltuk. AS-OCT-vizsgálat segítségével láthatóvá vált a DMD pontos lokalizációja és kiterjedése. Az elülső csarnokba injektált levegő és a konzervatív terápia (5%-os NaCl-oldat, levofloxacin, dexamethason cseppek) kudarca után 20% SF6 intracameralis beadása mellett döntöttünk. Az alkalmazott terápia hatására a DMD megszűnt, a szaruhártya feltisztult és a beteg látólessége javult.
Megbeszélés: Mivel klinikailag manifeszt esetek ritkán figyelhetők meg, a DMD-t nem a leggyakoribb szürkehályogműtéttel kapcsolatos szövődményként tartjuk számon, habár irodalmi adatok szerint az operációk közel 43%-ánál előfordul. Tartósan fennálló posztoperatív szaruhártya-ödéma esetén gondolni kell rá. A különböző osztályozási módok közül a HELP-algoritmust emeljük ki, amely AS-OCT felhasználásával mért paraméterek (a DMD magassága, kiterjedése, hosszúsága és pupillához való helyzete) segítségével nyújt terápiás ajánlást a DMD ellátásában.
Keywords
Descemet membrane detachment, anterior segment OCT, HELP algorithm
Kulcsszavak
Descemet-membrán-leválás, elülső szegment OCT, HELP-algoritmus
Bevezetés
A Descemet-membrán a corneális endothelium bazálmembránja. Együttesen képezik az endothelium-Descemet-membrán komplexet, amelynek fontos szerepe van a cornea dehidrált állapotának, és ezáltal transzparenciájának fenntartásában. Descemet-membrán-leválás (Descemet Membrane Detachment, DMD) során ez a komplex elválik a stromától, így funkcióját elvesztve a cornea vizet vesz fel, transzparenciája csökken (1, 6, 21). A kórképet először Weve és munkatársai azonosították 1927-ben, majd idővel különböző szempontok szerint kezdték el osztályozni (1, 21).
A DMD-nek etiológia szerint 3 fő típusát tudjuk megkülönböztetni. Beszélhetünk iatrogén, traumás és spontán formáról. Leggyakrabban a iatrogén DMD-vel találkozhatunk, amely szemészeti műtétek, beavatkozások kapcsán fellépő komplikáció (1, 6, 21). Szürkehályogműtétek során a DMD előfordulása közel 43% (1, 12, 20, 21). Ezek többsége azonban klinikailag nem jelentős, és a műtétet követő napokban spontán megszűnik. A klinikailag manifeszt DMD előfordulása ennél jóval kisebb, ECCE (extracapsularis cataracta extractio) esetében 2,6%, míg phacoemulsificatio esetén 0,5% (1, 12). Egyéb bulbusmegnyitó műtétek, pl. keratoplasztika, trabeculectomia, kapcsán is számolnunk kell ezzel a szövődménnyel, de különböző lézeres beavatkozások, pl. Nd:YAG-lézer iridotomia/capsulotomia, után is leírták már (1, 21, 23). A traumás formák elsősorban kémiai sérülések vagy tompa traumák következtében alakulhatnak ki (1, 6, 15, 16, 21). Spontán megjelenés esetén valamilyen predisponáló tényező (pl. corneadisztrófia) jelenléte szükséges. Ilyenkor komplikációmentes műtétet követően hetekkel-hónapokkal később alakul ki a DMD (1, 2, 6, 17, 21, 22).
A iatrogén DMD kialakulási esélyének minimalizálása érdekében fontos a rizikófaktorok ismerete. Ezek egy része már preoperatívan jelen van és nem befolyásolhatók. Ilyen a beteg előrehaladott életkora vagy valamilyen corneadisztrófia fennállása (1, 6, 21). A kockázati tényezők másik nagy csoportját a befolyásolható, intraoperatív faktorok képezik. A helytelen sebészi technikák mind fokozhatják a DMD előfordulását (1, 6, 10, 21). Különösen fontos a corneális sebkészítés technikája. A corneális sebnek fontos tulajdonsága többek között a mérete, alakja vagy mélysége, amelyek pontos kivitelezése komoly kihívást jelenthet nem megfelelő eszközök vagy tapasztalatlan operatőr esetén (3, 4, 10).
A DMD diagnózisának felállítása során klinikai tünetek és jelek mellett különböző szemészeti képalkotó módszerek is segítségünkre lehetnek (1, 6, 18, 19, 21). Legtöbb esetben a DMD kicsi, és spontán gyógyul, ezért észrevétlen marad, azonban néhány esetben, ha a leválás kiterjedt és a centrumot is involválja, a páciensnek panaszt, látásromlás okoz (1, 6, 21). Réslámpás vizsgálat során a DMD áttetsző membránként jelenhet meg az elülső csarnokban, ún. „kettős elülső csarnok” megjelenést eredményezve, de általában a kifejezett corneaödéma miatt ez nem vizualizálható (1, 6, 21). Súlyos, nem javuló posztoperatív szaruhártya-ödéma esetében gondolni kell rá, és további vizsgálatokat kell elvégezni a pontos diagnózis érdekében. Számos diagnosztikus módszer segítségünkre lehet, pl. gonioszkópia, elülső szegment optikai koherencia tomográfia (AS-OCT), ultrahang biomikroszkópia (UBM), Scheimpflug-kamera, vagy éppen a különböző OCT-n alapuló biométer készülékek is (1, 6, 18, 19, 21). Esetismertetésünk kapcsán elsősorban az AS-OCT jelentőségét emeljük ki a DMD diagnózisában és terápiájának megválasztásában.
Esetismertetés
Egy 64 éves férfi beteg jobb szemének phacoműtéte az utolsó lépésig komplikációmentesen, lege artis zajlott, majd a corneális sebzáráskor a szaruhártya rétegeinek szétválását észleltük. Állapotrögzítés és dokumentáció céljából AS-OCT-vizsgálatot végeztünk, amelyen jól látszódott a DMD lokalizációja és kiterjedése (1. ábra).
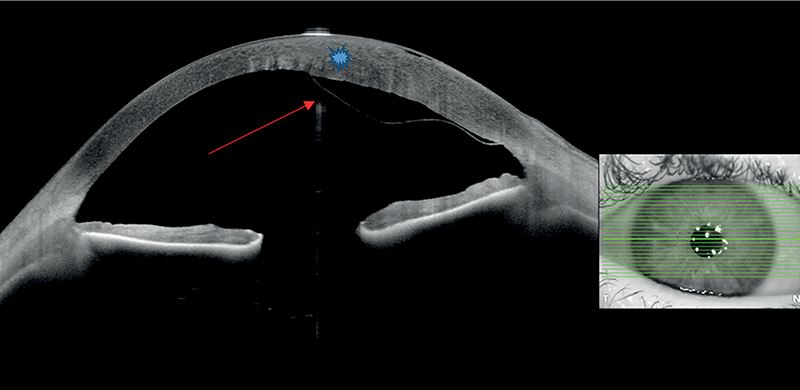
Ekkor intracameralis levegő beadása mellett döntöttünk. A beteget 3 nappal később kontrollvizsgálatra hívtuk vissza, amelynek során azt észleltük, hogy a DMD nem változott, a beteg legjobb korrigált látóélessége (BCVA) 0,9 volt. A beteggel egyeztetve hipertóniás, 5%-os NaCl-oldat óránkénti cseppentését rendeltük el a már eddig is alkalmazott topikális antibiotikum és gyulladáscsökkentő kezelés kiegészítéseként. Az 1 héttel későbbi viziten a DMD továbbra is fennállt, elhelyezkedése, magassága és hosszúsága változatlan volt (2. ábra), de a corneaödéma fokozódott, vastagsága nőtt és ennek megfelelően a beteg látóélessége is romlott, a BCVA már csak 0,6 volt.
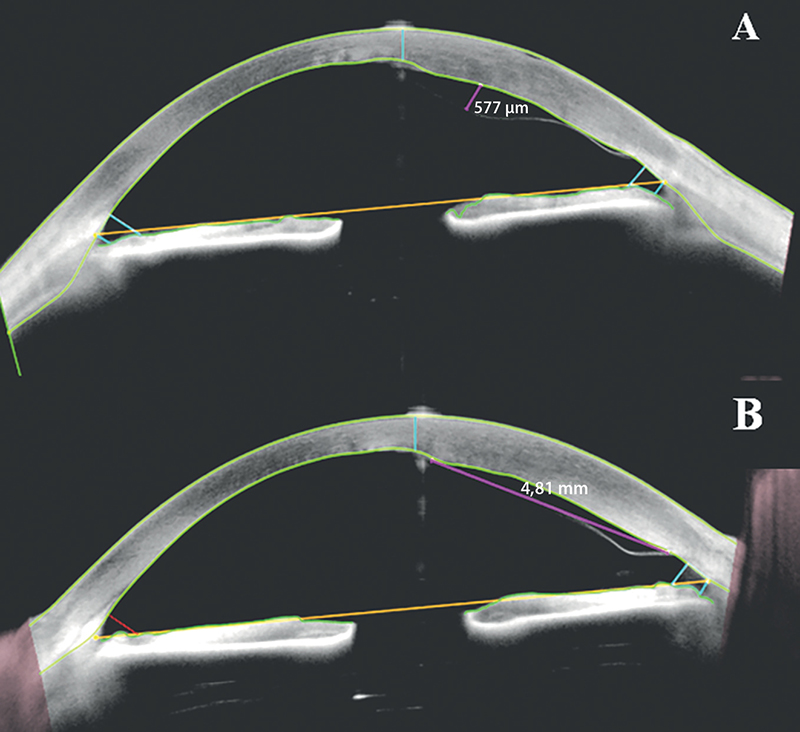
Ekkor a descemetopexia megismétlése mellett döntöttünk, intracameralisan 20% SF6 gázt alkalmaztunk. A beavatkozás során 30 G-s tű segítségével a DMD-vel ellentétes oldalon történt a gáz beadása az elülső csarnokba. A pácienst ajánlásoknak megfelelően 20 percig háton fekvő pozícióba helyeztük, majd a beadott gázbuborék 1/3-át leengedtük, hogy elkerüljük a posztoperatív pupilláris blokkot (21). Otthonában a háton fekvő pozíció folytatását javasoltuk a következő 3-5 napban, valamint az eddig is alkalmazott cseppterápia (levofloxacin, dexamethason és hipertóniás sóoldat) mellett cycloplegiát (ciclopentolat szemcsepp) írtunk elő, szintén annak érdekében, hogy csökkentsük a lehetséges szövődmények, elsősorban a pupilláris blokk kialakulásának esélyét. Felhívtuk továbbá a páciens figyelmét, hogy erős fájdalom esetén szemnyomásmérés és pupilláris blokk kizárása céljából soron kívül jelentkezzen ambulanciánkon. A következő, 1 héttel későbbi kontrollvizsgálaton azt tapasztaltuk, hogy a descemetopexia kapcsán szövődmény nem jelentkezett és a levált Descemet-membrán visszafeküdt, a corneaödéma megszűnt, amelyet AS-OCT-vizsgálattal is dokumentáltunk (3. ábra).
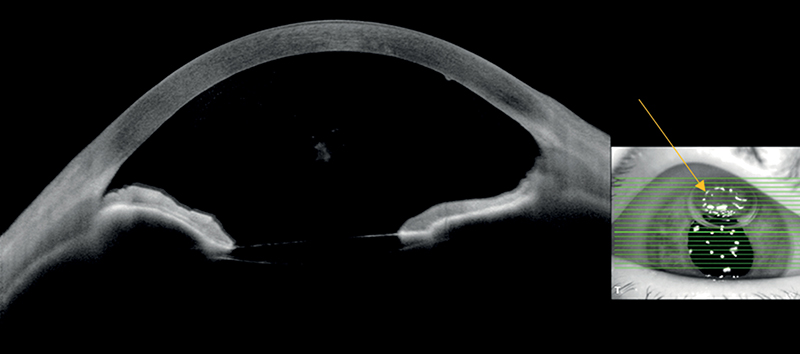
A beteg látóélessége ekkor még nem változott jelentősen, amelyet a szaruhártya hátlapján észlelt Descemet-membrán-redők magyaráztak. A harmadik hónapban történő ellenőrzésen a szaruhártya integritásának teljes helyreállását tudtuk AS-OCT-képpel rögzíteni (4. ábra).
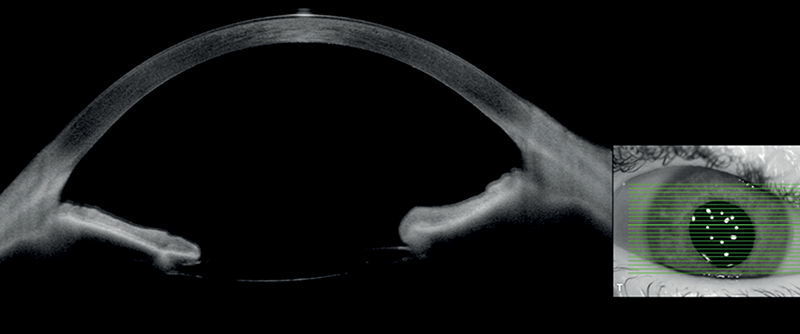
Megbeszélés
A mindennapi gyakorlatban a DMD-t nem a leggyakoribb szürkehályogműtéttel kapcsolatos szövődményként tartjuk számon, de az irodalmi adatok jól mutatják, hogy a szubklinikus formák meglehetősen gyakoriak. Klinikailag manifeszt esetek ugyan sokkal ritkábban fordulnak elő, de bizonyos jelek, különösen tartósan fennálló posztoperatív szaruhártya-ödéma esetén gondolnunk kell rá. A diagnózis, és ezáltal a megfelelő terápia késése jelentősen meghatározza a prognózist, ugyanis a DMD tartós fennállása a szaruhártya dekompenzációjához vezethet irreverzibilis strukturális változásokat (pl. endothelsejtek pusztulása, Descemet-membrán hegesedése) idézve elő (1, 21).
A DMD klasszifikációját tekintve számos megoldás született az évek alatt. Ezek kezdetben egyszerűek, elméleti jellegűek voltak és nem tartalmaztak terápiás ajánlásokat (1, 5, 19, 21). 2015-ben jelentek meg az első AS-OCT-alapú klasszifikációk, amelyek a DMD kiterjedését és morfológiáját alapul véve terápiás döntéshozatali algoritmust is megfogalmaztak (12, 20). Esetünk bemutatásával a HELP-algoritmust emeljük ki, ami egy jól követhető, gyakorlatias ellátási séma, amennyiben iatrogén, szürkehályogműtét kapcsán bekövetkező DMD-vel állunk szemben (12).
Az AS-OCT jelentősége abban rejlik, hogy kifejezett szaruhártya- ödéma jelenlétében gyakran lehetetlen a DMD pontos diagnózisát felállítani réslámpás vizsgálattal. Ilyen esetekben nehéz meghatározni a DMD konfigurációját, kiterjedését és elhelyezkedését, ami létfontosságú a kezelés megtervezésében (12, 13, 20).
A HELP egy mozaikszó, amely az AS-OCT segítségével mért DMD paraméterekre utal. A DMD magassága a „H” (height), a levált Descemet-membrán és a stroma közötti távolság μm-ben mérve. Az „E” (extent) azt jelzi, hogy a DMD mely zónáit érinti a szaruhártyának (5. ábra).
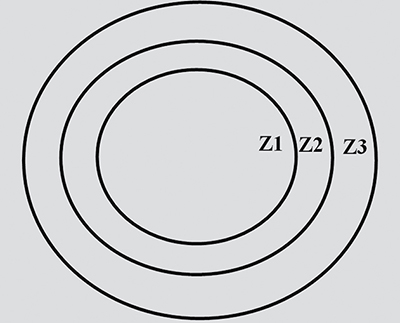
1. zóna (Z1): centrálisan elhelyezkedő, a centrumtól mért 5 mm sugarú kör alakú terület. 2. zóna (Z2): paracentrálisan elhelyezkedő, a centrumtól mért 5 és 8 mm sugarú körök közti gyűrű alakú terület. 3. zóna (Z3): perifériásan elhelyezkedő, a centrumtól mért 8 mm sugarú körtől távolabb fekvő terület. Az 1. zóna esetében külön ki kell térni a pupilláris érintettségre („P”), de a terápiát nem elsősorban ez, hanem a „H” (magasság) és az „L” (hosszúság) fogja befolyásolni (12)
A DMD hosszúsága az „L” (length), a levált Descemet-membrán két végpontja közti távolság mm-ben mérve. A DMD pupillához való helyzete tágítatlan pupilla mellett a „P” (pupil) (12). Utóbbit a gyakorlatban az „E” paraméterrel szoros összefüggésben értelmezzük.
A HELP-algoritmus Kumar és munkatársai által 2015-ben publikált, Indiában végzett prospekítv vizsgálat, amely 161 szem bevonásával készült. A fent megnevezett paramétereket alapul véve a következő ajánlást fogalmazták meg szürkehályogműtét kapcsán észlelt, korai posztoperatív DMD ellátásával kapcsolatban (12).
Konzervatív terápia:
- <100 µm magasságú és <1 mm hosszúságú, bármely zónában,
- 100–300 µm magasságú és 1-2 mm hosszúságú, amely a 2. és 3. zónát érinti,
- 300 µm magasságú és >2 mm hosszúságú, amely csak a 3. zónát érinti.
Sebészi terápia:
- 100–300 µm magasságú és 1-2 mm hosszúságú, amely az 1. zónát érinti,
- >300 µm magasságú és >2 mm hosszúságú, amely az 1. és 2. zónát érinti.
A konzervatív kezelés hipertóniás NaCl-oldat, antibiotikum és kortikoszteroid topikális alkalmazását foglalta magába, míg a műtéti beavatkozás descemetopexiát, azaz intracameralis gáz (14% C3F8 vagy 20% SF6) vagy steril levegő injekciót jelentett. Amennyiben a konzervatív terápia mellett 4 hét elteltével sem tapasztaltak javulást egyik vizsgált paraméterben sem, sebészi megoldáshoz folyamodtak (12).
A descemetopexia egyik leggyakoribb szövődménye a levegő/gázbuborék okozta pupilláris blokk kialakulása, amely az intraocularis nyomás jelentős megemelkedéséhez vezethet. Ennek kiküszöbölésére több módszer is létezik, többek között a páciens beavatkozás utáni pozícionálása, vagy a posztoperatívan alkalmazott cycloplegia. Szintén ajánlott kb. 15-20 perc után az elülső csarnokba adott gázbuborék 1/3-ának leengedése, hogy a pupilla alsó széle szabad legyen. Ennek hiányában preventív alsó lézeres perifériás iridotomia (LPI) elvégzése is indokolt lehet (1, 6, 21). Ritkábban egyéb komplikációk is előfordulhatnak, pl. uveitis vagy iris iszkémia (ún. Urrets Zavalia szindróma), amelynek oka az iris lencséhez történő kompressziója a levegő/gázbuborék által (21).
Irodalmi adatok szerint descemetopexia céljából levegő, 14% C3F8 vagy 20% SF6 is használható, de nincs egységes álláspont arra vonatkozóan, hogy melyik a hatékonyabb. Endothel-toxicitásuk állatkísérletekben hasonló volt, ugyanakkor egyes szerzők gáz alkalmazása mellett több esetben tapasztaltak szövődményt, pl. pupilláris blokkot, így biztonságossági szempontból érdemes lehet első körben a levegőt választani. Ezzel szemben komplikáltabb, terápiarefrakter esetekben már célszerű inkább a gázokat preferálni, mert a levegő gyorsan felszívódik, a gázok viszont hetekig (14%C3F8 6 hétig, 20%SF6 2 hétig) az elülső csarnokban maradnak, ezáltal tartósabban kifejtve hatásukat (1, 8, 21).
A descemetopexia primeren általában 90-100%-ban sikeres, csupán az esetek kis százalékában nem vezet eredményre. Ilyenkor mindenképp érdemes megismételni, mielőtt bonyolultabb eljárásokhoz folyamodnánk (1, 6, 8, 21). Az ismételt descemetopexia kudarca esetén számos további terápiás lehetőség áll rendelkezésre, ezek azonban megosztók hatékonyságukat és biztonságosságukat tekintve. Ide tartozik többek között a mechanikus tamponád (pl. intracameralis viszkoelasztikus anyag vagy perfluorocarbon folyadék) alkalmazása, a levált Descemet-mebrán varrattal történő rögzítése vagy manuális repozíciója is (1, 6, 21). Gab-Alla és munkatársai leírták, hogy a descemetopexia hatékonyságát növelheti, ha nem önmagában, hanem folyadék drenázzsal kombinálva végzik, főleg azokban az esetekben, amikor a primer descemetopexia kudarcot vallott (7). A Descemet-membrán és a stroma közötti folyadék eltávolítására különböző technikákat próbáltak már (14), a könnyebb kivitelezés és ellenőrizhetőség érdekében intraoperatív AS-OCT alkalmazása is javasolt lehet (1, 21). Végső megoldásként keratoplasztika jön szóba. A DMEK (Descemet Membrane Endothel Keratoplasty) és egyéb alternatív módszerek, pl. DSO (Descemet Srtipping Only), részesítendők előnyben a terápiarefrakter DMD-s esetek kezelésében (1, 11, 21). A lamelláris keratoplasztika lehet a megoldás azoknál a betegeknél is, akiknél a strukturális eredményt, azaz a DMD megszűnését nem követi funkcionális javulás a szaruhártya transzparenciáját negatívan befolyásoló Descemet-membrán-redők, hegek miatt (9).
Következtetés
Szürkehályogműtétek után tartósan fennálló posztoperatív szaruhártya-ödéma esetén gondoljunk DMD-re. Az AS-OCT kulcsfontosságú eszköz nemcsak a diagnózisban, hanem a legoptimálisabb kezelési módszer megválasztásában is. A kisebb kiterjedésű DMD-k általában spontán oldódnak, viszont nagyobb DMD-k esetén ez a spontán javulás kétesélyes és elhúzódó lehet. Ilyenkor gyakran maradnak vissza Descemet-membrán-redők vagy hegek a szaruhártyán. Ha ezek a centrumban alakulnak ki, a maradandó látásromlás veszélye nagy, ezért centrumot érintő DMD esetén nem szabad kockáztatni, azonnali sebészi terápiát kell alkalmazni. Amennyiben csak a szaruhártya perifériája érintett, a látáskárosodás lehetősége még hegesedés esetén is kisebb, így lehet konzervatív terápiával kezdeni. Esetünk során a HELP-algoritmust alapul véve sebészi beavatkozásra volt szükség, első lépésben inracameralis levegő, második lépésben intracameralis 20% SF6 gáz injekció formájában. A konzervatív terápia közbeiktatására páciensünknél azért volt szükség, mert aggodalmait fejezte ki az ismételt invazív beavatkozással kapcsolatban, de annak hatástalansága miatt végül beleegyezett a descemetopexia megismétlésébe, ami sikerhez vezetett.
Nyilatkozat
A szerzők kijelentik, hogy az esetismertetés megírásával kapcsolatban nem áll fenn velük szemben pénzügyi vagy egyéb lényeges összeütközés, összeférhetetlenségi ok, amely befolyásolhatja a közleményben bemutatott eredményeket, az abból levont következtetéseket vagy azok értelmezését.
Irodalom
1. Beniwal A, Vanathi M, Venugopal A, Chaurasia S, Tandon R. Descemet's membrane detachment: An updated comprehensive review of etiopathogenesis, diagnosis, and management. Indian J Ophthalmol 2024; 72(11): 1560–1568.
https://doi.org/10.4103/IJO.IJO_877_24
2. Bhatia HK, Gupta R. Delayed-onset descemet membrane detachment after uneventful cataract surgery treated by corneal venting incision with air tamponade: a case report. BMC Ophthalmol 2016; 16: 35. Published 2016 Apr 4.
https://doi.org/10.1186/s12886-016-0212-6
3. Dai Y, Liu Z, Wang W, et al. Incidence of Incision-Related Descemet Membrane Detachment Using Phacoemulsification With Trapezoid vs Conventional 2.2-mm Clear Corneal Incision: A Randomized Clinical Trial. JAMA Ophthalmol 2021; 139(11): 1228–1234.
https://doi.org/10.1001/jamaophthalmol.2021.4148
4. Dai Y, Liu Z, Wang W, et al. Real-Time Imaging of Incision-Related Descemet Membrane Detachment During Cataract Surgery. JAMA Ophthalmol 2021; 139(2): 150–155.
https://doi.org/10.1001/jamaophthalmol.2020.5396
5. Dua HS, Sinha R, D'Souza S, et al. “Descemet Membrane Detachment”: A Novel Concept in Diagnosis and Classification. Am J Ophthalmol 2020; 218: 84–98.
https://doi.org/10.1016/j.ajo.2020.05.038
6. https://eyewiki.org/Descemet_Membrane_Detachment , letöltés dátuma: 2025.március
7. Gab-Alla AA. A Comparative Study between Air Bubble Tamponade Alone versus Air Bubble Tamponade with Internal Fluid Aspiration for Nonplanar Descemet's Membrane Detachment after Phacoemulsification. J Ophthalmol 2021; 2021: 9953418. Published 2021 Jul 6.
https://doi.org/10.1155/2021/9953418
8. González AL, Silva F, Barrientos R, Paredes F. Descemet's Membrane Detachment: An Intraoperative Complication in Cataract Surgery with Phacoemulsification. Int Med Case Rep J 2020; 13: 673–677. Published 2020 Dec 1.
https://doi.org/10.2147/IMCRJ.S283770
9. Gupta S, Mahalingam K, Agarwal T. Spontaneous attachment of complex Descemet's membrane detachment following multiple failed interventions. BMJ Case Rep 2021; 14(8): e243960. Published 2021 Aug 13.
https://doi.org/10.1136/bcr-2021-243960
10. Gurnani B, Kaur K. Tips to prevent inadvertent stromal staining and Descemet membrane detachment while performing paracentesis during cataract surgery. Indian J Ophthalmol 2023; 71(5): 2300–2301.
https://doi.org/10.4103/IJO.IJO_3310_22
11. Khan NC, Lin CC. Descemet stripping only for Descemet's membrane detachment and sectoral corneal edema. Am J Ophthalmol Case Rep 2022; 29: 101784. Published 2022 Dec 24.
https://doi.org/10.1016/j.ajoc.2022.101784
12. Kumar DA, Agarwal A, Sivanganam S, Chandrasekar R. Height-, extent-, length-, and pupil-based (HELP) algorithm to manage post-phacoemulsification Descemet membrane detachment. J Cataract Refract Surg 2015; 41(9): 1945–1953.
https://doi.org/10.1016/j.jcrs.2015.01.020
13. Li F, Zhu Z, Fan L, Yi G, Zhu X, Li N. A Simple Repair Algorithm for Descemet's Membrane Detachment Performed at the Slit Lamp. J Clin Med 2022; 11(23): 7001. Published 2022 Nov 27.
https://doi.org/10.3390/jcm11237001
14. Liu W, Ma JX, Tan X, Chai F, Liu J. A technique to treat Descemet's membrane detachment following cataract surgery. Front Med (Lausanne) 2024; 11: 1402853. Published 2024 Jun 11.
https://doi.org/10.3389/fmed.2024.1402853
15. Li YT, Wu WY, Li JY, Chan SY, Ang M, Feng Y. Types of Descemet Membrane Detachment After Ocular Surface Burns: The Factor Long Been Ignored. Cornea 2023; 42(11): 1426–1431.
https://doi.org/10.1097/ICO.0000000000003210
16. Li Z, Gao W, Yang Y, Liang W. Diagnosis and treatment of traumatic Descemet's membrane detachment: A case series. Medicine (Baltimore) 2023; 102(25): e34121.
https://doi.org/10.1097/MD.0000000000034121
17. Moramarco A, Iannetta D, Cimino L, Romano V, Gardini L, Fontana L. Case Report: “Spontaneous Descemet Membrane Detachment”. J Clin Med 2022; 12(1): 330. Published 2022 Dec 31.
https://doi.org/10.3390/jcm12010330
18. Ruggeri F, Rullo D, Maugliani E, et al. The role of anterior segment optical coherence tomography in post-cataract surgery Descemet membrane detachment. Int Ophthalmol 2025; 45(1): 74. Published 2025 Feb 18.
https://doi.org/10.1007/s10792-024-03397-y
19. Samarawickrama C, Beltz J, Chan E. Descemet's membrane detachments post cataract surgery: a management paradigm. Int J Ophthalmol 2016; 9(12): 1839–1842. Published 2016 Dec 18.
https://doi.org/10.18240/ijo.2016.12.23
20. Sharma N, Gupta S, Maharana P, Shanmugam P, Nagpal R, Vajpayee RB. Anterior Segment Optical Coherence Tomography-Guided Management Algorithm for Descemet Membrane Detachment After Intraocular Surgery. Cornea 2015; 34(9): 1170–1174.
https://doi.org/10.1097/ICO.0000000000000514
21. Singhal D, Sahay P, Goel S, Asif MI, Maharana PK, Sharma N. Descemet membrane detachment. SurvOphthalmol 2020; 65(3): 279–293.
https://doi.org/10.1016/j.survophthal.2019.12.006
22. Trindade LC, Attanasio de Rezende R, Bisol T, J Rapuano C. Late Descemet membrane detachment after uneventful cataract surgery. Am J Ophthalmol Case Rep 2022; 29: 101783. Published 2022 Dec 23.
https://doi.org/10.1016/j.ajoc.2022.101783
23. Turaga K, Kalary J, Velamala IP. Descemet's membrane detachment after Nd:YAG laser iridotomy in a patient with pseudoexfoliation. BMJ Case Rep 2022; 15(2): e246071. Published 2022 Feb 7.
https://doi.org/10.1136/bcr-2021-246071
