Sub-Tenon triamcinolone acetonide treatment in juvenile uveitis
doi: 10.55342/szemhungarica.2025.162.1.14
Original scientific paper
Summary
Introduction: Approximately 5% of the uveitis population is younger than 16 years old. The special challenges in the treatment of uveitis in children are a major concern today. They may be at special risk of complications because the inflammation is frequently chronic, and the diagnosis is often delayed because of the absence of noticeable signs and symptoms and the failure to report changes in vision in children. The systemic treatment with corticosteroids for non-infectious uveitis in childhood has an impact on the immature immune system and the developing bones. When a higher posterior effect is necessary, periocular corticosteroids can be administered.
We retrospectively studied the data of children with uveitis treated with sub-Tenon triamcinolone acetonide at the Department of Ophthalmology of Szeged.
Patients and methods: We treated 46 uveitic children at the Department of Ophthalmology between 2017 and 2021. There were 23 girls and 23 boys; the mean age at the time of the diagnosis of uveitis was eleven years. Their first ophthalmological examinations included visual acuity, intraocular pressure (IOP), exams with a slit lamp, optical coherence tomography and funduscopy.
Results: We studied the data of five patients treated with sub-Tenon triamcinolone acetonide. All of the patients had intermediate and posterior uveitis, and they received three injections 3 weeks apart. Their vision improved after the prompt treatment, and the cystoid macular oedema also had resolved. To enhance their status of minimal uveitic symptoms, they were started on methotrexate therapy.
Conclusions: Juvenile uveitis can cause several complications, and decrease visual acuity. Treating these children could be adventurous. The best route and dose are determined for each patient individually, but only the minimum amount needed to control inflammation should be used to reduce complications. The sub-Tenon approach works to deposit a long-lasting steroid around the eye, and the side effects are fewer than in systematic treatment.
Összefoglaló
Bevezetés: Az uveitises páciensek kb. 5%-a 16 évnél fiatalabb gyermek. Manapság nagy a kihívás az uveitises gyermekek kezelésében, a cél minél gyorsabban kezelni lehetőleg kevesebb mellékhatás nélkül. A gyerekek esetében nagyobb a szövődmény rizikója, hiszen gyakran a gyulladás krónikus, és a pontos diagnózis gyakran késik, mert a gyermekek nem panaszkodnak sem fájdalomra, sem látásromlásra. A kezelés alapja a kortikoszteroid, ami hatással van az éretlen immunrendszerre, és a növekvő csontokra. Intermedier és posterior érintettség esetén periocularis kortikoszteroid lehet a megoldás.
Célkitűzések: Retrospektíven elemezni a Szegedi Szemészeti Klinikán sub-tenon triamcinolonnal kezelt uveitises gyermekek adatait.
Módszerek: A Szegedi Szemészeti Klinikán negyvenhat uveitises gyermeket kezeltünk 2017–2021 között. A huszonhárom fiú és huszonhárom leány átlagéletkora a diagnóziskor 11 év volt. Látóélesség, szemnyomás, réslámpás, szemfenék és optikai coherens tomográfia vizsgálat történt.
Eredmények: Öt páciens részesült sub-tenon triamcinolon-acetonid injekciós kezelésben. Mindegyik gyermeknél intermedier és posterior uveitist diagnosztizáltunk, ezért mindegyikük 3 injekciót kapott 3 hetente. A kezelés hatására a látóélességük javult, a cisztoid makulaödéma megszűnt. A tünetmentesség fenntartása érdekében methotrexatterápiában is részesültek.
Megbeszélés: A gyermekkori uveitis súlyos szövődményekkel járhat, emiatt a látóélesség lecsökken. Nehéz ezen gyermekek kezelése, egyénileg kell meghatározni a megfelelő típusú és mennyiségű kezelést, hogy a gyulladást kontrollálni tudjuk.
Következtetés: Sub-tenon megközelítéssel hosszabb hatású és kevesebb mellékhatású kortikoszteroid effektust érhetünk el a szem körül.
Keywords
pediatric uveitis, sub-Tenon treatment, triamcinolone acetonide
Kulcsszavak
gyermekkori uveitis, sub-tenon injekció, triamcinolon-acetonid
Bevezetés
Az uveitis gyermekek esetében gyakran krónikus, elhúzódó lefolyású. A pontos diagnózis a tünetek hiányában késik, a gyerekek nem számolnak be látásromlásról, nem panaszkodnak, nehéz őket megvizsgálni és kezelni (1–3).
Gyermekkorban az uveitis incidenciája 4-6/100 000, míg felnőttkorban 26-102/100 000. A gyermekkori uveitis ritkább, de súlyosabb, az összes eset 2-8%-a (4). Az utóbbi években a panuveitisek száma nőtt, a hátsó uveitisek száma csökkent, valószínűleg azért, mert a toxoplasma és toxocara fertőzések gyakorisága a nyugati országokban kevesebb lett (3, 4). A diagnosztikai lehetőségek folyamatos fejlődése ellenére gyakran nem derül ki az uveitis kiváltó oka (3, 5).
Több tanulmány, mint pl. Kump és munkatársai foglalkoztak a gyermekkori uveitisek szövődményeivel (8). Leggyakoribb szövődménynek a szürkehályogot találták (52%), kevésbé gyakori az opacitas zonularis (35%), a szekunder glaukóma (33%), maculopathia (36%), és a látóideg-érintettség (36%) (6–9).
Az uveitisek kezelésének célja, hogy csökkentsék, illetve megelőzzék a látást fenyegető szövődmények kialakulását (1, 6, 7). Fontos a beteg panaszainak és a betegség tüneteinek mérséklése és az uveitist okozó alapbetegség gyógyítása. Gyermekkorban nehéz az uveitist kezelni, gyakoribbak a komplikációk, mint felnőttkorban. A kezelés ellenére nagy az amblyopia kialakulásának a veszélye. Az általánosan alkalmazott kortikoszteroidokat hosszabb ideig kell alkalmazni a megfelelő hatás elérésére, emiatt több a szövődmény. A csontrendszer fejlődésének gátlása által a növekedés elmaradását és a csontok gyakori törését okozhatják. Gyakran cushingoid megjelenés, peptikus fekély, myopathia, magas vérnyomás és pszichés zavar kísérheti a kezelést (10–12).
Regionálisan adott kortikoszteroidokat gyakran használnak nem infekciózus intermedier és posterior uveitisek esetén, ezen belül aktív gyulladás és cisztoid makulaödéma (CMO) kapcsán. A helyileg alkalmazott kortikoszteroid megemelheti a szemnyomást, nagyobb a rizikó a szürkehályog kialakulására és lokális irritációra (13–15). Periocularis triamcinolon-acetonid injekciót, 40 mg/ml-t a sub-tenon résen keresztül lehet a szembe juttatni, így a szem hátsó részén lehet stabil, hosszabb gyulladásgátló hatást elérni szemben a topikális kezeléssel, ezáltal a szisztémás hatást minimalizálva. Jelenleg a triamcinolon-acetonid sub-tenon alkalmazása off-label Magyarországon, viszont nemzetközi ajánlások jó hatású eredményekről számolnak be (13–15).
Célkitűzés
Tanulmányunkban klinikánk uveitis ambulanciáján megjelent, uveitissel diagnosztizált azon gyermekek adatait elemeztük, akik betegségük miatt sub-tenon triamcinolon-acetonid kezelésben részesültek. Kutatásunkhoz a Szegedi Tudományegyetem Etikai Bizottsága adott etikai engedélyt, engedélyszám: 5053.
Módszerek
Retrospektíven elemeztük a Szegedi Tudományegyetem Szemészeti Klinika uveitis ambulancián 2017. január 1. és 2021. december 31. között nem fertőzéses uveitis miatt kezelt gyermekek adatait. Ebben a periódusban 46 gyermeket diagnosztizáltunk nem infekciózus uveitissel, az átlagéletkoruk 11 év volt (1–18 év).
A diagnózis felállítása a fertőzések kizárását szolgáló szerológiai vizsgálatok (herpes simplex vírus 1-2, varicella zoster vírus, cytomegalovirus, Epstein–Barr-vírus, Toxocara, Toxoplasma, Borrelia burgdorferi, Treponema pallidum, hepatitis B, C), Quantiferron-teszt, gyermekreumatológiai (ANA, RF, HLA-B27 mintavétel, szisztémás autoimmun betegségek vizsgálata), gyermekkardiológiai (szív echográfia), gyermekneurológiai (demyelinizációs kórkép kizárása), gyermekpulmonológiai (mellkasröntgen: sarcoidosis, tbc kizárása), gyermeknefrológus (TINU kizárása) konzíliumok segítségével történt (16).
Közleményünkben azokat a nem fertőzéses eredetű eseteket dolgoztuk fel, ahol az uveitises gyermekek sub-tenon triamcinolonkezelésben részesültek. A szemészeti vizsgálatok során a gyermekeknél látóélesség, szemnyomás-, réslámpás-, szemfenék- és OCT-vizsgálat történt.
Eredmények
A vizsgált uveitises gyermekek közül öt páciens részesült intravénás narkózisban sub-tenon triamcinolon-acetonid injekciós kezelésben. A gyermekeknél intermedier és/vagy posterior uveitist diagnosztizáltunk, ezért átlagosan 3 injekciót kaptak 3 hét eltéréssel, minden alkalommal 40 mg/ml-t.
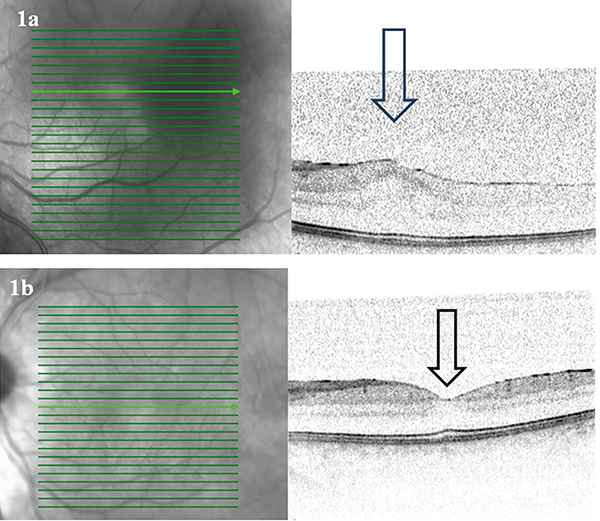
Az első páciens jobb szemén pars planitist, a bal szemén panuveitist és CMO-t diagnosztizáltunk. Kezdetben parabulbarisan részesült dexamethason injekcióban, majd, mivel tünetei nem szűntek meg, 32 mg metilprednizolon-kezelés indult szájon keresztül. A gyulladásos tünetek kiújulása után a jobb oldalon egyszer, a bal oldalon hatszor részesült sub-tenon triamcinolonkezelésben. Legjobb korrigált látóélessége jobb oldalon végig 1,0 volt, bal oldalon a kezelés előtti 0,1-ről a kezelés hatására 1,0 lett, a CMO megszűnt (1. a és 1. b ábra). A szisztémás kortikoszteroidkezelés leállt.
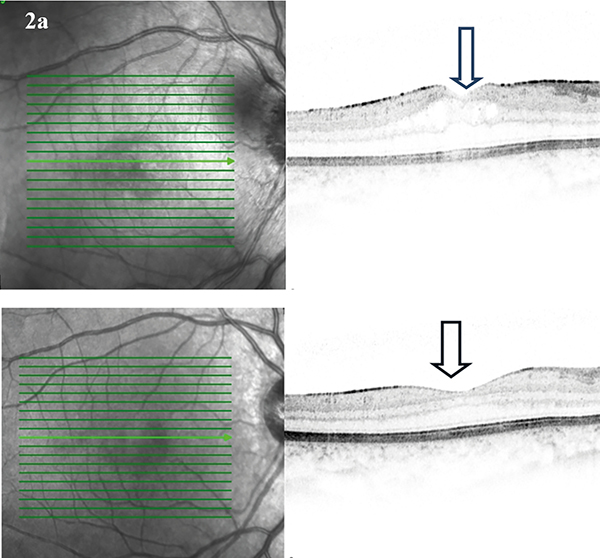
A második gyermek mindkét szemén pars planitis és CMO volt, emiatt 15 mg methotrexatkezelésben részesült. Sub-tenon triamcinolonkezelést egyszer kapott mindkét szemébe, ennek hatására jobb oldalon a legjobb korrigált látóélesség a kiindulási 0,5-ről 1,0 lett, bal oldalon pedig 0,4-ről szintén teljes lett, CMO megszűnt, (2. a és 2. b ábra). A methotrexatkezelés folyamatosan tartott.
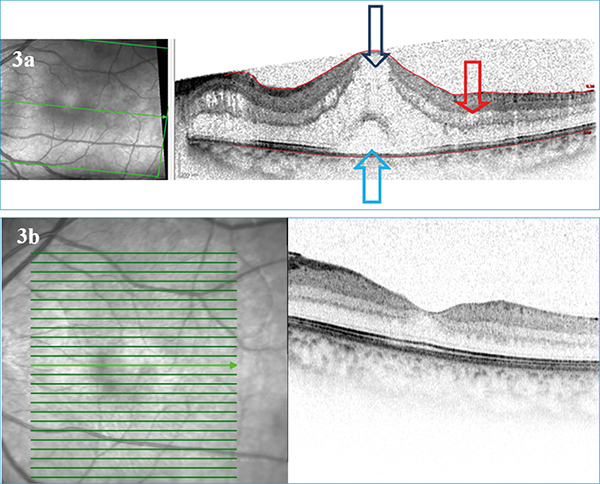
A harmadik páciens bal szemén panuveitist és CMO-t detektáltunk. Kezelése során ötször kapott dexamethason injekciót parabulbarisan, majd 16 mg/nap metilprednizolon és 20 mg methotrexat/hét terápiát indítottunk. A metilprednizolon dóziscsökkentés után leállt, methotrexatterápia végig tartott. A gyulladásos tünetei nem szűntek meg, ezért háromszor háromhetente sub-tenon triamcinolon injekciót kapott. A triamcinolonkezelés előtti 0,6 látóélessége 1,0 lett a terápia hatására, CMO megszűnt (3. a és 3. b ábra).
A negyedik gyermek bal szemén panuveitist diagnosztizáltunk. 32 mg metilprednizolon/nap terápiában részesült, amit lecsökkentve 17,5 mg methotrexát/hét váltotta fel. A továbbra is fennálló gyulladás miatt 3 hetente 3× részesült triamcinolonkezelésben. Látóélessége a kiinduló 0,06-ről 1,0 lett. Methotrexatterápiáját folyamatosan kapta.
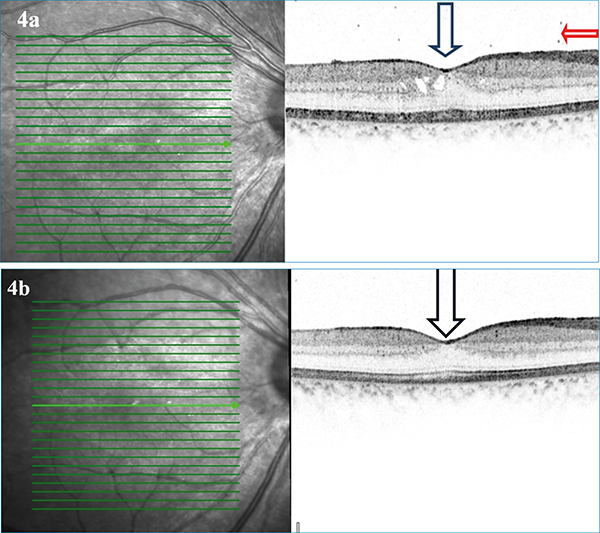
Az ötödik gyermek jobb szemén pars planitis és CMO miatt kezdődött kezelés. Parabulbarisan ötször kapott dexamethasonkezelést, a reumatológus a metilprenizolonját 4 mg/napban határozta meg, mellette 15 mg hetenkénti methotrexátban részesült. Sub-tenon triamcinolon injekciót egyszer kapott, ettől a látóélessége a kiindulási 0,01-ről 1,0 lett, CMO megszűnt (4. a és 4. b ábra).
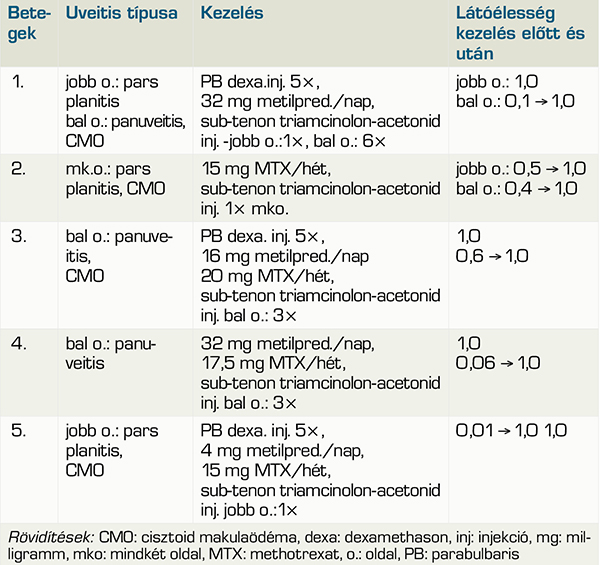
Az 1. táblázatban összefoglaltuk a gyernekeknél diagnosztizált uveitis típusát, oldaliságát, a triamcinolonterápia melletti kezelést és a legjobb korrigált látóélességet a kezelés előtt és után.
Megbeszélés
Nem infekciózus uveitisek esetén több lehetséges faktor közül az alapján határozzuk meg a terápiát, hogy mi áll rendelkezésre, mi a páciens számára a legbiztonságosabb, és a leghatásosabb (13, 14). A kezelési terv meghatározásában, főleg gyerekek esetén a gyermekreumatológussal is konzultálni kell, kevés protokoll áll rendelkezésünkre, ami segítené a különböző klinikai esetekben specifikus kezelés meghatározását. Vizsgálatunk célja volt, hogy többször használt lokális kortikoszteroid szemcseppek és szisztémás kortikoszteroid mellett más hatásos kezelési módot is találjunk, megismerjük az indikációs területeket és a gyakorlati hasznát.
Többféle regionális kortikoszteroid áll rendelkezésre manapság, mint az intravitrealisan és sub-tenon injekció formájában alkalmazható triamcinolon-acetonid és a biodegradabilis dexamethazon intravitrealis implantátum (17).
A „Systemic Immunosuppression Therapy for Eye Diseases (SITE) Cohort Study”-ban a periocularis kortikoszteroid injekciókat hatásosnak találták aktív intraocularis gyulladásban és makulaödémában és látásjavulást eredményeztek (18). Ezzel szemben a „Periocular vs. Intravitreal corticosteroids for uveal macular edema (POINT) study” szerint az intravitreálisan alkalmazott triamcinolon és dexamethazon-implantátum uveitises makulaödéma esetén hatásosabb a periocularis triamcinolonnál (15).
Egy másik tanulmányban a periocularis injekciókat, mint sub-tenon injekciót nagyon hatásosnak tartották az uveitis széles spektrumában, de a kezelés során kialakuló mellékhatásokról is beszámoltak, leginkább szürkehályog kialakulásáról. A periocularis injekciókat főleg aktív gyulladásban és a látásélességet rontó makulaödémában találták effektívnek. Mellékhatások ritkán fordultak elő, mint pl. okuláris hipertenzió, glaukóma vagy szürkehályog (19).
Mcharg és munkatársai összehasonlították a különböző regionális kortikoszteroidok hatását és a sub-tenon triamcinolont hatásosabbnak találták az intravitreális formánál. Ez utóbbi esetén nagyobb az esély a szemnyomás-emelkedésre (14). Jung és munkatársai gyermekekben vizsgálták a sub-tenon triamcinolon hatását lokális anesztézia mellett. Megállapították, hogy a triamcinolon a szemek 85,4%-ában csökkentette a gyulladásos tüneteket, 77-8%-ában pedig a makulaödéma megszűnését idézte elő 3 hónappal a kezelés után. Hat hónappal a vizsgálat után 12,5%-ban fordult elő okuláris hipertenzió, szürkehályog viszont egy esetben sem (13).
Tanulmányunk alapján a sub-tenon triamcinolon sub-tenon adagolása uveitises gyermekek esetén biztonságos és hatásos kezelésnek bizonyult. Az öt gyermek látása, akik intravénás altatásban sub-tenon injekciókban részesültek, a kezelés hatására javult, 1,0 lett. A kezdetben diagnosztizálható CMO a sub-tenon kezelés hatására elmúlt.
Következtetés
Gyermekkori uveitis több szövődménnyel jelentkezhet, ami következtében a látóélesség lecsökken. Ezt megelőzendő fontos a minél korábbi diagnózis, hogy a személyre szabott kezelést el tudjuk kezdeni. A gyermekek kezelését egyénre szabottan kell indukálni, és a gyulladás csökkentésére és a mellékhatások kivédésére a minimum dózist kell adni.
Sub-tenon kezeléssel a kortikoszteroid depozitként hosszabb ideig marad a szem körüli szövetekben és így a szisztémás mellékhatás is kevesebb. A gyulladást és a makulaödémát lecsökkenti, a látóélességet pedig javítja.
Nyilatkozat
A szerzők kijelentik, hogy eredeti közleményük megírásával kapcsolatban nem áll fenn velük szemben pénzügyi vagy egyéb lényeges összeütközés, összeférhetetlenségi ok, amely befolyásolhatja a közleményben bemutatott eredményeket, az abból levont következtetéseket vagy azok értelmezését.
Irodalom
1. Angeles-Han ST, Rabinovich CE. Uveitis in children. Curr Opin Rheumatol 2016; 28: 544–549.
https://doi.org/10.1097/BOR.0000000000000316
2. Cunningham ET, Smith JR, Tugal-Tutkum I, et al. Uveitis in children and adolescents. Ocul Immunol Inflamm 2000; 8: 251–261.
https://doi.org/10.1076/ocii.8.4.251.6459
3. Tugal-Tutkun I. Pediatric uveitis. J Ophthalmic Vis Res 2011; 6: 259–269. PMID: 22454749, PMCID: PMC3306124.
4. Zhao NO, Crowell EL. Epidemiology and Long-term Sequelae of Pediatric Uveitis. Int Ophthalmol Clin 2022; 62: 131–142.
https://doi.org/10.1097/IIO.0000000000000393
5. Sohár N. Pediatric uveitis (Gyermekkori uveitisek.) Szemészet 2017; 154: 191–198. (Hungarian)
6. Markomichelakis NN, Aissopou EK, Chatzistefanou KI. Pediatric non-infectious uveitis: Long-term outcomes and Complications. Ocul Immunol Inflamm 2023; 24: 1–8.
https://doi.org/10.1080/09273948.2022.2162422
7. Maccora I, Marra E, Pagnnini I, et al. Challenges and management of childhood noninfectious chronic uveitis. Expert Rev Clin Immunol 2023; 19: 599–611.
https://doi.org/10.1080/1744666X.2023.2198210
8. Kump LI, Cervantes-Castaneda R, Androudi SN. et al. Analysis of pediatric uveitis cases at a tertiary referral center. Ophthalmol 2005; 112: 1287–1292.
https://doi.org/10.1016/j.ophtha.2005.01.044
9. Sohár N, Skribek Á, Hammer H. Visual acuity in cases of juvenile uveitis. (Látásélesség alakulása gyermekkori uveitis esetében.) Szemészet 2011; 140: 73–76. (Hungarian)
10. Rosenberg KD, Feuer WJ, Davis JL. Ocular complications of pediatric uveitis. Ophthalmol 2004; 111: 2299–2306.
https://doi.org/10.1016/j.ophtha.2004.06.014
11. Friling R, Kramer M, Snir M, et al. Clinical course and outcome of uveitis in childhood. J AAPOS 2005; 9: 379–382.
https://doi.org/10.1016/j.jaapos.2005.04.005
12. Maleki A, Anesi SD, Look-Why S, et al. Pediatric uveitis: A comprehensive review. Surv Ophthalmol 2022; 67: 510–529.
https://doi.org/10.1016/j.survophthal.2021.06.006
13. Jung JL, Harasawa M, Patnaik JL, et al. Subtenon Triamcinolone Acetonide Injection with Topical Anesthesia in Pediatric Non-Infectious Uveitis. Ophthalmol Ther 2022; 11: 811–820.
https://doi.org/10.1007/s40123-022-00480-4
14. McHarg M, Young L, Kesav N, et al. Practice patterns regarding regional corticosteroid treatment in noninfectious uveitis: a survey study. J Ophthalmic Inflamm Infect 2022; 12: 3.
https://doi.org/10.1186/s12348-021-00281-z
15. Thorne JE, Sugar EA, Holbrook JT, et al. Periocular triamcinolone vs, intravitreal triamcinolon vs. intravitreal dexamethasone implant for the treatment of uveitis macular edema. Ophthalmol 2019; 126: 283-295.
https://doi.org/10.1016/j.ophtha.2018.08.021
16. Smeller L, Sümegi V, Tóth-Molnár E, et al. Biological therapy of uveitis in children (A biológiai terápia helye a gyermekkori uveitis ellátásában.) Orv Hetl 2022; 163(35): 1402–1408. (Hungarian).
https://doi.org/10.1556/650.2022.32578
17. Winterhalter S, et al. Dexamethasone implants in pediatric patients with noninfectious intermediate or posterior uveitis: first prospective exploratory case series. BMC Ophthalmology 2017; 17: 252.
https://doi.org/10.1186/s12886-017-0648-3
18. Yalcinsoy KO, Ozdal PC, Sen E, et al. Intraocular pressure elevation after posterior subtenon triamcinolone acetonide injection in pediatric non- infectious uveitis. Beyoglu Eye J 2022; 7: 298–303.
https://doi.org/10.14744/bej.2022.97752
19. Sen HN, Vitale S, Gangaputra SS, et al. Periocular corticosteroid injections in uveitis: effects and complications. Ophthalmol 2014; 121: 2275–2286.
https://doi.org/10.1016/j.ophtha.2014.05.021
