Our knowledge of the anterior vitreous membrane and the vitreolenticular interface
doi: 10.55342/szemhungarica.2025.162.1.2
Original scientific paper
Summary
The vitreous body makes up about 80% of the volume of the eye. It is a transparent gel-like substance, which consists mostly of water, collagen, and hyaluronic acid. We have a relatively extensive body of knowledge about the vitreous itself, but the anterior vitreous membrane and the vitreolenticular interface are less researched parts of the vitreous. In order to understand and see the role of this distinguished area in its context, it is worth reviewing the development, anatomy, and physiological significance of the vitreous body as a whole. All the changes occurring during the four overlapping stages of vitreous embryology also affect the final structure of the anterior vitreous. The Berger’s space represents the virtual space between the posterior surface of the lens and the anterior vitreous membrane. The hyalocapsular ligament (also known as Wieger's ligament) attaches the vitreous to the posterior lens capsule, forming a ring of 8-9 mm in diameter, 1 mm apart from the lens edge. Like the rest of the vitreous, the anterior vitreous is primarily important as an optical refractive medium, but there is increasing evidence that the vitreolenticular interface also plays a significant role in accommodation. There are specific congenital or acquired diseases of the anterior vitreous and the vitreolenticular interface. Phacoemulsification affects the state of the Berger’s space significantly; therefore, the use of gentle surgical techniques is important not only for endothelial protection and preservation of the zonula, but also for preserving the integrity of the vitreolenticular interface.
Összefoglaló
Az üvegtest a szem térfogatának mintegy 80%-át teszi ki. Átlátszó gélszerű anyag, amely legnagyobbrészt vízből, kollagénből és hialuronsavból áll. Magáról az üvegtestről relatíve bő ismeretanyag áll rendelkezésünkre, az elülső üvegtesti határhártya és a vitreolenticularis határfelszín viszont az üvegtest kevésbé kutatott része. Ahhoz, hogy megértsük, és összefüggéseiben lássuk ennek a kitüntetett területnek a szerepét, érdemes áttekinteni az üvegtest egészének fejlődéstanát, anatómiáját és fiziológiai jelentőségét. Az üvegtest embriológiájának négy, egymást átfedő fázisában bekövetkező valamennyi változás kihatással van az elülső üvegtest végső szerkezetének kialakulására is. A Berger-tér a lencse hátsó felszíne és az elülső üvegtesti határhártya közötti virtuális teret jelöli. A hyalo-capsularis szalag (más néven Wieger-szalag) rögzíti az üvegtestet a hátsó lencsetokhoz, a lencse peremétől 1 mm-re egy 8-9 mm átmérőjű gyűrűt alkotva. Akárcsak az üvegtest többi része, az elülső üvegtest is elsősorban, mint optikai törőközeg jelentős, ugyanakkor egyre több adat támasztja alá azt a feltételezést, hogy a vitreolenticularis határfelszínnek jelentős szerepe van az akkomodációban is. Az elülső üvegtestnek és a vitreolenticularis határfelszínnek speciális veleszületett és szerzett betegségei vannak. A phacoemulsificatio jelentősen befolyásolja a Berger-tér állapotát, ezért a kíméletes műtéttechnika alkalmazása nem csupán az endothelvédelem, és a zonula épségének megőrzése szempontjából fontos, hanem ennek révén megóvhatjuk a vitreolenticularis határfelszín integritását is.Keywords
vitreous, anterior vitreous membrane, Berger’s space, phacoemulsification
Kulcsszavak
üvegtest, elülső üvegtesti határhártya, Berger-tér, phacoemulsificatio
Bevezetés
Tanulmányunkban a szem legnagyobb térfogatú szövetét határoló képletről, az üvegtesti határhártyáról írunk, és annak is az eddig kevéssé vizsgált és kutatott részéről, az üvegtest elülső határhártyájáról, valamint az elülső határhártyával érintkező szövetekről. Az elülső üvegtesti határhártya az üvegtest elválaszthatatlan része, a lencse hátsó tokjával és a közöttük esetlegesen létrejövő térrel együtt az elülső határfelszínt/vitreolentikularis határfelszínt alkotja. Az elülső üvegtesti határhártya viselkedése hatással lehet mind az elülső, mind a hátsó üvegtestre, patológiája az üvegtest egészét érintheti és befolyással bírhat a vitreoretinalis határfelszínre is.
Jelen írásunkban ismertetjük az üvegtest fejlődéstanát, majd áttekintjük az üvegtest egészének, és ezen belül az elülső üvegtesti határfelszínnek az anatómiáját. Elemezzük az üvegtest molekuláris összetételét és anyagcseréjét, röviden tárgyaljuk az üvegtest fiziológiai szerepét, különös tekintettel az elülső üvegtesti határfelszínre. Bemutatjuk az vitreolenticularis határfelszín és az elülső üvegtest veleszületett patológiáit, valamint nem veleszületett betegségeit. Ismertetjük az elülső üvegtest vizsgálatára alkalmas diagnosztikus eszközöket, különös tekintettel az elülső szegmens optikai koherencia tomográfiára (AS-OCT). Végezetül elemezzük a phacoemulsificatio hatását a vitreolenticularis határfelszín integritására.
Az üvegtest fejlődéstana
Az üvegtest embriológiájának négy, egymást átfedő fázisában bekövetkező változásokat Sang foglalta össze, és írta le először (1). Az elsődleges üvegtestfázisban (primer vitreous stage) két fő folyamat zajlik: kialakul maga az elsődleges üvegtest, és kifejlődik az üvegtest érrendszere. A gesztáció 3-4. hetében a 4–5 mm-es embrióban a felszíni ektodermából lefűződő lencsehólyag, valamint a neuroektodermából kialakuló szemkehely által közre zárt, lassan növekvő belső teret tölti ki az elsődleges üvegtest. Ez kezdetben egy avaszkuláris, rostos hálózat, ún. „protoplazma híd” (1). Az 5. héten a szemkehely alsó részén elhelyezkedő embrionális szemhasadékon át vaszkularizált mesodermális sejtek nyomulnak be az elsődleges üvegtestbe és kialakul az üvegtest érhálózata, valamint a lencsehólyagot körülvevő erezett burok, a tunica vasculosa lentis. A gesztáció 6. hetében a 8–13 mm-es embrióban a lencsehólyag felszínén kifejlődik a lencsetok, ami innentől kezdve szeparálja a szemlencsét és az üvegtestet. Az üvegtest vaszkulatúrájának a gerincét az arteria hyaloidea adja, ami a primitív arteria ophthalmicaból ered és a tunica vasculosa lentisben végződik. A kapcsolat az elsődleges üvegtestbe benyomult vaszkularizált mezoderma és a szemhólyagot körülvevő mezoderma között – amiből a későbbiekben a chorioidea és a sclera alakul ki –, egészen 14 hétig, az embrionális szemhasadék záródásáig marad fenn (2).
A másodlagos üvegtestfázisnak (secondary vitreous stage) három fő mozzanata van, amelyek a következők:
- az acellularis másodlagos üvegtest kialakulása,
- a hyalocyta-fibroblast migráció, és
- a korai üvegtest-regresszió (1).
Az acellularis másodlagos üvegtest a 13–70 mm-es embrióban fejlődik ki, és teljes egészében a neuroektodermából származik. Az embrionális retina belső rétege és a vaszkularizált elsődleges üvegtest külső határa közötti teret tölti ki. Az acellularis másodlagos üvegtest a retina felszínével párhuzamos, finom, hullámos rostok sűrű soraiból épül fel, a hátsó póluson kezd el növekedni, majd később kiterjed a teljes elsődleges üvegtestre. Ebben a fázisban egy ideig demarkációs vonal, az ún. „intravitreális membrán” látható az elsődleges üvegtest és az újonnan képződött másodlagos üvegtest között (1). Elektronmikroszkóppal igazolták, hogy a másodlagos acellularis üvegtest rostjai a retina Müller-sejtjeinek talplemezeiből származnak, hasonlóan a retina legbelső rétegéhez, a membrana limitans internahoz (ILM) (3). A szemkehely elülső felében a másodlagos üvegtest rostjai összesűrűsödnek, és a szemkehely elülső határán kialakítják a Druaul-féle marginális köteget, amiből később az üvegtesti bázis fog kifejlődni. A vaszkularizált elsődleges üvegtestben két sejttípus lelhető fel: egy fibroblastszerű sejt az arteria hyaloidea tunica adventitiajában, valamint egy monocytatípusú sejt az elsődleges üvegtest gélállományában. Ez utóbbi a primitív csontvelőből a vérkeringés útján érkezik, majd átkerülve a másodlagos üvegtestbe a monocyta-makrofág rendszer részeként hyalocytává differenciálódik. A másodlagos üvegtestben a sejtmigrációt követően a sejtes elemek mintegy 10%-át teszik ki a fibroblastok és egy kevés gliasejt, még a sejtek 90%-át a hyalocyták alkotják. A fibroblastok termelik az üvegtestben előforduló strukturális fehérjék egy részét. A hyalocyták részben makrofágként működnek és fontos szerepet játszanak az üvegtest később említendő regressziójában, részben pedig nagy mennyiségű hialuronsavat termelnek (4). A hyalocyta-fibroblast migrációt követően a másodlagos üvegtest folyamatosan növekszik, egyre nagyobb teret foglal el az üvegtesti térben, és fokozatosan összenyomja a vaszkularizált elsődleges üvegtestet. Az elsődleges és másodlagos üvegtest határát képező intravitreális membrán előbb előrefelé kiszélesedő V-alakot ölt, majd a papillától a szemlencse hátsó pólusához húzódó, ereket tartalmaz köteggé kondenzálódik, és kialakul a Cloquet-csatorna. Ez a folyamat a 3. gesztációs hónapban a 45–60 mm-es embrióban kezdődik és a 200–240 mm-es embrióban ér véget (1). A szemlencse mögött az elsődleges és másodlagos üvegtest érintkezési felülete képezi a capsula perilenticularist, ami magába foglalja a Berger-teret, más néven a retrolentaris Eggelet-teret (5). A másodlagos üvegtestnek a hátsó lencsefelszínhez való kapcsolódási vonalát Egger-vonalnak nevezzük, amely később a Wieger-féle ligamentum hyaloideocapsularissá, röviden Wieger-szalaggá tömörül (6, 7).
A harmadlagos üvegtestfázisban (tertiary vitreous stage) kifejlődik a szemlencse függesztő rendszere, a zonula, és az üvegtesti vaszkulatúra további regressziója következik be (1). A 70 mm-es embrióban a szemkehely elülső határának neuroektodermája – ami megfelel a későbbi sugártest területének – harmadlagos üvegtesti rostokat kezd termelni (3). Ezek a rostok merőlegesen futnak a korábban említett Druaul-féle marginális köteg rostjaira, és a sugártest irányából a lencse ekvátorához futnak. A lencsefüggesztő rosthálózat tovább differenciálódik és kialakulnak a sugártestből kiinduló cilio-capsularis-, valamint a pars plicataból kiinduló orbiculo-capsularis rostok. A két fő rosthálózat közt létrejövő teret Hannover-csatornának, még a rostok és a másodlagos üvegtest közötti teret Petit-térnek nevezzük (8). A harmadlagos üvegtestfázisban komplettálódik az elsődleges üvegtest regressziója. Az elsődleges üvegtest vaszkulatúrájának endothelsejtjeiben glikogén és lipiddepozitumok képződnek, ami az endothel- és pericyta-sejtek pusztulásához vezet. Az erek tunica mediajában ezzel egy időben a simaizomsejtek fibroblastszerű sejtekké differenciálódnak, az erek lumene beszűkül, majd a maradék sejtmasszát hyalocyták fagocitálják. A Cloquet-csatornában elzáródott, csaknem teljesen átlátszó, ún. „szellemerek” maradnak vissza (9).
A késői fetális fázisban a 7. gesztációs hónappal kezdődően, a 240 mm-es magzatban az üvegtest érrendszere és a tunica vasculosa lentis elkezd teljesen visszafejlődni, az endothelsejtek és a pericyták elvesztésével az elsődleges üvegtest teljesen elsorvad (1). Az üvegtest hyalocytái és más, korábban az elsődleges, majd a másodlagos üvegtesthez kapcsolódó sejtek tovább vándorolnak az üvegtesti kéregbe. Az üvegtest össztérfogata tovább növekszik (10).
Fontos megemlíteni, hogy az emberi szem három nagy érrendszere – az üvegtest, a chorioidea, és a retina vaszkulatúrája –, összehangoltan fejlődik és biztosítja az adott struktúra tápanyag- és oxigénellátását. Az egyes vaszkulatúrák a magzati élet során egymást követően alakulnak ki, illetve regrediálnak részlegesen úgy, hogy kifejlődésük időintervalluma jelentősen átfed egymással. Míg az üvegtest érrendszere döntően a 3–22., a chorioidea érhálózata pedig a 6–26. magzati héten nyeri el végső formáját, addig a retina vaszkulatúrájának fejlődése a 12. gesztációs héten kezdődik és csak posztpartum fejeződik be (11).
Az üvegtest anatómiája
Az üvegtest két fő topográfiai területre oszlik: a központi részre, amelyet üvegtesti gélnek nevezünk, valamint a perifériás üvegtesti kéregállományra. Az üvegtestet az üvegtesti határhártya veszi körbe. A határhártya hátsó része a retinához és a corpus ciliarehoz tapad, még az elülső üvegtesti határhártya a lencsefüggesztő rostokkal és a szemlencse hátsó tokjával van kapcsolatban. A kortikális üvegtest elülső részét üvegtesti bázisnak nevezzük. A bazális üvegtestben a kollagén rostok különösen sűrűn állnak, és az üvegtest gyűrűszerű területet hozva létre szilárdan tapad az elülső retinához, valamint a corpus ciliare pars planajához. A pars plana és retina határát képező ora serratán túl előre körülbelül 2 mm-rel, hátrafelé pedig 3-4 mm-rel nyúlik túl ez a terület (12). Az üvegtesti bázis olyan erősen tapad a retinán, hogy szövetroncsolás nélkül nem lehet leválasztani, és nem véletlen, hogy ebben a régióban fordul elő a legtöbb nem észrevehető retinaszakadás (12). Az üvegtest a fibronektin és laminin adhéziós molekulákon keresztül tapad a retina felszínéhez, az ILM-hez. Ez a kapcsolat – az üvegtesti bázis mellett –, különösen erős a retina erei mentén, a papilla szélén, a makula területében és a hátsó lencsetokon. A kortikális üvegtestben sűrűn tömörült kollagénszálak vannak, amelyek a retina belső felületével nagyjából párhuzamos irányban futnak (12, 13). A hátsó üvegtest része a bursa praemacularis, amely az üvegtest és a makula kapcsolódását jelöli (14). Az üvegtest a papilla szélén tapadva tölcsér alakot vesz fel, amelyet a Cloquet-csatornának, a területet pedig Martegiani-területnek nevezzük (12, 14). 24–51 éves emberek szemét vizsgálva a bursa praemacularis felső határa nem volt kimutatható a vizsgált szemek túlnyomó többségénél, valamint azt találták, hogy a bursa praemacularis össze van olvadva a Martegiani-terület kiterjesztésével, azaz a Cloquet-csatornával, vagy más néven az Eisner-féle hyaloidalis traktussal (14). Az Eisner-féle hyaloidalis traktus S-alakú hullámvonalat leírva a hátsó lencsetokhoz fut, ahol az Erggelet-térben végződik (15). Jelen ismereteink szerint úgy tűnik, hogy az üvegtesti rosthálózat kölcsönösen összefüggő ciszternákat és csatornákat is tartalmaz, amelyek közül érdemes még megemlíteni a corpus ciliarét és a makulát összekötő ún. ciliobursalis csatornát (16).
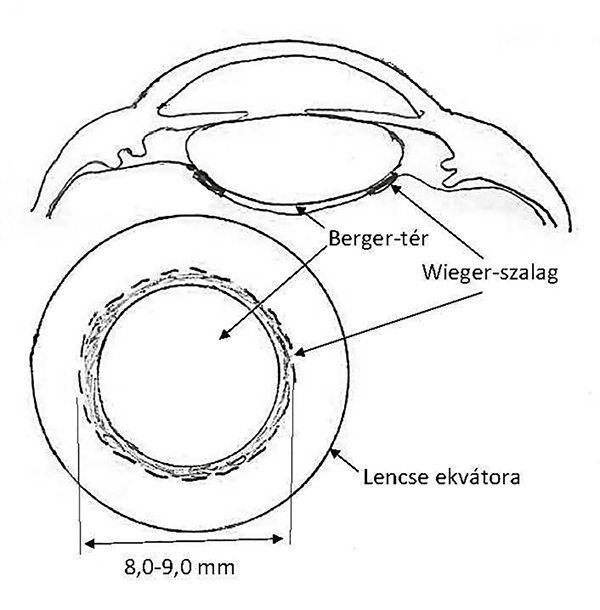
Az Emil Bergerről elnevezett Berger-tér a lencse hátsó felszíne és az elülső üvegtesti határhártya (AHM) közötti, definíció szerint ép Wieger-szalaggal határolt, sok esetben csupán virtuális teret jelöli. Wieger, Berger munkatársa azonosította a hyalo-capsularis szalagot (más néven Wieger-szalagot), amely a lencse peremétől 1 mm-re egy 8-9 mm átmérőjű gyűrűt alkot, és az üvegtestet a hátsó lencsetokhoz rögzíti (17) (1. ábra).
Az üvegtest molekuláris összetétele és anyagcseréje
Az üvegtest átlátszó gélszerű anyag, amely legnagyobbrészt vízből, kollagénből és hialuronsavból (HA) áll; a szem térfogatának mintegy 80%-át teszi ki, ami számszerűsítve kb. 4,0 ml (18). Fő szerkezeti fehérjéje a kollagén, amely a porchoz hasonló heterotípusú fibrillumokból áll (19–21). A II-es típusú kollagén az üvegtest teljes kollagéntartalmának 75%-át (18, 22), a IX-es típusú pedig 15%-át teszi ki (23). Az üvegtesti gél alapstruktúráját ezek a kollagén szálak alkotják, amelyeket főként hidratált HA-molekulák választanak el egymástól. A HA-molekulák töltőanyagként és barrierként működnek a szomszédos kollagén szálcsák között (12). A HA-at először 1937-ben izolálták szarvasmarha üvegtestből. A HA születés után jelenik meg az üvegtestben, feltételezhetően a hyalocyták, a corpus ciliare és/vagy a Müller-sejtek szintetizálják (20). A HA egy hidrofil glikoprotein, ami más glikoprotein tömbökkel, és kondroitin-szulfáttal komplexet alkotva kitölti a kollagén fibrillumok által képzett „állvány” közeit, biztosítja a szerkezet stabilitását, és ilyen módon döntő szerepet játszik az üvegtest molekuláris morfológiájának fenntartásában (24–26). A HA vonzza az ún. counter ionokat, amelyek megkötve a vizet hozzájárulnak a távolságok fenntartásához, az üvegtest háromdimenziós szerkezetének stabilizálásához, valamint befolyásolják a gyógyszerek üvegtesti diffúzióját is (27, 28). Az üvegtestben ugyancsak feltalálható XVIII-as típusú kollagén pedig bizonyítottan az endosztatin progenitora, ami viszont az angiogenezis erős inhibitora (18, 29, 30).
Az üvegtest embrionális fejlődése során jól definiálható biokémiai transzport-folyamatok is nyomon követhetők. Az ILM, a neuroretina bazálmembránja többek között fehérje makromolekulákból épül fel. Bizonyítást nyert, hogy az ILM-et alkotó legfontosabb fehérjék – a laminin és a IV-es típusú kollagén –, az agrin kivételével nem a retinából, hanem a szemlencséből és a sugártestből származnak. Ezek a nélkülözhetetlen fehérje makromolekulák a másodlagos üvegtest közvetítésével jutnak el a retinához az embrionális korban (31). Az üvegtest strukturális proteinjei, a II-es típusú kollagén és a fibrillin szintén a sugártestből származnak (32). A laminin, valamint a II-es és IV-es típusú kollagén szintézise nagyon aktív az embrionális korban, majd fokozatosan csaknem nullára csökken a második postnatalis évre. Az ILM-nek és az üvegtestnek ezzel a nagyon alacsony felnőttkori anyagcseréjével magyarázható, hogy pars plana vitrectomia után, valamint ILM peelinget követően gyakorlatilag nincs regeneráció (33, 34).
Az üvegtest fiziológiai szerepe
Az üvegtest szerepe a szem normálműködésében sokrétű, és mind a mai napig nem teljesen tisztázott. Vannak természetesen általánosan elfogadott, vitathatatlan tények, mint például az üvegtest optikai törőközeg funkciója. Kevésbé köztudott, de szintén általánosan elfogadott az üvegtest oxigénmegkötő, barrier szerepe. Az oxigén a chorioidea és a retina keringéséből származik, és diffúzió révén jut az üvegtestbe. Az oxigén nagy részét a hyalocyták elfogyasztják, és ezáltal korlátozzák a bradytroph anyagcseréjű szemlencsét, és az elülső szegmens más részeit elérő oxigén mennyiségét. Az üvegtest magas aszkorbátszintje is ezzel függhet össze, ez is védi az elülső szegmens szöveteit az oxidatív károsodástól, ami a szemlencse esetében a cataractogenesis gátlását jelenti (18).
Az üvegtestben is megtalálható a XVIII-as típusú kollagén progenitora az endosztatinnak. Immunhisztokémiai vizsgálatokkal kimutatták, hogy a lencsetokon, az ILM-en, és a corpus ciliare nonpigmentált epitheliumán endosztatin expresszálódik, ami erős inhibitora a neovaszkularizációnak. A szemlencse és az üvegtest körül tehát „gátat” képező, specifikusan endosztatint expresszáló struktúrák gyűrűje van. Tekinthetjük úgy is, hogy az üvegtest XVIII-as típusú kollagéntartalma révén fiziológiásan megakadályozza, hogy az erek bejussanak ezekbe az avaszkuláris szövetekbe (18, 29, 30).
Az egymással kölcsönösen összefüggő üvegtesti ciszternáknak és csatornáknak az egyik szerepe feltételezhetően az, hogy csökkentik a szemmozgások során az üvegtestnek a makulához viszonyított tehetetlenségi mozgása által keltett vonóerőket. Különösen igaz ez a bursa praemacularisra (12). A közvetlen antero-posterior kapcsolat a retrolentális, valamint a praemacularis és praeopticus terek között ugyanakkor számos betegség patogenezisében szerepet játszhat.
Egyre több adat támasztja alá azt a feltételezést, hogy a vitreolenticularis határfelszínnek jelentős szerepe van az akkomodációban is. Intraoperatív AS-OCT-felvételekre alapozva Tassignon és munkatársai bebizonyították, hogy a Berger-tér egy valódi anatómiai tér, és feltételezhetően e térnek valódi anatómiai célja is van. Ők vetették fel először, hogy ez a Wieger-szalag által határolt 8-9 mm átmérőjű folyadékrés synoviaként működik, és elősegíti a szemlencse alakváltozását. A hátsó tok mögött elhelyezkedő folyadékgyülem ugyanis sokkal kisebb ellenállást fejt ki a lencse alakváltozásával szemben, mint a relatíve szilárdabb üvegtesti gél (35). Számítógépes modellezéssel kimutatták, hogy a Wieger-szalag részt vehet a szemlencse hátsó görbületének alakításában, ami részét képezheti az akkomodációnak (36). Sikerült modellezni a csarnokvíz és az üvegtest áramlását az akkomodációs ciklus alatt. Kiderült, hogy a chorioidea rugalmas megnyúlása és összehúzódása olyan hidrodinamikai kölcsönhatásokat idéz elő, amelyek az üvegtest közvetítésével tevődnek át a szemlencsére. A modell alátámasztja azt az elképzelést is, hogy a presbyopia nem csupán a lencse megmerevedéséből, hanem az extralenticularis struktúrák rugalmasságának elvesztéséből, és a szem rigiditásának általános növekedéséből ered (37). A vireolenticularis határfelszín másik kompartmentjéről, a hátsó lencsetokról kiderült, hogy a mechanikai szilárdságának korral összefüggő csökkenése korábban elkezdődik, mint az elülső lencsetoké. Akkomodációs funkciótartományban, azaz alacsony terhelés mellett a hátsó lencsetok mechanikai hatékonysága a tok vastagságától függött, azzal egyenes arányos volt (38).
A vitreolenticularis határfelszín és az elülső üvegtest veleszületett patológiái
A vitreolenticularis határfelszín és az elülső üvegtest veleszületett patológiás elváltozásai legnagyobbrészt az üvegtest és a szemlencse embrionális korban meglévő vaszkulatúrájának elégtelen visszafejlődésére vezethetők vissza (39). Egy 2001-ben készült amerikai felmérés szerint ez a betegségcsoport tehető felelőssé a gyermekkori vakság 5%-áért (40). Az arteria hyaloidea persistens, a primer hiperplasztikus perzisztáló üvegtest (PHPV), valamint a cataracta congenita egyes formái; a Mittendorf-pont, a lenticonus posterior, és a cataracta polaris posterior (CPP) tartoznak ebbe a betegségcsoportba.
A normális magzati fejlődés során az arteria hyaloidea a 18. héten kezd el visszafejlődni, és a 29. hétre a csaknem láthatatlan Cloquet-csatornává alakul át (41). Ennek elmaradása esetén az arteria hyaloidea lumene részben vagy egészben nyitva marad, és összeköti a papillát a szemlencse hátsó pólusával. A papilláris kapcsolódási pontot Bergmeister-papillának, a lencsével való érintkezést Mittendorf-pontnak, magát az állapotot pedig arteria hyaloidea persistensnek nevezzük (42). Az arteria hyaloidea persistens lehet tünetmentes, de okozhat kataraktát, ismétlődő üvegtesti vérzést, és retinaleválást is (43).
A PHPV a fetális perzisztáló üvegtesti vaszkulatúra legsúlyosabb formája, amelynek kardinális tüneteit Goldberg foglalta össze először 1997-ben. A kórkép jellemző tünetei: membrana pupillaris persistens, irido-hyaloidalis erek és tunica vasculosa lentis maradványok jelenléte, Mittendorf-pont, katarakta, arteria hyaloidea persistens, Bergmeister-papilla, abnormális makula, hypoplasia és dysplasia nervi optici, valamint a bulbus méretbeli és alaki malformációja. Ez a fejlődési rendellenesség ismétlődő súlyos üvegtesti vérzéssel, és nem ritkán retinaleválással is jár (44). Mai tudásunk szerint az üvegtesti vaszkulatúra visszafejlődése normálisan egy kétlépcsős folyamat, amelynek valamelyik szakasza zavart szenved, és erre vezethető vissza a PHPV kialakulása. Az első fázisban az apoptózist fokozott makrofágaktivitás indítja el, amit a második fázis endothelsejt pusztulása követ. Ez utóbbit az arteria ophthalmicából származó vérbeáramlás csökkenése és/vagy a lencse által termelt vaszkuláris endotheliális növekedési faktor csökkent termelődése idézi elő (45, 46).
A Mittendorf-pont egy lassan, vagy nem progrediáló veleszületett szürkehályog-forma, ami megfelel az arteria hyaloidea elülső kapcsolódási pontja maradványának a hátsó lencsetok centrumában, vagy annak nasalis-alsó paracentrális területén (47). Az esetek egy részében mellette arteria hyaloidea persistens is látható. A Mittendorf-pont rendszerint kevéssé rontja a látást, és csak ritkán igényel műtéti megoldást (48).
A lenticonus posterior a szemlencse veleszületett kónikus vagy szférikus, gyakran aszimmetrikus hátrafelé való kiboltosulása, ami rendszerint lencsehomállyal is jár (49). Az esetek egy részében egyértelműen igazolható a fetális vaszkulatúra perzisztálása, mint kóroki tényező (50). Előfordul sporadikusan, de az esetek többségében X-hez kötött vagy autoszóm domináns öröklésmenetet mutat (51). Megoldása speciális műtéti technikát igényel, hátsó capsulorhexis, elülső vitrectomia, vagy a pars plana felől lensectomia elvégzése javasolt, a műlencsét pedig rendszerint a sulcus ciliarisba lehet csak implantálni (52).
A cataracta congenita egyik alcsoportjának, a CPP-nek korrekt sebészi ellátása régi problémája a szemészetnek. A CPP háromdimenziós kiterjedésű, a lencse hátsó pólusán lévő vaskos plakk beterjed az üvegtesti térbe is, rajta nem ritkán arteria hyaloidea persistens tapad, és lehet a PHPV egyik részjelensége is (48). Levágott hagymakarikára emlékeztető vaskos plakk formája elkülöníti a cataracta corticalis posteriortól, ami műtéttechnikailag nem jelent különösebb kihívást. A CPP a cataracta congenita miatt gyermekkorban műtétre kerülő esetek 7%-át teszi ki (53). A CPP másik csoportja nem okoz kataraktaműtétet indokló látásromlást gyermekkorban, hanem lassú progressziót követően, jellemzően a 3-5. évtizedben kerül műtétre a beteg (54). A betegség rendszerint autoszóm domináns öröklésmenetű, de előfordulnak sporadikus esetek is (55). A CPP műtétje során figyelembe kell venni, hogy hátsó pólusi plakk területében hiányzik, vagy nagyon gyenge a hátsó tok, ezért a legtöbb operatőr hidrodisszekció végzése helyett hidrodelaminációt javasol, valamint igyekszik minden lehetséges módon minimalizálni a lencsetokra ható stresszt a műtét során (56).
A vitreolenticularis határfelszín és az elülső üvegtest szerzett patológiái
A vitreolenticularis határfelszín és az elülső üvegtest szerzett patológiáinak legnagyobb részét azok az állapotok teszik ki, amelyek a Berger-térbe (BS) került, ott felhalmozódott, vagy lerakódott anyagokkal jellemezhetők. A BS, amint azt korábban említettük, a lencse hátsó felszíne és az AHM közötti virtuális teret jelöli. Ismereteink gyarapodásával nyilvánvalóvá vált, hogy a BS jelenléte vagy hiánya egyre nagyobb klinikai jelentőséggel bír. Az idevonatkozó szakirodalom tanulsága szerint különböző anyagok halmozódhatnak fel a BS-ben. Proliferatív diabéteszes retinopathia egyes eseteiben (57), vagy tompa trauma után (58, 59) vér volt kimutatható a BS-ben. Little mutatta ki először, hogy komplikációmentes phacoemulsificatio során a lencsetöredékek utat találhatnak a BS-be (60). He és munkatársai egy olyan esetről számoltak be, amikor ablatio retinae miatt végzett pars plana vitrectomia és szilikonolaj-feltöltést követően az üvegtesti szilikonolaj-tamponádtól elkülönülten a BS-ben is egy szilikonolaj-csepp volt kimutatható (61). Mares és munkatársai 7 retinoblastoma miatt enucleált szemet vizsgálva tumorsejteket nem, viszont amiloid anyagot és piknotikus sejteket tudtak kimutatni a BS-ben (62). Salman és munkatársai egy olyan esetet publikáltak, ahol intravitrealis injekciót követően triamcinolon-acetát rekedt meg a szemlencse mögött hirtelen, átmeneti látásvesztést okozva (63). Dubrelle és munkatársai intravitreálisan injektált dexametazon-implantátum BS-ben való megrekedéséről számoltak be. Az implantátum az 1 hónappal később elvégzett sima lefolyású phacoemulsificatio során mozdult csak ki a BS-ből, és szűnt meg a beteg „úszkáló homály” látása (64). Grzybowski és Kanclerz feltételezése szerint a fluid misdirection szindróma egyik formája, a phacoemulsificatio során tapasztalt szemnyomás-növekedés valószínű oka a műtét közben a BS-ben akkumulálódó öblítő folyadék (65). Japán szerzők egy 68 éves férfinél a BS-ben idiopathiás opacifikációt találtak. Az átlátszatlan folyadékot műtéti úton eltávolították, a vegyelemzés magas fehérje- és alacsony mukopoliszacharid-koncentrációt mutatott ki mindenféle mögöttes patológia nélkül (66). Intraoperatív OCT (iOCT) segítségével az elülső interface dysgenesisén alapuló, új típusú veleszületett szürkehályogot tudtak leírni, amelyet AVLID-nek neveztek el: anterior vitreo-lenticular interface dysgenesis. Ez a fajta veleszületett szürkehályog a fejlett országokban az újszülött szürkehályog körülbelül egyharmadáért felelős.
Az elülső üvegtest vizsgálata
Az üvegtest szerkezeti felépítése – aminek átlátszóságát köszönheti –, az üvegtestet egy relatíve nehezen vizualizálható és vizsgálható struktúrává teszi a szemben. Míg azonban az üvegtest centrális és hátsó része, hátsó pólusi retinához való viszonya in vivo könnyen és meglehetősen jól vizsgálható B-scan ultrahanggal (67–72), valamint optikai koherencia tomográfiával (OCT) (67, 69–74), addig az elülső üvegtest vizsgálata más megközelítést igényel.
Az előző fejezetben említett idiopathiás opacifikációt a BS-ben réslámpás vizsgálattal írták le (66). A klasszikus réslámpás vizsgálat ugyanakkor rendkívül korlátozott. Jellemzően akkor látható a Berger-tér, ha valamilyen „idegen” anyag legalább részben kitölti. Saját tapasztalataink szerint saját lencsés szemen tiszta BS réslámpával való megjelenítése még jó teljesítményű réslámpával is szinte lehetetlen. Műlencsés állapotban bár az elülső határhártya „közelebb” van a corneához, az elülső üvegtesti határhártya rendkívül finom képlet, ábrázolását a műlencse és a hátsó tok közötti retrolentáris tér, esetleges tokredők, illetve a határhártya által lezárt mozgó üvegtesti szálcsák nagyon zavarhatják, így könnyen félreérthető a látott kép. Ultrahang biomikroszkópia segítségével az elülső üvegtest relatíve jól vizsgálható műlencsés szemen, hátránya viszont ennek a vizsgálati metódusnak az ultrahang limitált felbontó képessége, valamint a vizsgálat kontakt jellege, ami korlátozza alkalmazhatóságát a perioperatív szakban (75, 76). A mágneses rezonancia képalkotás (MRI) vizsgálatot 1984-ben említették először, mint az üvegtest különféle elváltozásainak kvalitatív és kvantitatív vizsgálatát lehetővé tevő eljárást (77). Az üvegtest – beleértve az elülső üvegtestet is –, rutinszerű vizsgálata MRI-vel azonban sem a tudományos vizsgálatoknál, sem a napi betegellátásban nem vált rutinná az eljárás korlátozott információtartalma, valamint drágasága miatt.
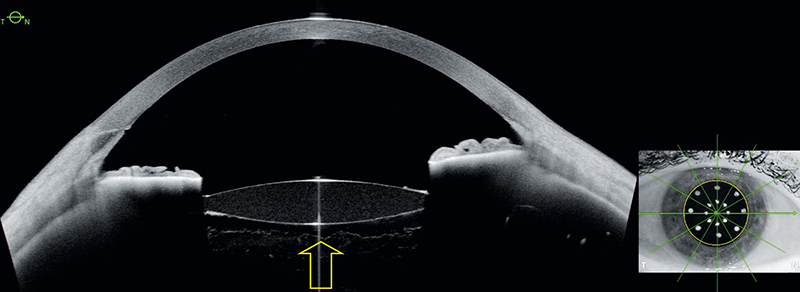
Az elülső üvegtest vizsgálatában az igazi áttörést az OCT-technológia fejlődése hozta el. 2016-ban Tassignon és Dhubhghaill vizualizálta először valós idejű iOCT-vel a BS-t phacoemulsificatio során (78). Mares és munkatársai 2020-ban két pseudophakiás szemen AS-OCT-vel tudta megjeleníteni a BS-t (62). 2021-ben Ruminski és munkatársai alkalmazott először swept-source AS-OCT (SS-AS-OCT) technológiát az elülső üvegtest volumetrikus vizsgálatára. Megállapították, hogy az elülső üvegtest átlátszatlansága, hasonlóan a szemlencse és a hátsó üvegtest homályaihoz fokozott fényszórással és a kontrasztérzékenység csökkenésével jár (79). Lin és munkatársai 2022-ben réslámpás biomikroszkópiával és AS-OCT-vel vizsgálták a phacoemulsificatio hatását a BS-re a műtét előtt, és 1 hónappal a műtét után (80), Zhang és munkatársai pedig SS-AS-OCT-t használtak ugyanilyen céllal (81). Saját vizsgálatainkban az Anterion SS-AS-OCT-t (Heidelberg Engineering, Heidelberg, Németország) használtunk az AHM, illetve a BS megjelenítésére a preoperatív, és a korai és késői posztoperatív szakban (82, 83) (2. ábra).
A phacoemulsificatio hatása a vitreolenticularis határfelszín integritására
Köztudott, hogy a phacoemulsificatio nem csupán a lencse állapotát változtatja meg alapjaiban, hanem a műtét az egész szem integritását érinti. Phacoemulsificatio során a szem legtöbbet vizsgált része a szaruhártya-endothelium és a szaruhártya görbülete. Előbbi a nagy áramlási sebesség és az ultrahang-energia, valamint a viszkoelasztikus anyag elégtelen használata miatt jelentősen károsodhat (84, 85), míg az utóbbit elsősorban a seb mérete, elhelyezkedése, a limbushoz való viszonya, illetve a műtét során elszenvedett mechanikai hatások befolyásolhatják (86, 87). 1975 óta számos publikáció számolt be arról, hogy a hátsó üvegtesti határhártya leválása (PVD) sokkal gyakrabban fordul elő szürkehályog-műtét után (88–90), és a retinaleválás esélye többszörösére nő a phacoemulsificatiót követően, különösen a nagyfokú rövidlátó szemeknél (89–91). A vitreolenticularis határfelszín, valamint az AHM viselkedését phacoemulsificatio során, illetve után csak nemrégiben kezdték tanulmányozni. Tassignon és Dhubhghaill 2016-ban valós idejű iOCT-t használva először számoltak be intraoperatíve észlelt elülső üvegtesti határhártya-leválásról (AVD) phacoemulsificatio során 1 szemen (78). Anisimova és munkatársai 2020-ban 28 szemet vizsgálva iOCT-vel 75, még posztoperatív AS-OCT-vel 82%-ban tudta ábrázolni a BS-t. Ugyancsak Anisimova és munkatársai tudtak detektálni először OCT-vel szemlencse-mikrofragmentumokat a BS-ben, amit iOCT-vel az esetek 57, még posztoperatív AS-OCT-vel 32%-ban lehetett kimutatni (92). Vael és munkatársai 2022-ben 99 szemet szövődménymentes phacoemulsificatio során iOCT-vel vizsgálva az esetek 63%-ban talált AVD-t. A műtét során észlelt AVD gyakorisága nem mutatott összefüggést a nemmel és a szem tengelyhosszával, ugyanakkor szignifikánsan gyakoribb volt idősebb életkorban (93). A legutóbbi időkben is több publikáció látott napvilágot, ahol spectral domain AS-OCT-t, vagy SS-AS-OCT-t használtak a hátsó tok és AHM lehetséges változásainak megjelenítésére, és világossá vált, hogy a phacoemulsificatio jelentősen befolyásolja a BS állapotát (80–83, 92, 94–96). A phacoemulsifikációt követően a BS gyakran megnagyobbodik a műtét után, vagy a preoperatívan rögzített AHM bizonyos esetekben leválik a hátsó tokról, azaz AVD következik be (78, 80–84, 92–96). Bebizonyosodott, hogy a beteg magasabb életkora (82, 83, 93, 95), a lencse anyagok jelenléte a BS-ben (LM-BS) (78, 80, 92, 94), a zonuláris rostok gyengesége (80), cornea nagyobb törőereje (95) predesztinál AVD-re. A szem tengelyhosszának szerepe ugyanakkor kérdéses (81, 82, 93, 95). Adatok állnak rendelkezésre a phacoemulsificatio sebészeti paramétereiről, miszerint a teljes műtéti idő, az összes leadott ultrahang-energia (CDE), az ultrahangos idő, az átlagos longitudinális teljesítmény, a teljes aspirációs idő, a folyadékfelhasználás, az infúziós nyomás, az aspirációs áramlási sebesség, a palack magassága és a vákuum, befolyásolják a BS kialakulását (80, 81, 94, 96, 97).
Saját vizsgálataink során 1 éven át dokumentáltuk az AHM tapadását vagy leválását eseménytelen phacoemulsificatio után, és elemeztük egyes intraoperatív műtéti paraméterek hatását a változásokra (82, 83). Sikerült beigazolni, hogy AVD tekintetében szignifikáns lineáris trend volt megfigyelhető a zonula gyengeség és a magas CDE kapcsán minden kontrollkor (p<0,024 és p<0,005). Hasonlóan, az 1 hónapos, 3 hónapos és 1 éves kontrollon a nagyfokú magkeménység (p<0,044) és magas folyadékfogyasztás (p<0,021) esetén szignifikáns összefüggés mutatkozott az AVD-vel. Az LM-BS-csoportjában szignifikáns korreláció mutatkozott a zonulagyengeség fokozódásával (OR=0,085; 95% CI: 0,017–0,420; p=0,002), és a nagyobb mennyiségű folyadék felhasználásával (OR=1,049; 95%). CI: 1,003–1,096; p=0,037). A fenti adatokból egyértelműen következik, hogy a zonulagyengeség, a magas CDE, a kemény mag és a nagymértékű folyadékfogyasztás kockázati tényezői a posztoperatív AVD-nek (83). Vizsgálataink arra is rámutattak, hogy preoperatíve levált AHM mellett a BS átlagos mélysége minden mérési ponton, valamennyi kontroll alkalmával szignifikánsan nagyobb volt posztoperatíve, mint a műtét után kialakult AVD esetén (82).
Megfigyeléseink alapján arra a következtetésre jutottunk, hogy a Berger-tér és az elülső üvegtesti határhártya-leválás fogalmak nem felcserélhetők. A Berger-tér elnevezést javasolt megtartani szigorúan az eredeti definícióban megfogalmazott esetre: azaz ép Wieger-szalag által körkörösen határolt centrális térre. Minden más esetben, amikor a határhártya részlegesen vagy teljesen eltávolodott a hátsó toktól, az elülső üvegtesti határhártya leválás, anterior vitreous detchment, AVD elnevezés használata javasolt (82, 83).
Következtetések
Az emberi üvegtest egy rendkívül összetett struktúra, amelynek pontos funkcióját csak a fejlődéstan és az anatómiai viszonyok alapos tanulmányozásával érthetjük meg. Mára világossá vált, hogy az üvegtest nem csupán egy átlátszó optikai közeg, hanem fontos oxigénmegkötő, barrier szerepe is van, amelynek révén fiziológiásan megakadályozza, hogy az erek bejussanak a szem avaszkuláris szöveteibe. Ugyancsak érdemes tudni, hogy közvetlen antero-posterior kapcsolat áll fenn a retrolentális, valamint a praemacularis és praeopticus terek között, ami számos betegség patogenezisében szerepet játszhat. Az elülső üvegtest ezentúl részt vesz az akkomodáció folyamatában is. Az elülső üvegtest legjobban SS-AS- OCT-vel vizsgálható. A phacoemulsificatio jelentősen befolyásolja a BS állapotát, ezért a kíméletes műtéttechnika alkalmazása nem csupán az endothelvédelem, és a zonula épségének megőrzése szempontjából fontos, hanem ennek révén megóvhatjuk a vitreolenticularis határfelszín integritását is.
Nyilatkozat
A szerzők kijelentik, hogy összefoglaló eredeti közleményük megírásával kapcsolatban nem áll fenn velük szemben pénzügyi vagy egyéb lényeges összeütközés, összeférhetetlenségi ok, amely befolyásolhatja a közleményben bemutatott eredményeket, az abból levont következtetéseket vagy azok értelmezését.
Irodalom
1. Sang DN. Embryology of the vitreous. Congenital and developmental abnormalities. Bull Soc Belge Ophthalmol 1987; 223 Pt 1: 11–35.
https://doi.org/10.1007/978-1-4757-1901-7_2
2. Zypen E van der, Fankhauser F. Ultrastructure of the hyaloid canal and its retraction during gestation. Klin Monbl Augenheilkd 1982; 180: 329–332. (German) https://doi.org/10.1055/s-2008-1055078
3. Balazs EA. Fine structure of the developing vitreous. Int Ophthalmol Clin 1975; 15: 53–63. https://doi: 10.1097/00004397-197501510-00006
4. Balazs EA, Toth LZ, Eckl EA, Mitchell AP. Studies on the structure of the vitreous body. XII. Cytological and histochemical studies on the cortical tissue layer. Exp Eye Res 1964; 3: 57–71.
https://doi.org/10.1016/s0014-4835(64)80008-7
5. Duke-Elder S, Cook C. Normal and abnormal development. In: Duke-Elder S. (ed.), Systems in ophthalmology. Vol. III, part 1: Embryology. St. Louis: C. V. Mosby; 1963. p. 141–154.
6. Albrecht M, Eisner G. The hyalo-capsular zonula. Graefes Arch Clin Exp Ophthalmol 1982; 218: 88–92. https://doi.org/10.1007/BF02153717
7. Rosen E. Zonulo-hyaloidea ligament. Ann Ophthalmol 1970; 2: 857–862.
8. Rohen JW, Rentsch FJ. Architecture and function of the human zonula ciliaris. Morphological principles for a new theory of accommodation. Albrecht Von Graefes Arch Klin Exp Ophthalmol 1969; 178: 1–19. German
https://doi.org/10.1007/BF00428041
9. Ko MK, Chi JG, Chang BL. Hyaloid vascular pattern in the human fetus. J Pediatr Ophthalmol Strabismus 1985; 22: 188–193.
https://doi: 10.3928/0191-3913-19850901-07
10. Balazs EA, Toth LZ, Ozanics V. Cytological studies on the developing vitreous as related to the hyaloid vessel system. Albrecht Von Graefes Arch Klin Exp Ophthalmol 1980; 213: 71–85. https://doi.org/10.1007/BF00413534
11. Lutty GA, McLeod DS. Development of the hyaloid, choroidal and retinal vasculatures in the fetal human eye. Prog Retin Eye Res 2018; 62: 58–76.
https://doi.org/10.1016/j.preteyeres.2017.10.001
12. McCannel CA. Basic and Clinical Science Course. Vol. 12. San Francisco, CA: American Academy of Ophthalmology; 2019–2020. American Academy of Ophthalmology: Basic and Clinical Science Course; pp. 307–308.
13. Gal-Or O, Ghadiali Q, Dolz-Marco R, Engelbert M. In vivo imaging of the fibrillar architecture of the posterior vitreous and its relationship to the premacular bursa, Cloquet's canal, prevascular vitreous fissures, and cisterns. Graefes Arch Clin Exp Ophthalmol 2019; 257 :709–714.
https://doi.org/10.1007/s00417-018-04221-x
14. Schaal KB, Pang CE, Pozzoni MC, Engelbert M. The premacular bursa's shape revealed in vivo by swept-source optical coherence tomography. Ophthalmology 2014; 121: 1020–1028.
https://doi.org/10.1016/j.ophtha.2013.11.030
15. Eisner G. Zur Anatomie des Glaskörpers [Gross anatomy of the vitreous body (author's transl)]. Albrecht Von Graefes Arch Klin Exp Ophthalmol 1975; 193: 33–56. German.
https://doi.org/10.1007/BF00410525
16. Polak BC, Ringens PJ, Worst JG. Physiological vitreous changes may contribute to the pathogenesis of macular degeneration. Acta Ophthalmol 2012; 90: e652–653.
https://doi.org/10.1111/j.1755-3768.2012.02539.x
17. Wieger G. Inaugural Dissertation. Université de Strasbourg; Strasbourg, France: 1883. Über den Canalis Petiti und ein ‘Ligamentum Hyaloideocapsulare’.
18. Kirchhof B, SriniVas S, Schachat A, Wilkinson C, Hinton D, Wiedemann P, Freund KB, Sarraf D.(eds): Ryan's Retina, 3 Volume Set 7th Edition, Elsevier, 2022 (eBook ISBN: 9780323722148; Hardcover ISBN: 9780323722131). Graefes Arch Clin Exp Ophthalmol 2023; 261: 599.
https://doi.org/10.1007/s00417-022-05874-5
19. Eyre DR, Apon S, Wu JJ, Ericsson LH, Walsh KA. Collagen type IX: evidence for covalent linkages to type II collagen in cartilage. FEBS Lett 1987 Aug 17; 220: 337–341.
https://doi.org/10.1016/0014-5793(87)80842-6
20. Balazs EA. Hyaluronan as an ophthalmic viscoelastic device. Curr Pharm Biotechnol 2008; 9: 236–8.
https://doi.org/10.2174/138920108785161596
21. Szirmai JA, Balazs EA. Studies on the structure of the vitreous body. III. Cells in the cortical layer. AMA Arch Ophthalmol 1958; 59: 34–48.
https://doi.org/10.1001/archopht.1958.00940020058006
22. Schmut O, Mallinger R, Paschke E. Studies on a distinct fraction of bovine vitreous body collagen. Graefes Arch Clin Exp Ophthalmol 1984; 221: 286–9.
https://doi.org/10.1007/BF02134125
23. Bishop PN, Crossman MV, McLeod D, Ayad S. Extraction and characterization of the tissue forms of collagen types II and IX from bovine vitreous. Biochem J 1994; 299: 497–505.
https://doi.org/10.1042/bj2990497
24. Cain SA, Morgan A, Sherratt MJ, Ball SG, Shuttleworth CA, Kielty CM. Proteomic analysis of fibrillin-rich microfibrils. Proteomics 2006; 6: 111–122.
https://doi.org/10.1002/pmic.200401340
25. Hubmacher D, Reinhardt DP, Plesec T, Schenke-Layland K, Apte SS. Human eye development is characterized by coordinated expression of fibrillin isoforms. Invest Ophthalmol Vis Sci 2014; 55: 7934–7944.
https://doi.org/10.1167/iovs.14-15453
26. Ramos MF, Atta M, Stern ME, Brassard JA, Kim AS, Matsumoto S, Vangyi C. Safety Evaluation of Ocular Drugs. In: Ramos MF (ed.): A Comprehensive Guide to Toxicology and Precilinical Drug Development. 2nd ed., Academic Press, Elsevier 2017; 757–811.
https://doi.org/10.1016/B978-0-12-387815-1.00024-1
27. Kim H, Robinson SB, Csaky KG. Investigating the movement of intravitreal human serum albumin nanoparticles in the vitreous and retina. Pharm Res 2009; 26: 329–37.
https://doi.org/10.1007/s11095-008-9745-6
28. Comper WD, Laurent TC. Physiological function of connective tissue polysaccharides. Physiol Rev 1978; 58: 255–315.
https://doi.org/10.1152/physrev.1978.58.1.255
29. Bhutto IA, Kim SY, McLeod DS, Merges C, Fukai N, Olsen BR, Lutty GA. Localization of collagen XVIII and the endostatin portion of collagen XVIII in aged human control eyes and eyes with age-related macular degeneration. Invest Ophthalmol Vis Sci 2004; 45: 1544–52.
https://doi.org/10.1167/iovs.03-0862
30. Ohlmann AV, Ohlmann A, Welge-Lüssen U, May CA. Localization of collagen XVIII and endostatin in the human eye. Curr Eye Res 2005; 30: 27–34.
https://doi.org/10.1080/02713680490894333
31. Halfter W, Dong S, Dong A, Eller AW, Nischt R. Origin and turnover of ECM proteins from the inner limiting membrane and vitreous body. Eye (Lond) 2008; 22: 1207–1213. https://doi.org/10.1038/eye.2008.19
32. Halfter W, Winzen U, Bishop PN, Eller A. Regulation of eye size by the retinal basement membrane and vitreous body. Invest Ophthalmol Vis Sci 2006; 47: 3586–3594. https://doi.org/10.1167/iovs.05–1480
33. Ihanamäki T, Pelliniemi LJ, Vuorio E. Collagens and collagen-related matrix components in the human and mouse eye. Prog Retin Eye Res 2004; 23: 403–434.
https://doi.org/10.1016/j.preteyeres.2004.04.002
34. Halfter W, Dong S, Schurer B, Ring C, Cole GJ, Eller A. Embryonic synthesis of the inner limiting membrane and vitreous body. Invest Ophthalmol Vis Sci 2005; 46: 2202–2209.
https://doi.org/10.1167/iovs.04-1419
35. Tassignon MJ, Ní Dhubhghaill S. Real-Time Intraoperative Optical Coherence Tomography Imaging Confirms Older Concepts About the Berger Space. Ophthalmic Res 2016; 56: 222–226.
https://doi.org/10.1159/000446242
36. Goldberg DB. Computer-animated model of accommodation and theory of reciprocal zonular action. Clin Ophthalmol 2011; 5: 1559–1566.
https://doi.org/10.2147/OPTH.S25983
37. Goldberg DB. Computer-animated model of accommodation and presbyopia. J Cataract Refract Surg 2015; 41: 437–445.
https://doi.org/10.1016/j.jcrs.2014.07.028
38. Krag S, Andreassen TT. Mechanical properties of the human posterior lens capsule. Invest Ophthalmol Vis Sci 2003; 44: 691–696.
https://doi.org/10.1167/iovs.02-0096
39. Saint-Geniez M, D'Amore PA. Development and pathology of the hyaloid, choroidal and retinal vasculature. Int J Dev Biol 2004; 48: 1045–1058.
https://doi.org/10.1387/ijdb.041895ms
40. Khaliq S, Hameed A, Ismail M, Anwar K, Leroy B, Payne AM, Bhattacharya SS, Mehdi SQ. Locus for autosomal recessive nonsyndromic persistent hyperplastic primary vitreous. Invest Ophthalmol Vis Sci 2001; 42: 2225–2228.
41. Achiron R, Kreiser D, Achiron A. Axial growth of the fetal eye and evaluation of the hyaloid artery: in utero ultrasonographic study. Prenat Diagn 2000; 20: 894–9.
https://doi.org/10097-0223(200011)20:113.0.co;2-j
42. Jones HE. HYALOID REMNANTS IN THE EYES OF PREMATURE BABIES. Br J Ophthalmol. 1963 Jan;47(1):39–44.
https://doi.org/10.1136/bjo.47.1.39
43. Chen C, Xiao H, Ding X. Persistent Fetal Vasculature. Asia Pac J Ophthalmol (Phila) 2019; 8: 86–95.
https://doi.org/10.22608/APO.201854
44. Goldberg MF. Persistent fetal vasculature (PFV): an integrated interpretation of signs and symptoms associated with persistent hyperplastic primary vitreous (PHPV). LIV Edward Jackson Memorial Lecture. Am J Ophthalmol 1997; 124: 587–626.
https://doi.org/10.1016/s0002-9394(14)70899-2
45. Meeson A, Palmer M, Calfon M, Lang R. A relationship between apoptosis and flow during programmed capillary regression is revealed by vital analysis. Development 1996; 122: 3929–3938.
https://doi.org/10.1242/dev.122.12.3929
46. Meeson AP, Argilla M, Ko K, Witte L, Lang RA. VEGF deprivation-induced apoptosis is a component of programmed capillary regression. Development 1999; 126: 1407–1415.
https://doi.org/ 10.1242/dev.126.7.1407
47. Stocklin P. Normvarianten der Morphologie der kindlichen Linse [Normal variations of morphology of crystalline lens in children]. Albrecht Von Graefes Arch Ophthalmol 1957; 158: 346–359. German.
48. Amaya L, Taylor D, Russell-Eggitt I, Nischal KK, Lengyel D. The morphology and natural history of childhood cataracts. Surv Ophthalmol 2003; 48: 125–144. https://doi.org/10.1016/s0039-6257(02)00462-9
49. Gibbs ML, Jacobs M, Wilkie AO, Taylor D. Posterior lenticonus: clinical patterns and genetics. J Pediatr Ophthalmol Strabismus 1993; 30: 171–175. https://doi.org/10.3928/0191-3913-19930501-10
50. Khokhar S, Dhull C, Mahalingam K, Agarwal P. Posterior lenticonus with persistent fetal vasculature. Indian J Ophthalmol 2018; 66: 1335–1336. https://doi.org/10.4103/ijo.IJO_276_18
51. Vivian AJ, Lloyd C, Russell-Eggitt I, Taylor D. Familial posterior lenticonus. Eye (Lond) 1995; 9 (Pt 1): 119–123.
https://doi.org/10.1038/eye.1995.19
52. Simons BD, Flynn HW Jr. A pars plana approach for cataract surgery in posterior lenticonus. Am J Ophthalmol 1997; 124: 695–696.
https://doi.org/10.1016/s0002-9394(14)70913-4
53. Mistr SK, Trivedi RH, Wilson ME. Preoperative considerations and outcomes of primary intraocular lens implantation in children with posterior polar and posterior lentiglobus cataract. J AAPOS 2008; 12: 58–61.
https://doi.org/10.1016/j.jaapos.2007.08.003
54. Vasavada A, Singh R. Phacoemulsification in eyes with posterior polar cataract. J Cataract Refract Surg 1999; 25: 238–245.
https://doi.org/10.1016/s0886-3350(99)80133-3
55. Yamada K, Tomita HA, Kanazawa S, Mera A, Amemiya T, Niikawa N. Genetically distinct autosomal dominant posterior polar cataract in a four-generation Japanese family. Am J Ophthalmol 2000; 129: 159–165.
https://doi.org/10.1016/s0002-9394(99)00313-x
56. Gurnani B, Kaur K. Posterior polar cataract. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 Jan.2023 Jun 11
57. Tolentino FI, Lee PF, Schepens CL. Biomicroscopic study of vitreous cavity in diabetic retinopathy. Arch Ophthalmol 1966; 75: 238–246.
https://doi.org/10.1001/archopht.1966.00970050240018
58. Naumann GO. Photographs of intralenticular hemorrhage following blunt ocular trauma. Arch Ophthalmol 1999; 117: 549.
https://doi.org/10.1001/archopht.117.4.549
59. Li ST, Yiu EP, Wong AH, Yeung JC, Yu LW. Management of traumatic haemorrhage in the Berger's space of a 4-year-old child. Int Ophthalmol 2017; 37: 1053–1055. https://doi.org/10.1007/s10792-016-0337-x
60. Little B. Bits in Berger’s space. Video J Cataract Refract Surg 2003; 19.
61. He S, Lin Z, Qiu Q. A patient with a Berger's space filled by silicone oil. BMC Ophthalmol 2023; 23: 307.
https://doi.org/10.1186/s12886-023-03035-8
62. Mares V, Nehemy MB, Salomão DR, Goddard S, Tesmer J, Pulido JS. Multimodal Imaging and Histopathological Evaluation of Berger's Space. Ocul Oncol Pathol 2020; 6: 3–9.
https://doi.org/ 10.1159/000495724
63. Salman A, Parmar P, Coimbatore VG, Meenakshisunderam R, Christdas NJ. Entrapment of intravitreal triamcinolone behind the crystalline lens. Indian J Ophthalmol 2009; 57: 324–325.
https://doi.org/10.4103/0301-4738.53066
64. Dubrulle P, Fajnkuchen F, Qu L, Giocanti-Aurégan A. Dexamethasone implant confined in Berger's space. Springerplus 2016; 13(5): 1786.
https://doi.org/10.1186/s40064-016-3490-9
65. Grzybowski A, Kanclerz P. Acute and chronic fluid misdirection syndrome: pathophysiology and treatment. Graefes Arch Clin Exp Ophthalmol 2018; 256: 135–154.
https://doi.org/10.1007/s00417-017-3837-0
66. Tanaka H, Ohara K, Shiwa T, Minami M. Idiopathic opacification of Berger's space. J Cataract Refract Surg 2004; 30: 2232–2234.
https://doi.org/10.1016/j.jcrs.2004.05.014
67. Sebag J. Imaging vitreous. Eye (Lond) 2002; 16: 429–439.
https://doi.org/10.1038/sj.eye.6700201
68. Mamou J, Wa CA, Yee KM, Silverman RH, Ketterling JA, Sadun AA, Sebag J. Ultrasound-based quantification of vitreous floaters correlates with contrast sensitivity and quality of life. Invest Ophthalmol Vis Sci 2015; 56: 1611–1617. https://doi.org/10.1167/iovs.14-15414
69. Sebag J. Seeing the invisible: the challenge of imaging vitreous. J Biomed Opt 2004; 9: 38–46.
https://doi.org/10.1117/1.1627339
70. Restori M. Imaging the vitreous: optical coherence tomography and ultrasound imaging. Eye (Lond) 2008; 22: 1251–1256.
https://doi.org/10.1038/eye.2008.30
71. Resch M, Balogh A. Proliferatív vitreoretinopathia. Szemészet 159; 2: 51–63.
https://doi.org/10.55342/SZEMHUNGARICA.2022.159.2.51
72. Németh J, Csákány B. A hátsó segmentum vizsgálata. In: Németh J (ed.): Szemészeti diagnosztikus képalkotó eljárások. 1th ed. Budapest: Semmelweis Kiadó; 2011. p. 162–170.
73. Balogh A, Milibák T, Szabó V, Nagy ZZ, Resch MD. Position of macula lutea and presence of proliferative vitreoretinopathy affect vitreous cytokine expression in rhegmatogenous retinal detachment. PLOS One 2020; 15: e0234525. https://doi.org/10.1371/journal.pone.0234525
74. Somfai GM. Optikai koherencia tomográfia a macula vizsgálatában. In: Németh J (ed.): Szemészeti diagnosztikus képalkotó eljárások. 1th ed. Budapest: Semmelweis Kiadó; 2011. p. 111–126.
75. Csákány B, Németh J. Az elülső segmentum vizsgálata, ultrahang-biomikroszkópia (UBM). In: Németh J (ed.): Szemészeti diagnosztikus képalkotó eljárások. 1th ed. Budapest: Semmelweis Kiadó; 2011. p. 156–160.
76. Pierro L, Azzolini C, Codenotti M, Locatelli C, Tremolada G, Brancato R. Ultrasound biomicroscopy of residual vitreous base after vitreoretinal surgery. Ophthalmologica 2002; 216: 13–15.
https://doi.org/10.1159/000048290
77. González RG, Cheng HM, Barnett P, Aguayo J, Glaser B, Rosen B, Burt CT, Brady T. Nuclear magnetic resonance imaging of the vitreous body. Science 1984; 223: 399–400.
https://doi.org/10.1126/science.6318321
78. Tassignon MJ, Ní Dhubhghaill S. Real-Time Intraoperative Optical Coherence Tomography Imaging Confirms Older Concepts About the Berger Space. Ophthalmic Res 2016; 56: 222–226.
https://doi.org/10.1159/000446242
79. Ruminski D, Sebag J, Toledo RD, Jiménez-Villar A, Nowak JK, Manzanera S, Artal P, Grulkowski I. Volumetric Optical Imaging and Quantitative Analysis of Age-Related Changes in Anterior Human Vitreous. Invest Ophthalmol Vis Sci 2021; 62: 31. https://doi.org/10.1167/iovs.62.4.31
80. Lin WL, Geng WJ, Ji M, Li PF, Luo JW, Guan HJ. [Effect of phacoemulsification on the Berger space]. Zhonghua Yan Ke Za Zhi. 2022; 58: 506–512. Chinese.
https://doi.org/10.3760/cma.j.cn112142-20220113-00013
81. Zhang Z, Yao J, Chang S, Kanclerz P, Khoramnia R, Deng M, Wang X. Incidence and Risk Factors for Berger's Space Development after Uneventful Cataract Surgery: Evidence from Swept-Source Optical Coherence Tomography. J Clin Med 2022; 11: 3580. https://doi: 10.3390/jcm11133580
82. Elekes Á, Németh G, Lauter D, Edelmayer M, Rupnik Z, Vámosi P. Examination of the Vitreolenticular Interface in Relation to Uneventful Phacoemulsification over One-Year Postoperative Period. J Clin Med 2024; 13: 3219. https://doi.org/10.3390/jcm13113219
83. Elekes Á, Vámosi P. Examination of Vitreolenticular Interface in Relation to Different Phacoemulsification Parameters in Early and Late Postoperative Period. J Clin Med 2024; 13: 4855.
https://doi.org/10.3390/jcm13164855
84. Binder PS, Sternberg H, Wickman MG, Worthen DM. Corneal endothelial damage associated with phacoemulsification. Am J Ophthalmol 1976; 82: 48–54.
https://doi.org/10.1016/0002-9394(76)90663-2
85. Mayali H, Baser EF, Kurt E, Ilker SS. Corneal endothelial damage in phacoemulsification using an anterior chamber maintainer compared with using an ophthalmic viscosurgical device. J Cataract Refract Surg 2021; 47: 612–617. https://doi.org/10.1097/j.jcrs.0000000000000493
86. Gupta SN, Goel R, Kumar S. Factors affecting surgically induced astigmatism in manual small-incision cataract surgery. Indian J Ophthalmol 2022; 70: 3779–3784.
https://doi.org/10.4103/ijo.IJO_1034_22
87. Langenbucher A, Szentmáry N, Cayless A, Casaza M, Weisensee J, Hoffmann P, Wendelstein J. Surgically Induced Astigmatism after Cataract Surgery – A Vector Analysis. Curr Eye Res 2022; 47: 1279–1287.
https://doi.org/10.1080/02713683.2022.2052108
88. Friedman Z, Neumann E. Posterior vitreous detachment after cataract extraction in non-myopic eyes and the resulting retinal lesions. Br J Ophthalmol 1975; 59: 451–454.
https://doi.org/10.1136/bjo.59.8.451
89. Hayashi S, Yoshida M, Hayashi K, Tsubota K. Progression of posterior vitreous detachment after cataract surgery. Eye (Lond) 2022; 36: 1872–1877.
https://doi.org/10.1038/s41433-021-01732-6
90. Qureshi MH, Steel DHW. Retinal detachment following cataract phacoemulsification-a review of the literature. Eye (Lond) 2020; 34: 616–631.
https://doi.org/10.1038/s41433-019-0575-z
91. Neuhann IM, Neuhann TF, Heimann H, Schmickler S, Gerl RH, Foerster MH. Retinal detachment after phacoemulsification in high myopia: analysis of 2356 cases. J Cataract Refract Surg 2008; 34: 1644–1657.
https://doi.org/10.1016/j.jcrs.2008.06.022
92. Anisimova NS, Arbisser LB, Shilova NF, Melnik MA, Belodedova AV, Knyazer B, Malyugin BE. Anterior vitreous detachment: risk factor for intraoperative complications during phacoemulsification. J Cataract Refract Surg 2020; 46: 55–62.
https://doi.org/10.1016/j.jcrs.2019.08.005
93. Vael A, Van Os L, Melis K, Tassignon MJ. Evaluation of the vitreolenticular interface with intraoperative OCT. J Cataract Refract Surg 2022; 48: 826–830.
https://doi.org/10.1097/j.jcrs.0000000000000866
94. Lin W, Luo J, Li P, Ji M, Guan H. Anterior vitreous detachment and retrolental material during cataract surgery: incidence and risk factors, with pathological evidence. J Cataract Refract Surg 2023; 49: 578–583.
https://doi.org/10.1097/j.jcrs.0000000000001156
95. Mori H, Ueno Y, Fukuda S, Oshika T. Detection of Anterior Hyaloid Membrane Detachment Using Deep-Range Anterior Segment Optical Coherence Tomography. J Clin Med 2022; 11: 3057.
https://doi.org/10.3390/jcm11113057
96. Scarfone HA, Rodriguez EC, Rufiner MG, Riera JJ, Fanego SE, Charles M, Albano R. Vitreous-lens interface changes after cataract surgery using active fluidics and active sentry with high and low infusion pressure settings. J Cataract Refract Surg 2024; 50: 333–338.
https://doi.org/10.1097/j.jcrs.0000000000001359
97. Vasavada V, Srivastava S, Vasavada V, Vasavada S, Vasavada AR, Sudhalkar A, Bilgic A. Impact of fluidic parameters during phacoemulsification on the anterior vitreous face behavior: Experimental study. Indian J Ophthalmol 2019; 67: 1634–1637.
https://doi.org/10.4103/ijo.IJO_465_19
