Our experiences and results with selective laser trabeculoplasty
doi: 10.55342/szemhungarica.2024.161.2.81
Original scientific paper
Summary
Aim: Selective laser trabeculoplasty is a proven, effective laser treatment for glaucoma. In addition to the initial recommendations, more and more clinical experience is being gathered in other indications. Methods: As a result of several mechanisms, the selective laser increases the permeability of the trabecular meshwork, thus reducing the intraocular pressure. The method is efficient and repeatable, as it does not cause permanent damage to the other parts of the trabecular network. Based on published and personally researched data, the laser is efficient in approximately 60-75% of the treated patients, and an approximately 20-25% decrease in intraocular pressure can be achieved by its application. Results: Since May 2016, we have performed 834 selective laser trabeculoplasty on 433 glaucoma patients at the Ophthalmology Department of the University of Pécs. In 72% of our patients, we achieved an effective 20% decrease in intraocular pressure. In 67% of the patients, the purpose of the laser treatment was complementary to the existing therapy, due to disease progression. Treatment change due to eyedrop intolerance or side effects was the indication in 15% of patients. In certain cases, we can use selective laser trabeculoplasty safely and effectively to reach patients eyedrop-free. Conclusion: Following the results of the LiGHT (Laser in Glaucoma and Ocular Hypertension) study, selective laser trabeculoplasty has taken its rightful place among antiglaucoma treatments. As a complementary treatment, its effectiveness is a 26% decrease in intraocular pressure. We consider selective laser treatment to be suitable as a replacement for monotherapy, because the intraocular pressure did not rise even after stopping the eye drops for the treated patients. Selective laser use is a cost-effective and reliable method as of primary and even independent therapy and can provide a good quality of life as an alternative to eyedrop treatments. Based on the treatment results so far, our aim is to have selective laser trabeculoplasty be used in as a high proportion as possible in the future, and to have it move forward from the “last chance” category.
Összefoglaló
Célkitűzés: A szelektív lézer trabekuloplasztika bizonyítottan hatékony lézerkezelés a glaukóma terápiájában. A kezdeti ajánlások mellett egyre több indikációban gyűlnek tapasztalatok. Módszer: A szelektív lézer többféle mechanizmus eredményeképpen a trabekuláris hálózat átjárhatóságát növeli, ezáltal csökkentve a szemnyomást. A módszer hatékony és ismételhető, mivel nem okoz maradandó károsodást a trabekuláris hálózat többi részében. Irodalmi és saját adatok alapján a lézer a kezelt betegek kb. 60-75%-ánál hatékony és kb. 20-25%-os szemnyomáscsökkenés érhető el vele. Eredmények: A Pécsi Szemészeti Klinikán 2016 májusa és 2023. szept 1. között 834 szelektív lézer trabekuloplasztikát végeztünk 433 glaukómás betegen. A betegeink 72%-ánál elértük a terápiás hatékonyságot jelentő 20%-os szemnyomáscsökkenést. A betegek 67%-ánál a lézerkezelés célja a meglévő terápia kiegészítése volt látótérprogresszió miatt. A szemcsepp-intolerancia vagy mellékhatás miatti terápiaváltás a betegek 15%-ánál volt a kezelés indikációja. A szelektív lézerkezelést bizonyos esetekben biztonsággal és hatékonyan tudjuk alkalmazni cseppmentesség elérése érdekében is. Következtetések: A LiGHT (Laser in Glaucoma and Ocular Hypertension) eredményei óta a szelektív lézer trabekuloplasztika elfoglalta méltó helyét a glaukómaellenes kezelések között. Kiegészítő kezelésként alkalmazva hatékonysága 26%-os szemnyomáscsökkenést eredményezhet. Monoterápia elhagyására vagy a cseppmentesség elérése érdekében is választható kezelési alternatívának tartjuk a szelektív lézerkezelést, mert a szemcsepp elhagyása után sem emelkedett meg a szemnyomás értéke a vizsgált betegpopulációban. A szelektív lézer költséghatékony és megbízható módszer elsődleges és akár önálló terápiaként is, és jó életminőséget biztosíthat a szemcseppes kezelések alternatívájaként. Az eddigi kezelési eredmények alapján a célunk, hogy a szelektív lézer trabekuloplasztika minél szélesebb körben kerüljön alkalmazásra, és az „utolsó esély” kategóriából a korai kezelési körbe kerüljön azon páciensek esetében, akik alkalmasak a kezelésre.Keywords
selective laser trabeculoplasty, SLT, melanin, laser
Kulcsszavak
szelektív lézer trabekuloplasztika, SLT, melanin, lézer
Bevezetés
A glaukómás betegek kezelésének alapja a szemnyomás csökkentése, amelyet elérhetünk lokálisan alkalmazott szemcseppekkel, lézertechnikákkal és műtétekkel.
1995 óta használt a szelektív lézer trabekuloplasztika (SLT), amelyet az FDA 2001-ben elfogadott, mint hatékony glaukómaellenes terápiát. Az SLT-kezelésben az áttörést 2019-ben a Lancet folyóiratban publikált LiGHT (Laser in Glaucoma and Ocular Hypertension) tanulmány hozta meg, ahol elsővonalbeli kezelésnek javasolták, mivel a hatékonysága hasonló volt, mint a szemcseppterápiának (1).
Az SLT egy frekvenciaduplázott ND-YAG 532 nm hullámhosszú, zöld fényű lézer, amely a betegek 60-75%-ánál minimum 20%-os intraokuláris nyomáscsökkenést (IOP) okoz (2).
A Pécsi Szemészeti Klinika 2016 májusa óta rendelkezik szelektív lézer trabekuloplasztika végzésére alkalmas készülékkel, amellyel eddig 433 beteget kezeltünk. Közleményünk célja, az SLT-kezelés hatékonyságának, a kezelésre történő beválasztás kritériumainak és a kezelési eredményeinknek az áttekintése.
Módszer
SLT hatásmechanizmusa
Wise és Witter 1979-ben ajánlotta először az argonlézer trabekuloplasztikát (ALT) glaukómában a szemnyomás csökkentésére. Az ALT eredményessége mellett az idővel fokozatosan csökkenő terápiás hatása és mellékhatásai miatt a kutatók tovább keresték a megfelelő lézeres megoldást. 1995-ben Latina és Park szelektív lézert javasolt a trabekuloplasztika elvégzéséhez (3).
A szelektív lézer trabekuloplasztika (SLT) más mechanizmussal csökkenti a szemnyomást, mint az ALT-kezelés. A trabekuláris endothelsejtek különböző mennyiségű melanint tartalmaznak, amely szelektíven abszorbeálja az SLT-lézer energiáját. A keletkező fototermolízis során ezek a sejtek szétesnek, de a környezetükben található nem-pigmentált sejtek és egyéb trabekuláris alkotóelemek nem károsodnak. Ennek az oka, hogy a melanin termikus relaxációs ideje (~1 milliszekundum) hosszabb, mint az egy alkalommal leadott lézerimpulzus időtartama (3 nanoszekundum), emiatt nem történik szignifikáns hőleadás a környező képletek felé. A melanintartalmú sejtek környezete nem károsodik, ezért nem alakul ki hegesedés, emiatt az SLT-kezelés ismételhető (4).
Indikációk
A szakirodalom és a saját tapasztalataink alapján bebizonyosodott, hogy évről évre nőtt azon indikációk száma, ahol érdemes az SLT-t alkalmazni a glaukóma kezelési stratégiájában.
Primer nyitott zugú glaukóma, okuláris hipertenzió
Kezdetben az SLT-t a primer nyitott zugú glaukóma (POAG) és okuláris hipertenzió (OHT) fokozott rizikójú csoportjának kezelésére ajánlották, és számos tanulmányban bizonyították a hatásosságát, mind kezdeti, mind kiegészítő kezelésként alkalmazva. Nemcsak korai, hanem előrehaladott látótér-károsodással rendelkező primer nyitott zugú glaukómában is vizsgálták és eredményesnek tartották a szemnyomáscsökkentő hatását (5).
Primer zárt zugú glaukóma
Eleinte az SLT nem tartozott a zárt zugú glaukómás betegek terápiás lehetőségei közé, de tanulmányok bizonyították az SLT hatékonyságát és biztonságosságát, amennyiben volt elegendő kezelésre alkalmas terület. Saját tapasztalatunk is azt támasztja alá, hogy amennyiben legalább 180 fokban elvégezhető a kezelés, már hatékony szemnyomás-csökkenést lehet elérni (6).
Egyéb típusú glaukómák
A primer nyitott és részlegesen zárt zugú glaukómák mellett pseudoexfoliációs glaukómában (PXFG), pigmentglaukómában (PG), normotenzív glaukómában (NTG) is hatékonyan alkalmazható az SLT. Egyre több új indikációs területet is vizsgálnak a hatékonyság szempontjából, így a szteroidindukálta glaukóma, a juvenilis glaukóma, glaukómaellenes műtétek (mély szklerectomia, trabekulectomia) utáni IOP-emelkedés és a szilikonolaj miatti szemnyomás-fokozódás esetében is hatékonynak bizonyult az SLT.
Nem ajánlják az SLT-kezelést az alábbi esetekben: teljesen zárt csarnokzug, akut gyulladás, neovaszkuláris glaukóma, kiterjedt perifériás elülső összenövés (PAS), traumás glaukóma, valamint a páciens kooperáció hiánya esetén (7).
Kezelés
Az SLT-kezelés vonatkozásában az energiaszintre, gócszámra vagy a lézer által kezelt terület nagyságára nincs egyértelmű nemzetközi ajánlás. A góc nagysága (400 mikrométer) és a kezelés ideje (0,3 nanoszekundum) azonban mindig állandó. Az energiatartomány elérhető spektruma az SLT-lézer készülékekkel 0,3-2,0 mJ, de a kezelések általában a 0,4-1,4 mJ közötti tartományban történnek (8). Kezdeti energiának a szakirodalomban 0,7-0,8 mJ energiaszintet javasolnak, emelkedő energiatitrálással 0,1 mJ lépésekkel, amíg a kavitációs buborék meg nem jelenik. Ezt az energiaszintet a küszöbenergiának tekintjük és itt vagy ez alatt 0,1 mJ-lal javasolt a kezelés. Minél pigmentáltabb a csarnokzug, annál alacsonyabb energia szükséges a kezelés elvégzéséhez. Az alkalmazott gócszám 50-100 darab egymást nem átfedve, a kezelési terület 180-360 fok (9). SLT utáni posztoperatív kezelés szempontjából nincs nemzetközi konszenzus. Két randomizált klinikai vizsgálatban a beavatkozás után kezeletlen, illetve gyulladásgátló szemcseppekkel (non-szteroid, szteroid) kezelt szemek összehasonlítása történt. Egyik tanulmány sem talált szignifikáns különbséget a gyulladásgátló terápiával kezelt és nem kezelt betegek esetében sem a hatékonyság, sem a posztoperatív mellékhatások tekintetében (10, 11, 12).
Mellékhatások
Az SLT kevés komplikációval járó beavatkozás. A nemzetközi publikációk alapján tapasztalt mellékhatások: enyhe iritis 89%, fájdalom vagy diszkomfort-érzés 5%, hyperaemia 6%, IOP-emelkedés 5%. Több tanulmányban vizsgálták a tranziens IOP-kiugrás előfordulását az SLT után. Ezek többségében, az IOP növekedését csak az SLT-beavatkozás napján észlelték, amely szemcseppekkel vagy szükség esetén per os gyógyszerekkel könnyen uralható volt és nem jelentett hosszú távú komplikációt. A szemnyomás megemelkedését a kezelt betegek 2-26,2%-ánál tapasztalták, és nagyobb valószínűséggel jelent meg pigmentáltabb zugok esetében. Az irodalomban ritkábban leírt mellékhatások: elülső csarnokvérzés, makulaödéma, szaruhártya-ödéma, szaruhártyagyulladás és a refrakció átmeneti megváltozása. Perifériás elülső összenövés (PAS) kialakulásáról csak két esetben számoltak be, mint SLT szövődménye (13).
Eredményeink
A Pécsi Szemészeti Klinika 2016 májusa óta rendelkezik szelektív lézer trabekuloplasztika végzésére alkalmas Opto YAG &SLT M (Optotek Medical, Szlovénia) készülékkel.
Klinikánkon 2016. május 1. és 2023. szeptember 1. közt 433 beteg esetében választottuk az SLT-kezelést. A 433 betegnél 468 alkalommal történt beavatkozás, összesen 834 szemen. A betegek 8,1%-ánál (35 fő) ismételtük a kezelést.
A betegek nem szerinti megoszlása az alábbiak szerint alakult: 237 nő (55%) és 196 férfi (45%). Az átlagéletkor 66,01 év (±12,125), a legfiatalabb betegünk 14 éves, a legidősebb 92 éves volt a kezeléskor.
A 2015 és 2023 között SLT-re kerülő betegszám és kezelt szemek száma az 1. ábrán látható.
A kezeléseket 2015-ben kezdtük 5 beteggel (8 kezelés), akkor még kipróbálásra kapott SLT-készülékkel. A Pécsi Szemészeti Klinika 2016 májusa óta rendelkezik OPTOTEK-készülékkel és ugyanebben az évben már 20 beteg 35 szemén végeztünk SLT-kezelést. 2017–2018-ban tovább emelkedett a kezelt betegek száma, majd a betegszám jelentős emelkedése 2019-ben következett be, ekkor 101 beteg 193 szemén történt kezelés. A COVID-19-járvány tetőzése alatt (2020–2021-ben) jelentősen csökkent a betegek száma, de ekkor sem állt le teljesen a kezelés. Mivel ebben az időszakban a műtétek korlátozottabban voltak elérhetők a járványügyi szabályozások miatt, az SLT egy optimális lehetőség volt, hogy kiegészítsük a terápiát, amennyiben a beteg szemnyomása céltartományon felül volt. Mivel nem a legideálisabb indikációkban tudtuk a járvány időszakában alkalmazni az SLT-t, a hatékonyság sem volt ugyanolyan mértékű, mint az ezt megelőző időszakban. A 2022. évben 88 beteggel és 174 kezeléssel már megközelítettünk a 2019-es betegszámot, és 2023-ban már szeptember hónap elejére elértük az előző évi statisztikát (1. ábra).
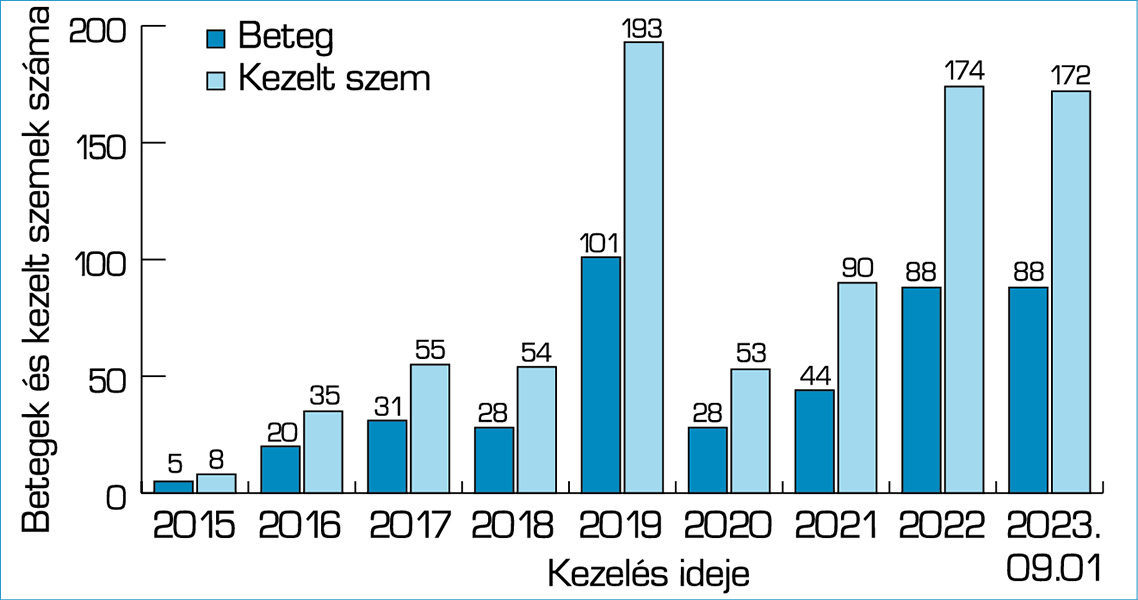
2015-ben 5 beteggel kezdtük az SLT-kezeléseket és fokozatosan emelkedett a betegek száma 2019-ig. A Covid-19-járvány alatt 2020–2021-ben a betegszám jelentősen lecsökkent 28 és 44 betegre, de 2019-ben ismét emelkedett, ekkor 88 beteget kezeltünk. 2023-ban az év első 2/3-ában már elértük az előző évi esetszámot, így az év végéig jelentős növekedés lesz az előző évi kezelésekhez képest. Az ábrán láthatóak a betegszámok és a kezelt szemek száma is.
A kezelésre kerülő betegek glaukómatípusok szerinti megoszlását a 2. ábrán tüntettük fel.
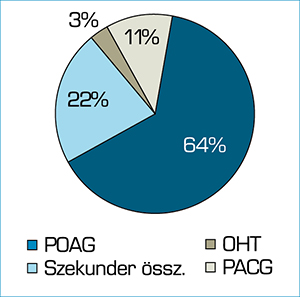
POAG-os betegek tették ki a kezeltek 64%-át (277 fő). A szekunder glaukómások képezték a 2. legnagyobb csoportot, a betegek 22%-a tartozott ide, ebből pseudoexfoliációs 9% (39 beteg), pigmentglaukómás 6% (26) beteg volt. A részlegesen zárt zugúak (PACG) a kezeltek 11%-át tették ki 49 beteggel. Okuláris hipertenzió (OHT) miatt a betegek 3%-át (13 beteg) kezeltük.
A 433 betegből a betegek 64%-a (277 fő) primer nyitott zugú glaukómával rendelkezett.
A második legnépesebb csoport 22%-kal a szekunder glaukómák vegyes csoportja, a 95 beteg megoszlása: 39 fő (9%) pseudoexfoliációs glaukómás (PXFG), 26 fő (6%) pigmentglaukómás (PG) és a többi beteg esetén műtét utáni szövődményből adódóan emelkedett meg a szemnyomás.
A részlegesen zárt zugú glaukómás betegek csoportja 11% (49 fő) volt – esetükben akkor végeztük el a kezelést, ha minimum 180 fokban el tudtuk végezni a lézeres kezelést.
SLT-re kerülő betegek megoszlását indikáció szerint a 3. ábra mutatja.
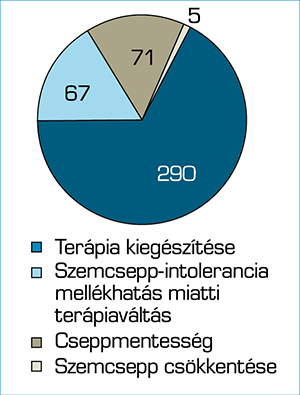
A legnagyobb indikációs csoport 290 fővel (67%) terápiakiegészítés céljából került kezelésre.
Szemcsepp hatóanyag- és tartósítószer-intolerancia miatt választottuk az SLT-kezelést 67 betegnél (15%) és 71 esetben (16%) cseppmentesség céljából végeztük el az SLT-kezelést.
A legnagyobb csoportba (a betegek 66,97%-a) 290 fő tartozott, akik esetében a meglévő glaukómaellenes terápia kiegészítése volt a cél a betegség előrehaladásának megelőzése érdekében. Ide soroltuk azon betegeket, akiknél a kezelőorvos a már maximális konzervatív terápia ellenére is a betegség progresszióját diagnosztizálta, azokat, akiknél a meglevő szemcsepp elégtelensége esetén nem újabb szemcseppet, hanem SLT-t alkalmaztunk, valamint a trabekulektomián átesett betegeket, akiknek a céltartománynál magasabb volt a szemnyomásuk. A szemcsepp-intolerancia vagy mellékhatás miatti terápiaváltás a betegek 15,47%-ánál (71 betegnél) volt a kezelés indikációja. Az SLT kiemelendő előnye, hogy biztonsággal és hatékonyan tudtuk alkalmazni kezdeti terápiaként olyan esetekben, amikor a beteg szerette volna elérni a cseppmentességet. 71 betegünk (16,34%) ezen indikáció miatt került SLT-kezelésre. Azt tapasztaltuk, hogy minél fiatalabb a beteg, annál könnyebben választja az SLT-kezelést kezdő terápiának. Bár már a kezdetekkor is alkalmaztuk az SLT-t első lépésként, a LiGHT-tanulmány megjelenése óta a kollégák is nagyobb arányban irányítják hozzánk a betegeket, hogy a lézerrel kezdődjön a glaukómaellenes terápia, vagy a monoterápia helyett cseppmentesség legyen elérhető. A 4. ábra a kezdő kezelés és kiegészítő kezelés arányát szemlélteti, és jól látható, hogy egyre jobban emelkedik az antiglaukómás cseppet nem igénylő kezdő kezelések száma a kiegészítő kezelések mellett.
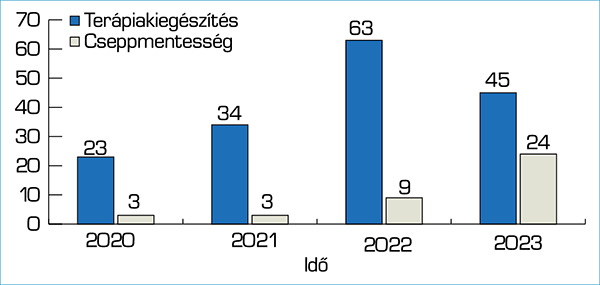
A monoterápiában részesülő betegek esetében is egyre többen válhattak cseppmentessé az SLT-t követően.
2020–2022 években a cseppmentesség miatti SLT-kezelések aránya 12%, 2023-ban a betegek 35%-a (24 beteg a 69-ből) került lézerkezelésre ezen indikáció miatt.
Kezelési stratégiánk
Amikor az SLT-vel elkezdtük a kezelést a Pécsi Szemészeti Klinikán, egyértelmű nemzetközi ajánlás nem volt sem az előkezelést, sem az utógondozást illetően, így kialakítottunk egy saját protokollt.
Meghatároztuk a kezelés indikációját, a szemnyomásmérések és látótér-vizsgálatok időpontjait, valamint a kezelés előtti és utáni terápiát.
Kezelés előkészítése
Kezelés napján elvégzett vizsgálatok: látóélesség-meghatározás, szemnyomásmérés (GAT)
A kezelést 25-26 Hgmm alatti IOP-értéknél végeztük el. Amennyiben ennél magasabb volt a szemnyomásérték, akkor átgondoltuk, hogy más terápia esetleg hatékonyabb lenne-e? Mivel a legoptimálisabb esetben sem tud az SLT-kezelés 30%-nál nagyobb IOP-csökkenést elérni, így az ennél lényegesebb magasabb szemnyomásértékeknél nem fogjuk a célszemnyomás-értéket elérni. Előkészítésként pilocarpin cseppet használunk. Bár a kezdetekkor a pilocarpin alkalmazását illetően a szakirodalomban egyértelmű ajánlás nem szerepelt, tapasztalataink alapján megfelelő előkészítési módszernek bizonyult.
Számos esetben előfordult, hogy a csarnokzug nem volt kellőképpen nyitott az SLT elvégzéséhez, de a pilocarpin hatására a kezelendő terület könnyebben láthatóvá vált. Több alkalom is volt, amikor társintézményből beutalt betegek esetén a pilocarpinnal történő előkészítés után az appozícionális, nagyrészben zárt csarnokzug miatt inkább YAG-iridotomiát végeztünk. Az esetek döntő többségében ilyenkor – ha a nyomás továbbra sem rendeződött – egy-két hónapon belül el tudtuk végezni az SLT-kezelést, mert az iridotomiát követően kellőképpen kiszélesedett a csarnokzug. A kezelést Goldmann-3-as tükör gonioszkópiás lencséjén keresztül végeztük.
Kezelés
Energia értéke
A kezelési energia meghatározásában a lézergóc leadása utáni buborék megjelenése volt az irányadó. A kezelést a buborék megjelenése során alkalmazott energiaszinten végezzük, vagy 0,1 mJ-lal az alatt. A kezdeti energia 1,0 mJ, majd 0,1 mJ lépésekkel emeljük vagy csökkentjük a buborék megjelenéséig. Minél pigmentáltabb a csarnokzug, annál alacsonyabb energia szükséges. Saját tapasztalataink alapján a legtöbb esetben 1,0 mJ energiát alkalmaztunk. A legalacsonyabb alkalmazott energiaszint 0,4 mJ, legmagasabb 1,5 mJ volt.
Kezelési terület
A lézergócok elhelyezését a csarnokzugban a trabekuláris hálózat pigmentált részére pozícionálva végeztük. Az eleinte 180°-ban alkalmazott 50 lézergóc után kb. 1 év múlva áttértünk a 360°-ban alkalmazott 100 lézergóc kezelési stratégiára. A lézergócok átmérőjének mérete 400 µm, amelyeket nem átfedő módon helyeztük el.
Kezelés utáni teendő, utánkövetés
Kezelés után közvetlenül 1 csepp fluorometholont cseppentettünk a kezelt szembe.
Otthoni használatra nem rendeltük el gyulladáscsökkentő kezelést, sűrűbb műkönny-alkalmazást javasoltunk az enyhe irritáció miatt. A szemnyomáskontrollt az alábbi gyakorlat szerint végeztük: számításba vettük a kezelésre történő beutalási IOP-értéket, majd feljegyeztük a közvetlenül a lézerkezelés előtt, a kezelés után 1 órával, 1 nappal, 1 hónappal, 3 hónappal, 6 hónappal és 12 hónappal mért adatokat, ezt követően személyre szabottan folytattuk a szemnyomás ellenőrzését. A kezelés utáni 1 órás szemnyomásmérést az irodalomban leírt IOP-kiugrás miatt végeztük. A lézeres kezelések megkezdését követő 2 éves tapasztalatunk alapján nem észleltünk IOP-kiugrás az előkészítő terápiák mellett, így az 1 órás szemnyomáskontrollt elhagytuk. Amennyiben a terápia módosítása vagy a cseppmentesség volt a cél, azt legkorábban 1 hónap múlva tettük meg, addig az eredeti terápiát folytatta a beteg. Ezt követően még 1 és 2 hónap múlva is megmértük a szemnyomást megbizonyosodva arról, hogy a szemnyomás elérte-e a célértékét a cseppmentesség esetén is.
Mellékhatások
Az SLT egy jól tolerálható kezelés, komoly mellékhatás nem volt tapasztalható sem a kezelés alatt, sem utána. A szemnyomás-emelkedés a kezelést követően az irodalmi adatok szerint maximum 6 Hgmm körüli, amely gyorsan lecseng, maximum 1 nap alatt.
Saját tapasztalatunk az volt, hogy a lézerkezelés előtt adott szemnyomáscsökkentő cseppekkel kivédhetjük a kezelés utáni IOP-emelkedést.
Hyperaemia megjelenésének a valószínűsége irodalmi adatok alapján 66%, amely maximum 1-2 napig tart. A betegek figyelmét felhívtuk, hogy 1-2 napig előfordulhat a szem kipirosodása, így ettől nem ijedtek meg, a sűrűbben adott műkönnycseppekkel könnyen tolerálható mellékhatás volt a betegek számára. Kisfokú iritis szempontjából az irodalmi adat 89% 2-3 nappal a kezelés után, amelynek az esélye nő megelőző ALT-kezelés és fokozottan pigmentált trabekuláris hálózat esetén. Az évek során azt tapasztaltuk, ha ki is alakult az enyhe iritis, a betegeink közül három esetben rendeltünk el átmeneti fluorometholon-terápiát, és csupán 1 beteget kezeltünk 1 hétnél hosszabban gyulladáscsökkentő szemcseppel. Az iritis kialakulására az esély megnő, amennyiben a lézergócokat nem pontosan a trabekuláris hálózatra helyezzük, hanem az íriszt is érinti, emiatt a lézerkezelés pontos lokalizációjára kiemelt hangsúlyt kell fektetni. Ideiglenes enyhe diszkomfort előfordulása az irodalmi adatok alapján 58%, amelyet a kezelt betegeink visszajelzése alapján is megerősíthetünk, azonban ez a fájdalomig nem fokozódott. Az irodalom által leírt ritka mellékhatások (elülsőcsarnok-vérzés, makulaödéma, foveaégés, szaruhártya-borússág) közül gyakorlatunkban csak 1 alkalommal alakult ki enyhe íriszvérzés és 2 esetben szaruhártya-erózió.
Kezelés hatékonysága
A hatékony/nem hatékony arány
A 433 kezelt betegből 367 főnél (84,76%) tudtunk felvenni teljes adatsort a szemnyomás szempontjából, így az ő eredményeik alapján értékeltük ki a kezelés eredményességét. A 20% feletti szemnyomáscsökkenést tekintettünk hatékonynak, ez 105 betegnél nem teljesült, így hatékony kezelést a betegek 71,34%-ánál értünk el. Más módon értékelhető a hatékonyság abban az esetben, amikor a cél a monoterápia helyett a cseppmentesség elérése. Ebben az esetben azt is hatékonynak tekinthetjük, ha a szemcseppel elért szemnyomás értékét mértük a cseppmentes állapotban is (5. ábra). Ha ezeket a betegeket kivesszük a „nem hatékony” csoportból – hisz itt nem a 20%-os szemnyomáscsökkentés a cél, hanem a megfelelő szemnyomás stabilizálása csepp nélkül is –, akkor csak 21,01%-ban (91 fő) nem volt hatékony a kezelés.
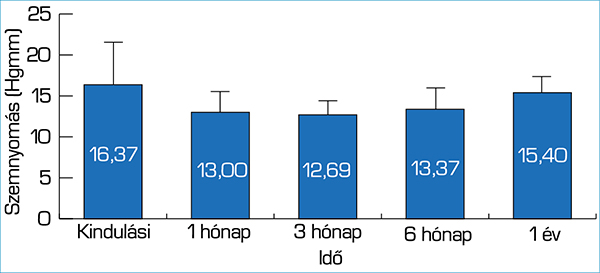
A kiindulási szemnyomásérték 16,37 Hgmm (±5,001 Hgmm). A szemnyomás átlagosan 13,00 Hgmm-re (±2,035 Hgmm) csökkent az első hónap végére. A 3. hónapban 12,69 Hgmm (±1,939 Hgmm), a 6. hónapban 13,37 Hgmm (±1,786 Hgmm) volt az átlagszemnyomás. Az első év végére a szemnyomás kis mértékben növekedett 15,40 Hgmm-re (±1,140 Hgmm) de még így sem érte el a kiindulási értéket.
Szemnyomáscsökkentés mértéke a hatékonynak tekintett csoportban
A hatékonyságot áttekintettük azon betegek esetében is, ahol 20% feletti szemnyomáscsökkenést tapasztaltunk a lézerkezelés hatására. Az átlag kezdeti szemnyomásérték 20,80 Hgmm (±6,879 Hgmm) volt, amely 1 hónappal a kezelés után átlag 14,67 Hgmm-re (±4,442 Hgmm) csökkent, amely megközelítőleg 29%-os, kb. 6 Hgmm-es szemnyomáscsökkenésnek felel meg. Az 1 hónap után mért alacsonyabb szemnyomásértékek átlaga az idő előrehaladtával minimálisan emelkedett, azonban a kezelést követő első év végére átlagosan így is kb. 26%-os szemnyomáscsökkenés volt megfigyelhető, amely több mint 5 Hgmm körüli csökkenést jelent (6. ábra).
A hatékonyság hosszú távú (1 éven túli) és indikációk szerinti megoszlásának feldolgozása folyamatban van.
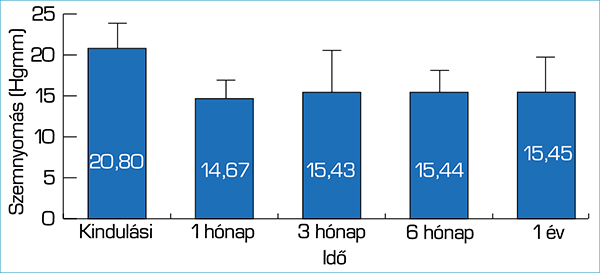
Azon betegeknél, ahol sikerült 20% feletti szemnyomás-csökkenést elérni, kiszámoltuk a csökkenés mértékét.
COVID-19 alatti SLT-kezelési tapasztalataink
Az új típusú koronavírus okozta pandémia alatt – mint minden betegségnek – a glaukómának a gondozása is teljesen átalakult, nagymértékben nehezíttetetté vált a rendszeres kontroll, így a legtöbb esetben a betegek az eredeti terápiájukat használták.
A járvány ideje alatt a rendszeres kontrollvizsgálatokra vagy egyáltalán nem, vagy igen korlátozottan volt lehetőség.
A rendeléseinken megjelent betegek főként a panasszal rendelkezők közül kerültek ki.
Amennyiben a klinikánkra beküldött betegeknél emelkedett szemnyomást vagy a betegség progresszióját tapasztaltuk, igyekeztünk a legbiztonságosabb és leghatékonyabb megoldást, esetleges terápiaváltást alkalmazni, hogy elérjük a szemnyomás célértékét. A cseppváltás, új cseppel való kiegészítés eredményének a felmérése miatti több kontroll nehezebben volt megoldható, így több alkalommal alkalmaztuk az SLT-kezelést a terápia kiegészítésére.
Néhány esetben felmerült, hogy a szemnyomást műtét által csökkentsük, de nem mindig voltak adottak a lehetőségek ennek kivitelezéséhez. Ilyenkor idő és funkciónyerés szempontjából – amennyiben a beteget alkalmasnak tekintettük – elvégeztük az SLT-kezelést.
A nehezített körülmények miatt nem lehetett a már bevált indikációs körben és a legoptimálisabb időben elvégezni a lézeres kezelést, vagy a kialakult rutin szerinti utánkövetési ritmusban folytatni a kontrollokat, emiatt az eredmények is sokkal szerényebbé váltak, összehasonlítva a járvány előtti időszakkal. A COVID-19-járvány az SLT-protokollunkban is hozott némi változást: a nagyszámú kezelés mellett sem tapasztaltunk IOP-kiugrást a kezelések után, így a lézeres beavatkozást követő 1 órás szemnyomáskontroll elmaradt. Az 1 napos szemnyomás-ellenőrzés megmaradt, azonban más intézményből beutalt betegeket a beutaló orvos felé irányítottuk kontrollvizsgálat céljából. Mivel a kezelés után gyulladást sem tapasztaltunk, rutinból továbbra sem írtunk gyulladáscsökkentőt, de a betegek figyelmét fokozottan felhívtuk, hogy bármely panasz esetén jelentkezzenek klinikánkon.
Megbeszélés
Az SLT bizonyított hatékonyságú antiglaukómás lézerkezelés, amellyel több, mint 25 éves nemzetközi tapasztalat áll rendelkezésre (14). Fokozatosan emelkedik az SLT-vel kezelt betegek száma és az SLT-kezelések aránya is a többi glaukómaellenes kezelési lehetőség között.
A LiGHT-tanulmány eredményei óta a szelektív lézer trabekuloplasztika elfoglalta méltó helyét a glaukómaellenes kezelések közt. A Pécsi Szemészeti Klinikán SLT-kezelésre kerülő betegek között is megemelkedett a cseppmentességet igénylők aránya a kiegészítő kezeléshez képest.
Sikeresen alkalmazható szemnyomáscsökkentésre mind kezdeti, mind kiegészítő terápiaként a korai és az előrehaladott betegségek kezelésében is. Az SLT-kezelésnek nincs szisztémás mellékhatása és a lokális mellékhatások is enyhék és reverzibilisek, így, ha szükséges, az SLT-kezelést megismételhetjük, amennyiben a hatása idővel csökken. Eredményeink is azt támasztják alá, hogy hatékony kezelés kiegészítő kezelésként is, hiszen az 1 éves szemnyomáscsökkenés értéke közel 26%-os. Amennyiben monoterápia leváltása a cél, szintén hatékonynak az SLT-kezelés, mert a szemcsepp elhagyása után sem emelkedett meg a szemnyomás a kezdeti érték fölé.
A tapasztalatok növekedésével egyre szélesedik azon indikációs kör, ahol bizonyítottan jó hatásfokkal alkalmazható az SLT. Az SLT költséghatékony és megbízható módszer elsődleges és akár önálló terápiaként is, és jó életminőséget biztosíthat a szemcseppes kezelések alternatívájaként. Mivel a glaukómások száma fokozatosan emelkedik a költséghatékonyság egyre fontosabb szemponttá válik, mind az egyén, mind a finanszírozó szempontjából. Az eddigi kezelési eredmények alapján a célunk az SLT szélesebb körű alkalmazása, az „utolsó esély” kategóriából a kezdő kezelések közé való beemelése mind szélesebb körben.
Nyilatkozat
A szerzők kijelentik, hogy eredeti közleményük megírásával kapcsolatban nem áll fenn velük szemben pénzügyi vagy egyéb lényeges összeütközés, összeférhetetlenségi ok, amely befolyásolhatja a közleményben bemutatott eredményeket, az abból levont következtetéseket vagy azok értelmezését.
Rövidítések
SLT: szelektív lézer trabekuloplasztika; FDA: Food and Drug Administration; ND YAG: neodymium-doped yttrium aluminum garnet; IOP: intraokuláris nyomás; ALT: argon lézer trabekuloplasztika; POAG: primer nyitott zugú glaukóma; OHT: okuláris hipertenzió; PXFG: pseudoexfoliációs glaukóma; PG: pigmentglaukóma; NTG: normotenzív glaukóma; PAS: perifériás anterior synechia/elülső összenövés; LiGHT study: Laser in Glaucoma and Ocular Hypertension Trial
Irodalom
1. Gazzard G, Konstantakopoulou E, Garway-Heath D, Barton K, et al. LiGHT Trial Study Group. Laser in Glaucoma and Ocular Hypertension (LiGHT) trial. A multicentre, randomised controlled trial: design and methodology. Br J Ophthalmol 2018 May; 102(5): 593–598. Epub 2017 Sep 13. Erratum in: Br J Ophthalmol 2021 Feb; 105(2): e1. PMID: 28903966.
https://doi.org/10.1136/bjophthalmol-2017-310877
2. Kagan DB, Gorfinkel NS, Hutnik CM. Mechanisms of selective laser trabeculoplasty: a review. Clin Exp Ophthalmol 2014 Sep-Oct; 42(7): 675–81. Epub 2014 Jan 27. PMID: 24330092.
https://doi.org/10.1111/ceo.12281
3. Bovell AM, Damji KF, Hodge WG, et al. Long term effects on the lowering of intraocular pressure: selective laser or argon laser trabeculoplasty? Can J Ophthalmol 2011 Oct; 46(5): 408–13. Epub 2011 Aug 4. PMID: 21995983.
https://doi.org/10.1016/j.jcjo.2011.07.016
4. Kagan DB, Gorfinkel NS, Hutnik CM. Mechanisms of selective laser trabeculoplasty: a review. Clin Exp Ophthalmol 2014 Sep-Oct; 42(7): 675–81. Epub 2014 Jan 27. PMID: 24330092.
https://doi.org/10.1111/ceo.12281
5. Zhou Y, Aref AA. A Review of Selective Laser Trabeculoplasty: Recent Findings and Current Perspectives. Ophthalmol Ther 2017 Jun; 6(1): 19–32. Epub 2017 Mar 3. PMID: 28258400; PMCID: PMC5449301
https://doi.org/10.1007/s40123-017-0082-x
6. Zhou Y, Aref AA. A Review of Selective Laser Trabeculoplasty: Recent Findings and Current Perspectives. Ophthalmol Ther 2017 Jun; 6(1): 19–32. Epub 2017 Mar 3. PMID: 28258400; PMCID: PMC5449301.
https://doi.org/10.1007/s40123-017-0082-x
7. Song J. Complications of selective laser trabeculoplasty: a review. Clin Ophthalmol 2016 Jan 14; 10: 137–43. PMID: 26834456; PMCID: PMC4716769.
https://doi.org/10.2147/OPTH.S84996
8. Latina MA, Park C. Selective targeting of trabecular meshwork cells: in vitro studies of pulsed and CW laser interactions. Exp Eye Res 1995 Apr; 60(4): 359–71. PMID: 7789416.
https://doi.org/10.1016/s0014-4835(05)80093-4
9. Latina MA, de Leon JM. Selective laser trabeculoplasty. Ophthalmol Clin North Am 2005 Sep; 18(3): 409–19. vi. PMID: 16054998.
https://doi.org/10.1016/j.ohc.2005.05.005
10. De Keyser M, De Belder M, De Groot V. Randomized Prospective Study of the Use of Anti-Inflammatory Drops After Selective Laser Trabeculoplasty. J Glaucoma 2017 Feb; 26(2): e22–e29. PMID: 27552500.
https://doi.org/10.1097/IJG.0000000000000522
11. Zhou Y, Aref AA. A Review of Selective Laser Trabeculoplasty: Recent Findings and Current Perspectives. Ophthalmol Ther 2017 Jun; 6(1): 19–32. Epub 2017 Mar 3. PMID: 28258400; PMCID: PMC5449301.
https://doi.org/10.1007/s40123-017-0082-x
12. Groth SL, Albeiruti E, Nunez M, et al. SALT Trial: Steroids after Laser Trabeculoplasty: Impact of Short-Term Anti-inflammatory Treatment on Selective Laser Trabeculoplasty Efficacy. Ophthalmology 2019 Nov; 126(11): 1511–1516. Epub 2019 Jun 6. PMID: 31444008; PMCID: PMC6810843.
https://doi.org/10.1016/j.ophtha.2019.05.032
13. Song J. Complications of selective laser trabeculoplasty: a review. Clin Ophthalmol 2016 Jan 14; 10: 137–43. PMID: 26834456; PMCID: PMC4716769.
https://doi.org/10.2147/OPTH.S84996
14. Arora KS, Robin AL, Corcoran KJ, et al. Use of Various Glaucoma Surgeries and Procedures in Medicare Beneficiaries from 1994 to 2012. Ophthalmology 2015 Aug; 122(8): 1615–24. Epub 2015 Jun 16. PMID: 26092196.
https://doi.org/10.1016/j.ophtha.2015.04.015
