Anterior Segment Optical Coherence Tomography of Corneal Grafts Underwent Penetrating Keratoplasty
doi: 10.55342/szemhungarica.2024.161.3.134
Original scientific paper
Summary
Purpose: Imaging techniques, such as Optical Coherence Tomography (OCT) and tomography based on the Scheimpflug principle, are of great importance in the diagnosis and follow-up of corneal pathologies as well as in post-operative monitoring of the cornea. From the high resolution cross-sectional images, the axial curvature of both corneal surfaces, and corneal thickness can be measured, thus total corneal power can be calculated. We compared keratometric and pachymetric data from anterior segment OCT between two groups of post-penetrating keratoplasty patients and healthy individuals. The reproducibility of these data was studied as well in both groups.
Methods: 23 post-penetrating keratoplasty patients were examined using swept-source anterior segment OCT (Anterion, Heidelberg Engineering GmbH, Heidelberg, Germany) on average 73.1±13.4 months after suture removal. The control group comprised data from 56 healthy individuals. Axial curvature of anterior and posterior corneal surfaces and total corneal power at the steep and flat meridians were measured. The mean central value of the total corneal power was also registered. The central corneal thickness and thinnest corneal point thickness were also the parameters that we compared between the two groups. Reproducibility of keratometric and pachymetric data was measured on 13 post-penetrating keratoplasty patients and 15 healthy individuals, obtaining data 3 times on each eye.
Results: Axial curvatures at the steep meridian of anterior (48.3±3.5 D vs. 44.4±3.0 D; p<0.001) and posterior corneal surfaces (–6.9±0.4 D vs. –6.5±0.6 D; p=0.001) were greater in the post-keratoplasty group than in the control group. These values did not differ significantly at the flat meridian (anterior surface axial curvature: 43.5±2.9 D vs. 42.9±2.2 D; p=0.302; posterior surface axial curvature: –6.0±0.5 D vs. –6.1±0.4 D; p=0.276). Total corneal power at the steep meridian (48.5±4.0 D vs. 43.8±3.1 D; p<0.001) and its mean central value (46.1±3.2 D vs. 43.1±2.7 D; p<0.001) were also greater in the post-keratoplasty group. There was no significant difference in the total corneal power at the flat meridian between the two groups (43.7±3.1 D vs. 42.5±2.7 D; p=0.084). The mean central corneal thickness was 567.0±49.9 µm after penetrating keratoplasty, significantly larger than in the control group (537.2±48.8 µm; p=0.016). However, no significant difference was observed between the two groups in the thinnest corneal point thickness (534.9±59.1 µm vs. 526.7±50.4 µm; p=0.534). Intraclass correlation coefficient was greater than 0.9 in both groups for each keratometric and pachymetric parameter.
Conclusions: Swept-source OCT provides reliable, well reproducible data on corneal curvature and thickness in post-keratoplasty patients and healthy individuals as well. Besides best corrected visual acuity, anterior segment OCT is an excellent tool for the assessment and monitoring of the optical results after corneal transplantation.
Összefoglaló
Célkitűzés: A szaruhártya-kórképek diagnosztikájában, követésében, valamint a szaruhártyaműtétek utáni állapot ellenőrzésében az optikai koherencia tomográfián (OCT) és Scheimpflug-elven működő képalkotó módszerek nagy jelentőséggel bírnak. Segítségükkel nagy felbontású keresztmetszeti képek nyerhetőek, valamint a szaruhártya vastagsága, elülső és hátulsó görbülete, így optikai törőereje válik meghatározhatóvá. Jelen tanulmányunkban elülső szegmentum optikai koherencia tomográfiával mért keratometriai és pachymetriai értékeket hasonlítunk össze perforáló keratoplasztikán átesett és egészséges szemek csoportján. Vizsgáltuk továbbá a műszer által mért értékek reprodukálhatóságát mindkét csoportban.Módszerek: 23 perforáló keratoplasztikán átesett szemen végeztünk méréseket swept-source elven működő elülső szegmentum optikai koherencia tomográfiával (Anterion, Heidelberg Engineering GmbH, Heidelberg, Németország) átlagosan 73,1±13,4 hónappal a varratszedés után. Kontrollcsoportnak 56 egészséges szem adatait vettük alapul. Mindkét csoportban vizsgáltuk az elülső és hátulsó felszíni axiális, valamint a teljes cornealis törőerőt a meredek és a lapos tengelyben. A teljes cornealis törőerő esetén a centrális átlagértéket is megmértük. Továbbá a centrális cornealis vastagságot és a szaruhártya legvékonyabb pontjának értékét hasonlítottuk össze a két csoport között. A mért keratometriai és pachymetriai adatok reprodukálhatóságát is mértük 13 keratoplasztika utáni és 15 egészséges szemen, a méréseket egyénenként 3-szor megismételve.
Eredmények: A meredek tengelyben mért axiális törőerő nagyobb volt az elülső (48,3±3,5 D vs. 44,4±3,0 D; p<0,001) és a hátsó felszínen (–6,9±0,4 D vs. –6,5±0,6 D; p=0,001) keratoplasztika után a kontrollcsoporthoz képest. Ugyanezen értékek a lapos tengelyben azonban nem különböztek a két csoportban (elülső axiális görbület: 43,5±2,9 D vs. 42,9±2,2 D; p=0,302; hátulsó axiális görbület: –6,0±0,5 D vs. –6,1±0,4 D; p= 0,276). A teljes cornealis törőerő meredek tengelyben mért (48,5±4,0 D vs. 43,8±3,1 D; p<0,001) és átlagos centrális értékei (46,1±3,2 D vs. 43,1±2,7 D; p<0,001) szintén nagyobbak voltak a műtéten átesett csoportban. A lapos tengelyben mért teljes cornealis törőerő nem különbözött szignifikánsan a két csoportot összehasonlítva (43,7±3,1 D vs. 42,5±2,7 D; p=0,084). A szaruhártya centrális vastagsága keratoplasztika után 567,0±49,9 µm volt, amely szignifikánsan vastagabb volt az ép kontrollszemekhez képest (537,2±48,8 µm; p=0,016). A legvékonyabb pontot mérve azonban nem adódott szignifikáns különbség a két csoport közt (534,9±59,1 µm vs. 526,7±50,4 µm; p=0,534). Az intraclass korrelációs együttható (ICC) mindkét csoportban az összes vizsgált keratometriás és pachymetriás paraméterre nézve 0,9 feletti értéket mutatott.
Következtetések: A swept-source OCT a szaruhártya görbületéről és vastagságáról megbízható, jól reprodukálható adatokat biztosít mind egészséges, mind keratoplasztikán átesettek körében. A korrigált látóélesség meghatározása mellett az elülső szegmentum OCT kiváló eszköz a műtét utáni optikai eredmény ellenőrzésére, követésére.
Keywords
optical coherence tomography (OCT), cornea, keratoplasty, anterior segment (AS)
Kulcsszavak
optikai koherencia tomográfia (OCT), szaruhártya, keratoplasztika, elülső szegmentum
Bevezetés
Az elülső szegmentum képalkotására számos technológia áll rendelkezésre. Ezek közül az ún. tomográfiás módszerek keresztmetszeti képekből rekonstruálják az elülső szegmentumot. Az OCT infravörös fényt, míg a Scheimpflug-elven működő tomográf látható spektrumba eső fényt (475 nm hullámhosszúságú kék fényt) használ. Előnyük a hagyományos topográfiai módszerekkel szemben, hogy nemcsak a szaruhártya elülső felszínét vizsgálják, hanem a teljes elülső szegmentumot a könnyfilmtől a hátulsó lencsetokig. Az OCT-technológia már az elmúlt két évtizedben széles körben elterjedt a retinalis kórképek diagnosztikájában. Ez a technológia azonban az elülső szegmentum képleteiről is képes hasonló, mikrométeres felbontású rekonstruált képeket készíteni. A vizsgálat egyik fontos indikációja szaruhártya-átültetést követően a transzplantátumok utánkövetése. Keratoplasztikát végzünk konzervatív terápiával nem kezelhető jelentős látóélesség-csökkenést okozó szaruhártya kórképek esetén. A műtét következtében még a tökéletes anatómiai eredmény mellett is várható a szaruhártya fiziológiájának, geometriájának megváltozása. Ennek oka a donorszaruhártya eltérő görbülete, a varratok húzóhatása, valamint az, hogy a trepanált donorszövet átmérője rendszerint kissé mindig nagyobb, mint a recipiensből szintén trepanációval eltávolított szövet átmérője. A fent említett hatások különösen az elülső cornealis felszínt érintő beavatkozásoknál (perforáló keratoplasztika – PKP, mély elülső lamelláris keratoplasztika – DALK) érvényesülnek, és különböző mértékben járulnak hozzá a szaruhártya törőerejéhez. Ezekben az esetekben a legjobban korrigált látóélesség széles skálán változhat. Tanulmányunkban elülső szegmentum optikai koherencia tomográfiával mért keratometriai és pachymetriai értékeket hasonlítottunk össze perforáló keratoplasztikán átesett és egészséges szemek csoportján. Ezen értékek jelentősen befolyásolják a műtét utáni látóélességet és a korrekciós lehetőségeit. Az adatok megfelelő értékelése szempontjából fontos az is, hogy a vizsgáló az általa használt tomográffal nyert adatok ismételhetőségével, reprodukálhatóságával tisztában legyen, ezért a méréseket kiterjesztettük ebbe az irányba is.
Betegek és módszerek
Vizsgálataink során meghatároztuk a szaruhártya elülső és a hátulsó felszíni axiális törőerejét, valamint a teljes cornealis törőerőt a meredek és a lapos tengelyekben, ezen kívül még a centrális és a cornea legvékonyabb pontján mért vastagságot AS-OCT-vel (Anterion, Heidelberg Engineering GmbH, Heidelberg, Németország) 23 perforáló cornealis grafton átlagosan 73,1±13,4 hónappal a varratszedés után. A teljes törőerő esetén a két tengelyben mért érték mellett egy harmadik, átlagos értéket is rögzítettünk. Az Anterion speciálisan a szaruhártya-diagnosztikára fejlesztett beállítása mellett a centrális 3 mm-es zónában számított keratometriai adatokat jelzi ki. Azonban a kívánt numerikus adatokat közvetlenül is leolvashatjuk tetszőleges helyen a cornea-topográfiához hasonló színskálázott térképek segítségével. Az asztigmia mértékére következtethetünk a meredek és lapos tengelyben mért elülső axiális törőerők különbségéből, de a műszer ezt külön értékként megjeleníti az asztigmia tengelyével együtt. A szabályos asztigmiára jellemző, színes térképen látható szimmetrikus „csokornyakkendő” mintázattól való eltérés pedig az asztigmia irregularitására utal. A berendezés továbbá képes hullámfront-analízissel a magasabb rendű optikai aberrációkat is megjeleníteni. Segítségével a szem tengelyhossza is megítélhető, így intraocularis műlencse tervezésére is használható. A mikrométeres felbontású, rekonstruált térbeli képek segítségével a szaruhártya geometriája mellett az elülső csarnok mélysége, a csarnokzug nyitottsága, az írisz helyzete is kiválóan megjeleníthető. Lamelláris keratoplasztikáknál pedig a donorlamella helyzetét, recipienssel való érintkezését vizualizálhatjuk. Vizsgálatunkban a transzplantátumokat 56 olyan egészséges szem szaruhártyájához viszonyítottuk, akiknél a szürkehályog-műtét előtti biometria AS-OCT-vel készült. Kontrollcsoportba bevont egyéneknél korábbi szembetegség, műtéti beavatkozás nem fordult elő és a fénytörési hibájuk nem haladta meg a 3 dioptriát. A keratoplasztikán átesettek életkora átlagosan 52,7 év volt, a kontrollcsoporté 44,9 év. A műtétet 8 esetben dystrophia corneae, 6 esetben keratoconus, 5 esetben degeneratio corneae, 3 esetben keratopathia bullosa indikálta, 1 esetben pedig ismételt keratoplasztika történt. A műszer által nyert adatok reprodukálhatóságát is mértük, megvizsgálva, hogy ugyanahhoz a szaruhártyához tartozó paraméterek mennyire térnek el az egymás utáni mérések során 15 ép és 13 keratoplasztikán átesett szemen. Ennek kivitelezése céljából ugyanarról a szemről három egymást követő mérést végeztünk, amik között a vizsgált személy az állát az álltartóról két-két percre elemelte. A keratometriai és a pachymetriai értékeken a leíró statisztikai elemzés mellett kétmintás t-próbát végeztünk, valamint a reprodukálhatóság vizsgálatára intraclass korrelációs együtthatót (ICC) határoztunk meg.
Eredmények
A vizsgált keratometriai és pachymetriai értékek átlagát, standard deviációját az 1. táblázat mutatja.
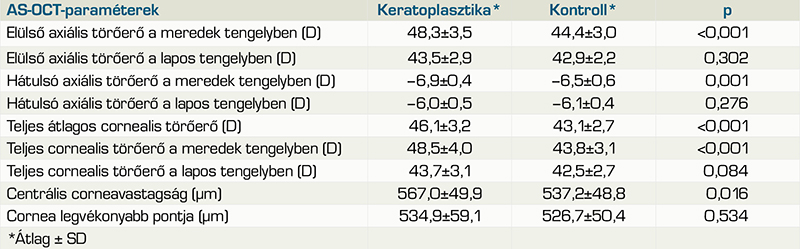
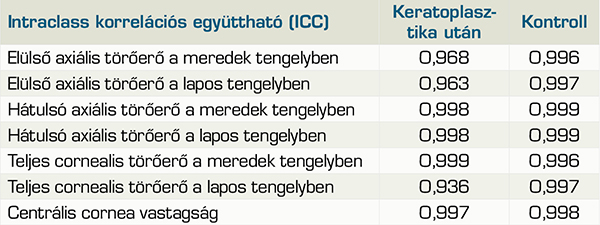
A perforáló keratoplasztikán átesett csoportban szignifikánsan nagyobb volt az axiális törőerő a kontrollcsoporthoz képest a meredek tengelyben az elülső (48,3±3,5 D vs. 44,4±3,0 D; p<0,001) és a hátulsó felszínen egyaránt (–6,9±0,4 D vs. –6,5±0,6 D; p=0,001). Ezek a különbségek a teljes cornealis törőerő értékeiben is megmutatkoztak: a meredek tengelyben mért (48,5±4,0 D vs. 43,8±3,1 D; p<0,001) és az átlagos teljes törőerő is (46,1±3,2 D vs. 43,1±2,7 D; p<0,001) szignifikánsan nagyobb volt a transzplantált csoportban. A lapos tengelyben mért értékek nem különböztek szignifikánsan (elülső axiális görbület: 43,5±2,9 D vs. 42,9±2,2 D; p=0,302; hátulsó axiális görbület: –6,0±0,5 D vs. –6,1±0,4 D; p=0,276; teljes cornealis törőerő: 43,7±3,1 D vs. 42,5±2,7 D; p=0,084). A pachymetriai adatokban is szignifikáns különbséget találtunk: a műtéten átesett csoportban centrálisan vastagabb volt a szaruhártya (567,0±49,9 µm vs. 537,2±48,8 µm; p=0,016), míg a legvékonyabb pont vastagságában nem mutatkozott szignifikáns különbség (534,9±59,1 µm vs. 526,7±50,4 µm; p=0,534). A reprodukálhatóság mérőszáma vizsgálatunkban az intraclass korrelációs együtthatók (ICC), amelyek 15 ép és a 13 keratoplasztikán átesett szemen minden vizsgált AS-OCT-paraméterre nézve 0,9 feletti értékeket mutattak, amelyek az adatok nagyfokú reprodukálhatóságára utalnak (2. táblázat).
Megbeszélés
Jelen tanulmányunkban perforáló keratoplasztikán átesett szaruhártyákat vizsgáltunk nagy felbontású, swept-source elven működő elülső szegmentum optikai koherencia tomográfia segítségével. A méréseket egészséges szemek hasonló adataival hasonlítottuk össze. Meghatároztuk a készülék reprodukálhatóságát is mindkét csoportban. Az OCT rövid koherencia hosszú interferometria elvén működő képalkotó eljárás. Működési elve a műszer által kibocsátott infravörös fénynek a vizsgált szövet rétegeiben való visszaverődésén alapul, hasonlóan az ultrahangkészülékekhez azzal a különbséggel, hogy utóbbi mechanikai (hang) hullámokat használ (1). Az első OCT-készülék biológiai alkalmazásáról először 1991-ben számoltak be, miszerint az eljárás képes a retinát és a koronáriákat, mint biológiai szöveteket mikrométeres felbontásban ábrázolni (2). A módszer elülső szegmentumon történő első sikeres alkalmazását 1994-ben mutatták be (3). Azóta a technológia állandóan fejlődik, a korábbi time-domain (TD) rendszereket Fourier-domain rendszerek (spectral-domain – SD – majd swept-source – SS – technológiák) váltották fel. Az így elért gyorsabb képfelvételi sebesség jobb képminőséggel, kisebb szemmozgásra való érzékenységgel is járt (1). Az általunk használt műszer (Anterion) swept-source rendszerrel van ellátva.
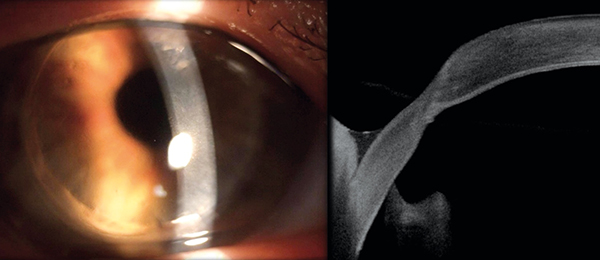
Vizsgálatainkban a lapos tengelyben mért törőerő-értékek nem különböztek szignifikánsan a műtéten átesettek és az egészségesek között. Ugyanakkor a meredek tengelyben mért axiális törőerő szignifikánsan nagyobb volt a keratoplasztikán átesett csoportban a kontrollokhoz képest. Ennek legvalószínűbb okai a donor és a recipiens trepanációs átmérőjének különbsége és a varratok kompressziós hatása. A transzplantált corneák átlagos elülső felszíni axiális törőereje a meredek tengelyben 48,3±3,5 D volt. Más tanulmányok ugyanezen paramétere hasonló értékeket mutattak (47,25±5,30 D; 47,9 D) (4, 5). Nassar és munkatársai továbbá arra a következtetésre jutottak, hogy a keresztmetszeti felvételeken a recipienssel határos, nem pontosan illeszkedő (hátsó cornealis felszín síkjából kiemelkedő vagy bemélyedt) graft-területek száma összefügg a posztoperatív asztigmia mértékével (6). Az axiális törőerő értékei még varratszedés után évekkel is változhatnak, amelyek különösen a keratoconus indikációval átültetett graftokon mutatkoznak meg (7). Raecker és munkatársai szerint a keratoconus miatt végzett perforáló műtétek után a transzplantátumok átlagos topográfiás keratometriai értéke és asztigmiája idővel folyamatosan nő. Ezek a paraméterek 10 év elteltével szignifikánsan nagyobbak voltak összehasonlítva a Fuchs-dystrophia miatt végzett műtétek eredményeivel, és további évek elteltével az észlelt különbség tovább nőtt (7). Tapasztalataink szerint – amennyiben a keratoconus miatt végzett műtétek után kellően hosszú idő, több év, évtized telik el – a megváltozott cornealis geometria a numerikus adatok mellett réslámpánál is megfigyelhető: a transzplantátum kiboltosul, a donor és recipiens érintkező felszíne megnyúlik, ugyanezen terület elvékonyodik, valamint a hegvonal elülső és hátulsó felszínen lévő kontúrja eltávolodik egymástól (1. ábra). Ezt a megfigyelést mások is megerősítették (8).
Méréseink szerint az átlagos centrális corneavastagság is szignifikánsan nagyobb volt a műtéti csoportban (567,0±49,9 µm) a kontroll egyénekhez képest, emellett hasonlóságot mutatott korábbi közlemények eredményeivel (526,0 µm; 555,0 µm; 537,4 µm; 635,9 µm; 536,0 µm; 563,0 µm) (9–12). Ugyanakkor a legvékonyabb cornealis ponton mért érték nem különbözött szignifikánsan a két csoportot összehasonlítva.
Korábban már összehasonlították az SS-OCT megbízhatóságát és reprodukálhatóságát a Scheimpflug-képalkotóhoz képest perforáló keratoplasztikán átesett betegeken. Az SS-OCT mind az elülső és hátulsó keratometriai adatokat, a centrális cornealis vastagságot, és az elülső csarnokmélységet is nagyobb megbízhatósággal, jobb reprodukálhatósággal mérte, mint a Scheimpflug-képalkotó eljárás (7). Hasonló eredményre jutott egy másik vizsgálat is, amely a két képalkotót operált és nem operált Fuchs-dystrophiás szemeken, valamint ép szaruhártyákon mért ICC-értékekkel hasonlította össze (13). A megbízhatóságbeli különbségek egyik fő oka arra vezethető vissza, hogy a látható fényt használó Scheimpflug-elvvel szemben az OCT infravörös tartományban lévő fénnyel működik. Az 1050–1300 nm-es tartományban lévő fény szöveti penetrációja jobb, mint a kisebb hullámhosszú fénysugaraké, illetve a látható fényt a biológiai szövetek nagyobb mértékben szórják az infravörös sugarakhoz képest (14, 15). A mindennapok is ezt igazolják, a Scheimpflug-képalkotóval különösen a hátsó cornealis felszínre vonatkoztatott paraméterekről nehéz vagy lehetetlen pontos számszerű adatokat nyerni abban az esetben, amikor a szaruhártya csökkent transzparenciájú területekkel is rendelkezik. Mindennek köszönhetően az SS-OCT-készülék jobban reprodukálható méréseket biztosít. Az általunk mért magas ICC-értékek megerősítik a korábbi tomográfiás vizsgálatok eredményeit, miszerint az AS-OCT nagy megbízhatósággal mér keratometriai és pachymetriai adatokat ép és műtéten átesett szaruhártyákon egyaránt.
Következtetések
Összességében megállapítható, hogy AS-OCT-vel a meredek tengelyben mért axiális görbületek és a centrális cornealis vastagság nagyobbak a perforáló keratoplasztika után az ép corneákhoz képest. Ugyanakkor a lapos tengelyben és a legvékonyabb pontban jelentős különbség nem mutatkozott. Az AS-OCT megbízható adatokat biztosít a szaruhártya összes paraméteréről. A műszer lehetőséget teremt refrakció szempontjából a műtéti eredmény utánkövetésére. Utóbbi abban lehet segítségére a szemorvosnak, hogy eldöntse, milyen refrakciót tovább javító konzervatív vagy műtéti megoldás megfelelő a páciens számára.
Nyilatkozat
A szerzők kijelentik, hogy eredeti közleményük megírásával kapcsolatban nem áll fenn velük szemben pénzügyi vagy egyéb lényeges összeütközés, összeférhetetlenségi ok, amely befolyásolhatja a közleményben bemutatott eredményeket, az abból levont következtetéseket vagy azok értelmezését.
Irodalom
1. Lukács MÁ, Módis L. Elülsőszegmentum-optikaikoherencia-tomográfia (OCT) a korszerű szemészeti diagnosztikában. [Anterior segment optical coherence tomography in modern ophthalmic diagnostics]. Orv Hetil 2024 Jul 21; 165(29): 1112–1121. Hungarian.
https://doi.org/10.1556/650.2024.33085
2. Huang D, Swanson EA, Lin CP, Schuman JS, Stinson WG, Chang W, Hee MR, Flotte T, Gregory K, Puliafito CA, et al. Optical Coherence Tomography. Science 1991 Nov 22; 254(5035): 1178–81.
https://doi.org/10.1126/science.1957169.
3. Izatt JA, Hee MR, Swanson EA, Lin CP, Huang D, Schuman JS, Puliafito CA, Fujimoto JG. Micrometer-scale resolution imaging of the anterior eye in vivo with optical coherence tomography. Arch Ophthalmol 1994 Dec; 112(12): 1584–9.
https://doi.org/10.1001/archopht.1994.01090240090031
4. Szalai E, Németh G, Hassan Z, Módis L Jr. Noncontact Evaluation of Corneal Grafts: Swept-Source Fourier Domain OCT Versus High-Resolution Scheimpflug Imaging. Cornea 2017 Apr; 36(4): 434–439. https://doi.org/10.1097/ICO.0000000000001133
5. Quintin A, Hamon L, Mäurer S, Langenbucher A, Seitz B. Vergleich der sterilen Spendertomographie in der Hornhautbank mit der Tomographie des Transplantates nach perforierender Keratoplastik. [Comparison of sterile donor tomography in the eye bank and graft tomography after penetrating keratoplasty]. Ophthalmologe 2021 Oct; 118(10): 1038–1044. German.
https://doi.org/10.1007/s00347-020-01256-6
6. Nassar GA, Arfeen SAES. Correlation between the graft-host junction of penetrating keratoplasty by anterior segment-optical coherence tomography and the magnitude of postoperative astigmatism. Indian J Ophthalmol 2017 Jul; 65(7): 574–578.
https://doi.org/10.4103/ijo.IJO_820_16
7. Raecker ME, Erie JC, Patel SV, McLaren JW, Hodge DO, Bourne WM. Long-term keratometric changes after penetrating keratoplasty for keratoconus and Fuchs Endothelial dystrophy. Am J Ophthalmol 2009 Feb; 147(2): 227–33.
https://doi.org/10.1016/j.ajo.2008.08.001
8. Weller JM, Hübner L, Kruse FE, Tourtas T. Characterisation of ectasia after penetrating keratoplasty in keratoconus eyes using anterior segment optical coherence tomography. Br J Ophthalmol 2024 Mar 20; 108(4): 506–512.
https://doi.org/10.1136/bjo-2022-322859
9. Uchino Y, Shimmura S, Yamaguchi T, Kawakita T, Matsumoto Y, Negishi K, Tsubota K. Comparison of corneal thickness and haze in DSAEK and penetrating keratoplasty. Cornea 2011 Mar; 30(3): 287–90. https://doi.org/10.1097/ICO.0b013e3181eeafd6
10. Pöltner G, Miller K, Berke A, Sickenberger W. Measuring of corneal thickness of contact lens wearers with keratoconus and keratoplasty by means of optical coherence tomography (OCT). Coll Antropol 2013 Apr; 37(Suppl 1): 165–73.
11. Raj A, Dhasmana R, Bahadur H, Nagpal RC. Evaluation of the Central Corneal Thickness with Anterior Segment Optical Coherence Tomogram after Penetrating Keratoplasty. J Clin Diagn Res 2016 Oct; 10(10): NC05-NC08.
https://doi.org/10.7860/JCDR/2016/20648.8750
12. Molter Y, Milioti G, Langenbucher A, Seitz B. Zeitpunkt, Rezidive und Prognose der immunologischen Abstoßungsreaktion nach Keratoplastik [Appearance, recurrence and prognosis of immunological graft rejection after penetrating keratoplasty]. Ophthalmologe. 2020 Jun; 117(6): 548–556. German.
https://doi.org/10.1007/s00347-019-00975-9
13. Arnalich-Montiel F, Ortiz-Toquero S, Auladell C, Couceiro A. Accuracy of Corneal Thickness by Swept-Source Optical Coherence Tomography and Scheimpflug Camera in Virgin and Treated Fuchs Endothelial Dystrophy. Cornea 2018 Jun; 37(6): 727–733.
https://doi.org/10.1097/ICO.0000000000001530
14. Li P, Johnstone M, Wang RK. Full anterior segment biometry with extended imaging range spectral domain optical coherence tomography at 1340 nm. J Biomed Opt 2014 Apr; 19(4): 046013.
https://doi.org/10.1117/1.JBO.19.4.046013
15. Wai-Fung Cheong, Scott A. Prahl, Ashley J. Welch. A Review of the Optical Properties of Biological Tissues. IEEE J Quantum Electronics 1990 Dec; 26(12): 2166–2185.
