Ocular surface graft versus host disease – diagnostics and therapy in our practice
doi: 10.55342/szemhungarica.2022.159.2.80
Original scientific paper
Summary
Purpose: Ocular graft versus host disease is a chronic ocular surface inflammation developing after allogenic haematopoetic stem cell transplantation. In this retrospective study, we analysed the data of patients, who were treated for ocular surface graft versus host disease in our ocular surface disease clinic between 2013, and February 2022.
Methods: After collecting anamnestic data, dry eye symptoms, signs of blepharitis, the measure of hyperaemia, scarring of conjunctiva, and the severity of corneal damage were recorded. We gathered therapeutic methods and observed patients’ status during the follow-up period.
Results: Eight patients suffering from ocular surface graft versus host disease were treated in the examined period (2 females, 6 males, age: 33.3±11.6 years). Ocular surface graft versus host disease developed 5-36 months after the transplantation. Systemic graft versus host disease preceded ocular involvement in every patient. The main complaints were dry eye and photosensitivity of 5 and 3 patients, respectively. Subconjunctival scarring was observed in 3 patients, symblepharon in one case. In four cases, corneal surfaces were damaged moderately, but they were involved in 3 patients severely. In addition to the tear substitution, autologous serum drops, fluorometholone drops, lacrimal punctal plug, therapeutic contact lens and cyclosporine eye drops were applied as treatment. During the follow-up periods (ranging from half-year to 7 years), the state of the ocular surfaces improved or stabilized at various severity stages. In one case, total limbal stem cell deficiency developed as a consequence of a bacterial ulcer.
Conclusions: If ocular graft versus host disease is recognized early and treated properly, the comfort of the patient and the state of the ocular surface can be improved significantly. In late-diagnosed-cases, irreversible damage can be developed, thus impairing life quality significantly.
Összefoglaló
Célkitűzés: Az ocularis graft versus host betegség allogén hemopoetikus őssejt-transzplantáció után kialakuló krónikus szemfelszíni gyulladás. Retrospektív tanulmányunkban a 2013. és 2022. február között klinikánk szemfelszíni ambulanciáján megfordult, szemfelszíni graft versus host betegségben szenvedő páciensek adatait dolgoztuk fel.Módszerek: Az anamnesztikus adatok rögzítése után összegyűjtöttük a szemszárazságra utaló tüneteket, a blepharitis jeleit, a kötőhártya belövelltségének és hegesedésének mértékét, valamint a szaruhártya károsodásának súlyosságát. Feljegyeztük az alkalmazott terápiás módszereket, és felmértük a betegek állapotának változását a követési idő alatt.
Eredmények: A vizsgált időszakban nyolc ocularis graft versus host betegségben szenvedő beteg állt kezelésünk alatt (2 nő, 6 férfi, életkor 33,3±11,6 év). A szemfelszíni graft versus host betegség a transzplantáció után 5-36 hónappal jelent meg. A szemészeti érintettséget minden esetben megelőzte a szisztémás ocularis graft versus host betegség kialakulása. 5 betegnél a szemszárazság, 3-nál a fényérzékenység volt a vezető panasz. Subconjunctivális hegesedést 4, symblepharont 1 betegnél észleltünk. A corneafelszín enyhébb eltéréseit 4, súlyosabb károsodását 3 betegnél találtuk. A kezelésként a könnypótláson túl saját savó cseppet, fluorometholon-tartalmú szemcseppet, könnypontdugót, terápiás kontaktlencsét, illetve cyclosporintartalmú szemcseppet alkalmaztunk. A fél évtől 7 évig terjedő követési idő alatt betegeinknél a szemfelszín állapota javult, illetve különböző súlyossági stádiumban stabilizálódott, egyiküknél késői szövődményként bakteriális corneafekély kapcsán teljes limbális őssejt-elégtelenség következett be.
Következtetések: Ha az ocularis graft versus host betegséget időben, a kezdeti stádiumban felismerjük és a beteget megfelelő kezeléssel látjuk el, a beteg komfortérzete jelentősen növelhető és a szemfelszín állapota stabilizálható. Későn felfedezett és gondozásba vett betegeknél irreverzibilis károsodás következhet be, ami az életminőséget jelentősen rontja.
Keywords
ocular surface, allogenic haematopoetic stem cell transplantation, graft versus host disease, dry eye, cicatrizing chronic conjunctivitis
Kulcsszavak
szemfelszín, allogén hemopoetikus őssejt-transzplantáció, graft versus host betegség, száraz szem, hegesedéssel járó krónikus conjunctivitis
Bevezetés
Az elsősorban malignus vérképzőszervi betegségekben alkalmazott allogén hemopoetikus őssejt-transzplantáció lényege, hogy donor csontvelőből, perifériás vérből, vagy köldökzsinórvérből származó hemopoetikus őssejteket juttatnak a recipiens szervezetbe. Az őssejtekkel együtt immunkompetens sejtek is bejutnak, az ezek által kiváltott immunreakció következtében jöhet létre a graft versus host betegség (graft versus host disease, GVHD).
Megkülönböztetünk akut és krónikus GVHD-t. Az akut graft versus host reakció célpontjai a hámsejtek. A NIH Consensus Conference definíciója szerint akut a GVHD, ha 100 napon belül bőr, gasztrointesztinális, illetve májérintettség alakul ki, de a 100 napon túl megjelenő GVHD is akutnak tekintendő, ha krónikus GVHD jelei nem láthatók. Krónikus GVHD nem csak a hámsejteket támadja meg, és bármely szervet károsíthatja. Krónikus GVHD-ben hiányoznak az akut GVHD jellemzői, vagy a két folyamat párhuzamosan zajlik (1, 2).
Az ocularis GVHD az allogén hemopoetikus őssejt-transzplantációban részesülők 40%-60%-ában alakul ki (3). Elsősorban a krónikus GVHD-hoz csatlakozik, az ebben szenvedők 50-80%-ánál fordul elő (4, 5). A GVHD a szemfelszínt részben közvetlen módon támadja a conjunctivában kialakuló akut, illetve krónikus gyulladás és fibrosis útján, illetve a corneahám károsításával.
Ugyanakkor közvetett módon rontja a szemfelszín állapotát a súlyos szemszárazság, amit a könnymirigy és a Meibom-mirigyek GVHD-ja és a kehelysejtek pusztulása együttesen idéz elő (3, 5, 6). A szemet és a többi szervet érintő betegség lefolyása, súlyossága nem mindig egyezik, sőt, a szemészeti megbetegedés önállóan is bekövetkezhet. Bár szemészeti GVHD része lehet katarakta, episcleritis, scleritis, posterior scleritis, anterior uveitis, vitritis, és serosus chorioidealeválás is, az esetek túlnyomó többségében a szemfelszín károsodása következik be.
Célkitűzés
Annak bemutatása, hogy ocularis graft versus host betegség miatt gondozott betegeinknél milyen kórtörténetet ismertünk meg, milyen diagnosztikus és kezelési módszereket alkalmaztunk, és hogy alakult a szemfelszín állapota a megfigyelési idő alatt.
Betegek és módszerek
Retrospektív tanulmányunkban a 2013. és 2022. február között klinikánk szemfelszíni ambulanciáján megfordult, szemfelszíni graft versus host betegségben szenvedő páciensek adatait dolgoztuk fel a Medsol és EESZT-rendszerben rögzített adatok alapján. A hemopoetikus őssejtátültetéssel kapcsolatban feljegyeztük az átültetést szükségessé tevő alapbetegséget, az életkort az átültetés idején, és hogy ki volt a donor (családtag vagy idegen), és milyen típusú őssejt transzplantációja történt. A szisztémás GVHD kapcsán rögzítettük azt, hogy az átültetés után mikor jelentek meg az első tünetek, és melyik szervek voltak érintettek. A szemfelszín GVHD-jára vonatkozóan feljegyeztük, hogy mennyi idő telt el a transzplantáció, illetve a szisztémás GVHD után az első tünetek megjelenéséig, és hogy a betegek milyen panaszokról számoltak be. A Medsolban rögzített státuszok alapján összegyűjtöttük a szemszárazságra utaló tüneteket (alacsony könnymeniscus, a könnyfilm szemcsézettsége, ha Schirmer-vizsgálat történt, annak alacsony volta, műkönnyhasználat, a szaruhártyafelszín szurkáltsága, filamentumok, szemfelszíni keratinizáció), és a blepharitis jeleit (szemhéjszél egyenetlensége, teleangiectasiák, hyperaemia, eldugaszolódott Meibom-mirigy kivezető csövek, alacsony könnyfilm-felszakadási idő). A kötőhártya állapotát az enyhe vagy kifejezett belövelltség, illetve a hegesedés jelenlétével, illetve ezek mértékével jellemeztük. A szaruhártya károsodását is rangsoroltuk súlyosság szerint: enyhének vettük a hám szurkáltságát, filamentumok jelenlétét, súlyosnak, ha nem gyógyuló hámhiány, conjunctivalizáció, illetve a mélyebb rétegek érintettsége alakult ki. Feljegyeztük a követés alatt megállapított legrosszabb és az utolsó kontrollon észlelt korrigált visust (Kettesy-tábla). Összegyűjtöttük az alkalmazott terápiás módszereket, és felmértük a betegek állapotának változását a követési idő alatt.
Eredmények
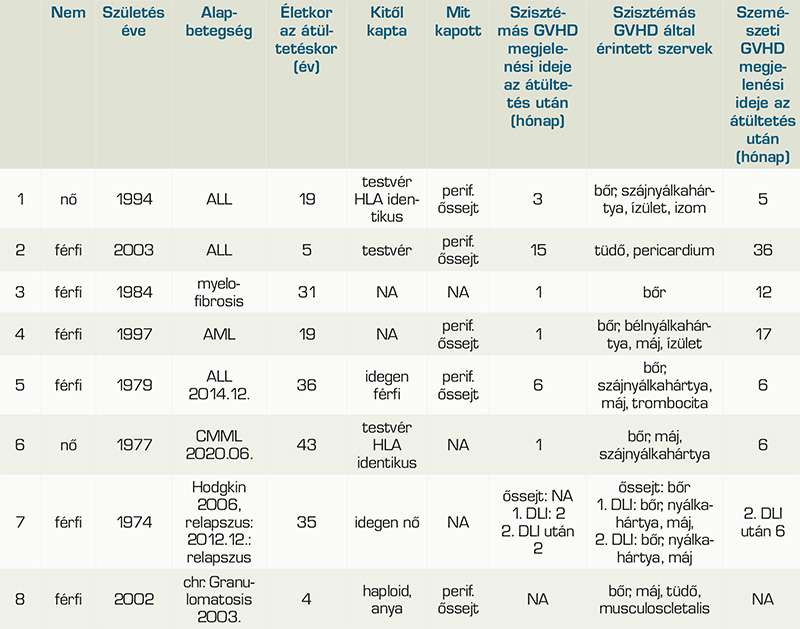
A vizsgált időszakban nyolc ocularis GVHD-ban szenvedő beteget, 6 férfit és 2 nőt kezeltünk mindkét szem érintettsége miatt. A betegek jelenlegi életkora 19 és 48 év között van (33,3±11,6). Az alapbetegségek között akut limfoid leukémia, akut mieloid leukémia, krónikus myelomonocytás leukémia, myelofibrosis, Hodgkin-lymphoma, és krónikus granulomatosis szerepelt. Az életkor az őssejtátültetés idején 4 és 43 év között változott. Az ismert esetekben perifériás vér őssejtek átültetése történt. A demográfiai adatokat részletesen az 1. táblázatban tüntettük fel.
A szemfelszíni GVHD a transzplantáció után 5-36 hónappal jelent meg. A szemészeti érintettséget minden esetben megelőzte a szisztémás GVHD kialakulása, az első szisztémás GVHD-s megjelenéstől számítva 2-21 hónappal alakult ki az ocularis GVHD. A szemfelszín megbetegedése a krónikus szisztémás GVHD-val párhuzamosan zajlott egy eset (4. eset, ld. 1. táblázat) kivételével, ahol csak akut szisztémás GVHD jelentkezett, a krónikus GVHD-ban egyedül a szemfelszín vett részt.
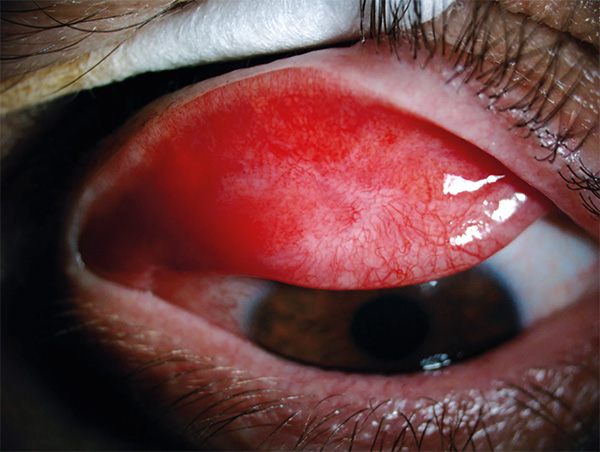
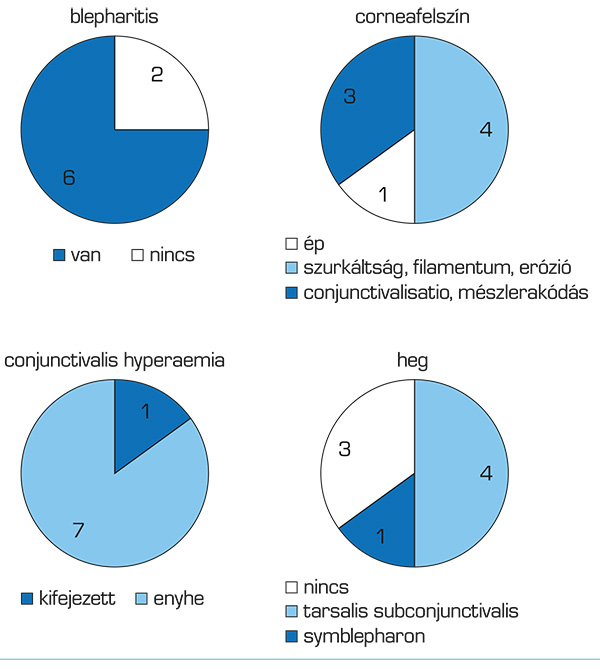
A szemészeti panaszok súlyossága változó volt. A különböző mértékű szemszárazságérzés dominált 5, fényérzékenység 3 betegnél, előfordult fájdalom és homályos látás, vagy kifejezett látásromlás is. A szemszárazság objektív jeleit (alacsony könnymeniscus, szemcsézett könnyfilm, alacsony Schirmer-érték, szurkált és/vagy filamentosus szaruhártyafelszín, keratinizáció, vagy újonnan szükségessé vált műkönnyhasználat) egy kivételével minden betegnél észleltük. Heges tarsalis kötőhártyát (1. ábra) 4 betegnél, symblepharont 1 betegnél találtunk. A conjunctiva belövelltségének és hegesedésének mértékét, a szemhéjszél/Meibom-mirigyek állapotát és a corneafelszín károsodásának mértékét a 2. ábrán mutatjuk be.
Minden beteg részesült általános immunszuppresszív kezelésben a szisztémás GVHD tüneteinek mérséklése céljából. Az alkalmazott gyógyszereket (szteroid, cyclosporin, tacrolimus, metothrexat, mikofenolat-mofetil, biológiai terápia) és fotoferezist a tünetek intenzitásának megfelelően adták. Önmagában a szemfelszíni megbetegedés miatt szisztémás kezelést a betegek nem kaptak.
A lokális kezelés alapja minden esetben a könnypótlás volt. Saját savót alkalmaztunk 5, fluorometholon-tartalmú szemcseppet szintén 5 betegnél. Könnypontdugót 2 beteg kapott, terápiás kontaktlencsét átmenetileg vagy folyamatosan 3 beteg viselt, illetve visel. Cyclosporintartalmú szemcseppet 2 esetben adtunk.
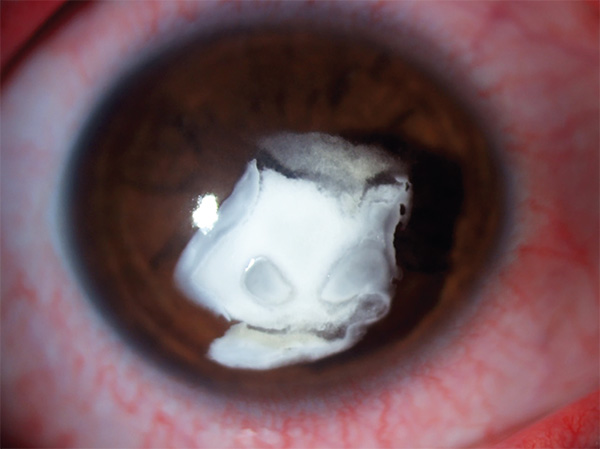
A betegeket fél évtől 7 évig terjedő ideig követtük nyomon. Egy mozgásában korlátozott beteg (7. eset) csak egy alkalommal jelent meg ambulanciánkon, csökkent könnytermelésen kívül szemfelszíni eltérés nem volt. A 7 követett beteg közül két, csak enyhe corneafelszíni károsodással kezelt betegnél (1. és 6. eset) romlás nem következett be, a panaszok tolerálhatók maradtak. 3 esetben (2., 4. és 5. eset), ahol filamentosus keratopathia, illetve hámhiány alakult ki, a kezelés hatására a panaszok (fényérzékenység, szemszárazságérzés) csökkentek, a filamentumok, illetve a hámhiány eltűntek. A 3. betegnél a cornea felszínes meszesedését (3. ábra) más intézményben eltávolították, ezután a corneastroma hegessé, erezetté vált. Két betegünknél, akik kisgyermekkorban estek át a hemopoetikus őssejtátültetésen, limbális őssejt-elégtelenség alakult ki. Egyikük (2. eset) bal szemén superior limbális keratoconjunctivitist követte a részleges limbuselégtelenség kialakulása, amelynek progressziója lokális cyclosporinkezelés mellett megállt. Másikuknál, a legrosszabb általános állapotban lévő, súlyos krónikus GVHD-ban szenvedő betegünknél (8. eset) 9 évvel az őssejt-átültetés után, gondozásunkba kerülésekor a jobb szemen már teljes cornealis őssejt-elégtelenség jeleit lehetett felfedezni. A bal szemen csaknem ép hám fedte a szaruhártyát, és ez az állapot kitartott 2021 őszéig, amikor egy bakteriális corneafekély kapcsán ezen a szemen is limbális őssejt-elégtelenség, teljes conjunctivalizáció következett be.
Megbeszélés
A hemopoetikus őssejtátültetés életmentő beavatkozás, és a graft versus host reakció folyamatára szükség van ennek sikeréhez, hiszen hozzájárul a maradék rosszindulatú sejtek elpusztításához, és elősegíti a transzplantált őssejtek befogadását (3, 5). Ugyanakkor a súlyos GVHD az életminőséget jelentősen rontó állapothoz vezethet.
Közleményünkben nyolc szemfelszíni graft versus host betegségben szenvedő betegünkről számolunk be. A szemfelszíni GVHD felismerését minden esetben segítette, hogy egyéb szervek GVHD-s megbetegedése már ismert volt a szemtünetek megjelenésekor. Kifejezett, újonnan megjelenő szemszárazságérzés – mint jellegzetes tünet – 5 betegnél jelezte a könnymirigy és Meibom-mirigyek GVHD-jának megjelenését. Közülük 4 esetben ezt a réslámpás vizsgálat, illetve a könnytermelés mérése is alátámasztotta. A 3 nem szemszárazság panasszal jelentkező betegnél – közülük a két gyermeknél – a vezető panasz a fényérzékenység volt. Az ő esetükben a diagnózist a heges, hyperaemiás conjunctiva, illetve a megviselt (szurkált, filamentosus, hámhiányos, illetve conjunctivalizált) corneafelszín tette egyértelművé.
Az International Chronic Ocular GVHD Consensus Group (7) többek között a cornea fluoreszcein-festődését veszi figyelembe a súlyosság megállapításánál. A betegeink szemfelszíni GVHD-ja egy kivételével minden esetben középsúlyosnak, illetve súlyosnak minősíthető, minthogy a szaruhártyahám károsodása a szurkáltságtól a filamentosus keratopathián át a nem gyógyuló hámhiányig, mészlerakódásig, illetve részleges vagy teljes conjunctivalizációig terjedt. A cornea érintettségének következményként a nyolc betegből négyben alakult ki legalább az egyik szemen tartós látásromlás. Mivel az ocularis GVHD kezdeti stádiumában elindított adekvát kezeléssel a gyulladás jelentősen mérsékelhető, és így a hegesedés és a cornealis komplikációk megelőzhetők, a German–Austrian–Swiss Consensus Conference a hemopoetikus őssejtátültetésen átesett betegek rendszeres szemészeti szűrését javasolja a panaszmentes esetekben is (4).
A GVHD kezelésének célja a gyulladás csökkentése szisztémás és helyi immunszuppresszió segítségével, és így a további károsodások megelőzése. Ugyanakkor a graft versus host reakciónak pozitív hatásai – a kemoterápia után esetlegesen megmaradt tumorsejtek elpusztítása és a transzplantált sejtek befogadása ellen ható recipiens immunreakció gyengítése – hozzájárulnak az őssejtátültetés sikeréhez. Ezért amennyiben lehetséges, a szisztémás immunszuppresszióval szemben előnyben kell részesíteni a lokális kezelést. Ha viszont a beteg más szervrendszerek érintettsége miatt szisztémás immunszuppresszív terápiát kap, az jó hatású a szemfelszíni gyulladásra is.
A szemfelszín állapotának javítása egyrészt a szemszárazság enyhítésével érhető el. Ezért a kezelés fontos eszközei a tartósítószer-mentes műkönny, a konzerválószer-tartalmú lokális készítmények kerülése, a könnypont elzárása, a szemhéjtoalett, a szisztémás doxycyclin és omega-3 zsírsav. A saját savó szemfelszíni GVHD-ban jelentősen képes növelni a beteg komfortérzetét, javítja a szemfelszín állapotát. A gyulladás csökkentése szteroid, illetve cyclosporintartalmú szemcsepp alkalmazásával a másik fontos eleme a terápiának. A betegek rendszeres kontrollt, folyamatos gondozást igényelnek (3, 5). Betegeink esetén az alkalmazott folyamatos intenzív lokális kezelés segítségével az állapot stabilizálódása, illetve a filamentumoktól és eróziótól mentes állapot fenntartása elérhető volt.
Műtéti beavatkozást egy esetben sem végeztünk, nem volt szükség amnionmembrán felvarrására sem a cornea hámosodásának elősegítésére. Rehabilitációs célú műtétek (symblepharolysis, limbális őssejtátültetés, szaruhártya-átültetés) kimenetele szemfelszíni GVHD-ban meglehetősen kérdéses további gyulladást provokáló hatásuk miatt.
Két betegünk kisgyermekkorban esett át hemopoetikus őssejtátültetésen. Bár irodalmi adatok szerint az ocularis GVHD gyermekeknél ritkább, mint felnőtteknél, azonban a malignus lefolyású krónikus szisztémás GVHD ebben a korosztályban hajlamosít a szemfelszín megbetegedésére, amit elsősorban az őssejtátültetést megelőző intenzív kemoterápiás kezelésnek tulajdonítanak (8). A súlyos krónikus GVHD a mi gyermekbetegeinknél a tüdőt, a pericardiumot, illetve a musculosceletalis rendszert érintette, ezek funkcióját jelentősen rontó következményekkel járt. A szemfelszín érintettsége is náluk volt a legsúlyosabb, amelynek következtében irreverzibilis elváltozás, a limbuselégtelenség alakult ki. Ehhez nyilván az is hozzájárult, hogy a rossz, sokszor életveszélyes általános állapotuk miatt nem fordult a figyelem a szemészeti megbetegedés irányába a kezdeti stádiumban. A két gyermek szemészeti állapotát is stabilizálni lehetett hosszú időn keresztül.
Következtetések
Összefoglalásként azt mondhatjuk, hogy ha az ocularis graft versus host betegséget időben, a kezdeti stádiumban felismerjük és a beteget megfelelő kezeléssel látjuk el, a beteg komfortérzete jelentősen növelhető és a szemfelszín állapota stabilizálható. Későn felfedezett és gondozásba vett betegeknél irreverzibilis károsodás következhet be, ami az életminőséget jelentősen rontja.
Nyilatkozat
A szerzők kijelentik, hogy az eredeti közleményük megírásával kapcsolatban nem áll fenn velük szemben pénzügyi vagy egyéb lényeges összeütközés, összeférhetetlenségi ok, amely befolyásolhatja a közleményben bemutatott eredményeket, az abból levont következtetéseket vagy azok értelmezését.
Irodalom
1. Filipovich A, Weisdorf D, Pavletic S, Socie G, Wingard J, Lee S, et al. National Institutes of Health consensus development project on criteria for clinical trials in chronic graft-versus-host disease: I. Diagnosis and staging working group report. Biol Blood Marrow Transplant 2005; 11(12): 945–56. https://doi.org/10.1016/j.bbmt.2005.09.004
2. Jagasia M, Greinix H, Arora M, Williams K, Wolff D, Cowen E, et al. National Institutes of Health Consensus Development Project on Criteria for Clinical Trials in Chronic Graft-versus-Host Disease: I. The 2014 Diagnosis and Staging Working Group report. Biol Blood Marrow Transplant 2015; 21(3): 389–401. http://dx.doi.org/10.1016/j.bbmt.2014.12.001
3. Mannis M, Holland E. Cornea. Fundamentals, Diagnosis and Management. 5th Edition: Elsevier Health Sciences; 2021.
4. Dietrich-Ntoukas T, Cursiefen C, Westekemper H, Eberwein P, Reinhard T, Bertz H, et al. Diagnosis and treatment of ocular chronic graft-versus-host disease: report from the German-Austrian-Swiss Consensus Conference on Clinical Practice in chronic GVHD. Cornea 2012; 31(3): 299–310. https://doi.org/10.1097/ICO.0b013e318226bf97
5. Nair S, Vanathi M, Mukhija R, Tandon R, Jain S, Ogawa Y. Update on ocular graft-versus-host disease. Indian J Ophthalmol 2021; 69(5): 1038–50. https://doi.org/10.4103/ijo.IJO_2016_20
6. Füst Á, Nagy Z. Graft versus host betegség a szemfelszínen. Orvostovábbképző Szemle 2022; 29(3): 41–5.
7. Ogawa Y, Kim S, Dana R, Clayton J, Jain S, Rosenblatt M, et al. International Chronic Ocular Graft-vs-Host-Disease (GVHD) Consensus Group: proposed diagnostic criteria for chronic GVHD (Part I). Sci Rep 2013; 3: 3419. http://dx.doi.org/10.1038/srep03419
8. Jeppesen H, Kielsen K, Siersma V, Lindegaard J, Julian H, Heegaard S, et al. Ocular graft-versus-host disease and dry eye disease after paediatric haematopoietic stem cell transplantation – incidence and risk factors. Bone Marrow Transplant 2022; 57(3): 487–98. https://doi.org/10.1038/s41409-022-01564-2
